James T.Rutka(鲁特卡)教授曾任世界神经外科学院院长,目前是世界神外专业杂志《Journal of Neurosurgery》主编,30多年来深耕儿童神外研究,带领团队不断突破,从脑瘤分子分型、精准治疗、新药治疗、微创治疗,为全球神经外科疑难病患儿带来希望,他发表研究《Pediatric Sinonasal Undifferentiated Carcinoma:Case Report and Literature Review》(儿童鼻腔鼻窦未分化癌:病例报告与文献综述),以下是研究简述。
01
PART
研究背景
鼻腔鼻窦未分化癌(SNUC)是一种罕见的、侵袭性的恶性肿瘤,起源于鼻腔和鼻旁窦。鼻腔未分化癌由Frierson等人于1986年首次报道,自那以后文献中报道的病例不足100例。先前有一例儿科病例报道,涉及一名印度的12岁男孩。SNUC在组织学上被归类为起源于鼻窦施耐德氏膜或鼻外胚层的神经内分泌癌谱系的一部分。在此,我们报道仅第二例儿童期发病的SNUC病例,涉及一名青少年,其病变起源于鼻腔并延伸通过鼻旁窦进入前颅窝和大脑。
02
PART
病例报告
一名15岁、既往健康的男性,因额部头痛加剧、恶心、呕吐和疲劳两周病史就诊。家属注意到在就诊前一个月出现言语失控和非典型行为。他的神经系统检查显示双侧视乳头水肿,无其他局灶性缺损。所有血液检查均正常,血清生殖细胞肿瘤标志物也为阴性。脑和鼻旁窦的计算机断层扫描(CT)和磁共振成像(MRI)扫描显示,右侧有一个5.5 x 4.4 x 5.6厘米的肿块,起源于鼻腔、筛窦和蝶窦。它已侵蚀筛板进入前颅窝。该肿块在CT扫描上未钙化(图1),与脑组织等密度,伴有不均匀的对比增强。该肿块在T1和T2加权MR图像上(图2、3、4)与脑组织等信号,并在钆增强后显示不均匀强化。注意到周围有血管源性脑水肿和占位效应。脊柱MRI未见转移证据。
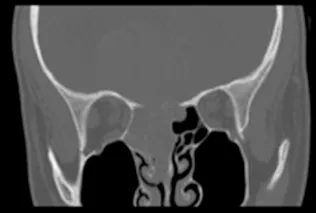
图1:冠状位CT扫描骨窗图像,显示肿瘤起源于右侧鼻腔,延伸至筛窦并通过筛板进入前颅窝。注意肿瘤团块内无钙化。
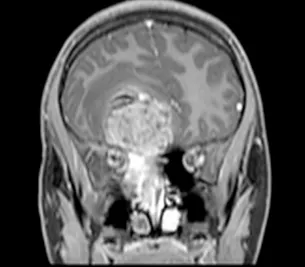
图2:冠状位T1加权钆增强MRI扫描,证实了起源于鼻腔并延伸至前颅窝的大肿瘤团块的发现。对额叶下部的占位效应和轻微的中线移位是明显的。
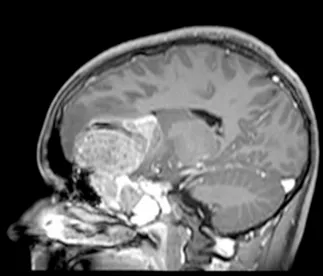
图3:矢状位T1加权钆增强MRI扫描,显示肿瘤团块从鼻旁窦侵蚀进入前颅窝。
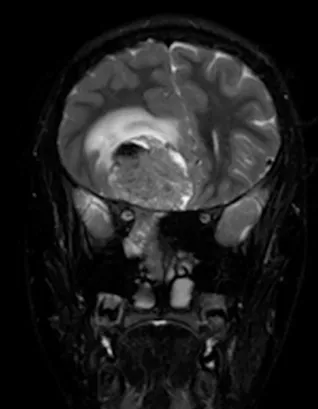
图4:冠状位T2加权MRI扫描,证实了颅内肿瘤成分的不均匀实性和囊性性质。病灶周围水肿以及肿瘤相关的中线移位也清晰可见。
03
PART
手术过程
设计了一个鼻内镜联合双额开颅的手术计划来处理这个病变。最初,采用右侧内镜经鼻入路获取组织进行病理诊断。在活检确诊SNUC后五天后,患者被再次送回手术室,以切除位于颅内和鼻旁窦的剩余肿瘤。进行了以中线右侧为中心的双额开颅术。从右侧通过大脑半球间前裂进行解剖,直到在前颅窝底上方约4厘米处遇到肿瘤。
该病变血管丰富,在使用超声吸引器在与正常脑组织交界处围绕肿瘤建立平面后,用吸引器切除。到达颅底时,可见肿块侵蚀筛板进入筛窦。使用内镜从上方和下方切除鼻窦中的肿瘤残余物。使用一块额颅骨分层骨移植片来修复前颅底的孔洞。然后使用带血管的骨膜组织瓣来支持硬脑膜缺损的闭合,并辅以浓缩的纤维蛋白组织胶。
组织学检查显示为实性片状的低分化细胞,核质比高,可见广泛浸润的小梁和泡状核,伴有中度的有丝分裂活性(图5)。
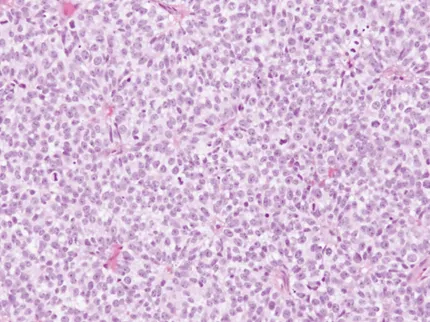
图5:H&E染色切片显微照片(40倍放大),显示实性片状的泡状核,高核质比,中度有丝分裂活性,以及明显的凋亡和坏死区域。
还可见明显的凋亡和坏死区域,以及带有纤维黏液样变区域的血管化肿瘤间质。免疫组织化学显示波形蛋白和广谱细胞角蛋白染色阳性(图6)。
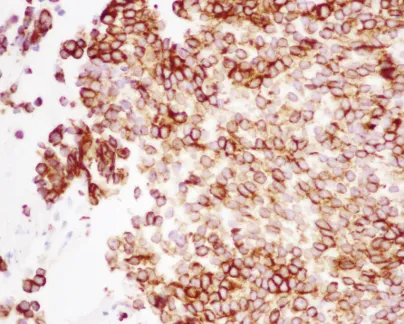
图6:显微照片(40倍放大),显示广谱细胞角蛋白弥漫阳性免疫组织化学染色。
Epstein Barr病毒(EBV)原位杂交为阴性。电子显微镜显示为原始小细胞和较大的上皮细胞的混合物,上皮细胞具有形成良好的长细胞间连接。诊断为SNUC。术后,他的神经系统状况无变化,头痛在术后第十天出院回家前显著减轻。术后两天进行的磁共振成像显示肿瘤大体全切。他接受了辅助分割放疗,包括对肿瘤床和周围边缘进行的30次分割共6000 cGy的照射。同时给予了顺铂化疗。术后十二个月,患者神经系统状况良好,无影像学或临床证据表明肿瘤复发(图7、8)。
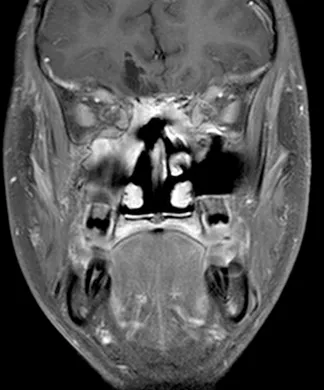
图7:冠状位T1加权钆增强MRI扫描,显示鼻腔和颅内肿瘤成分的大体全切。注意额叶占位效应的解决和肿瘤床无对比增强。
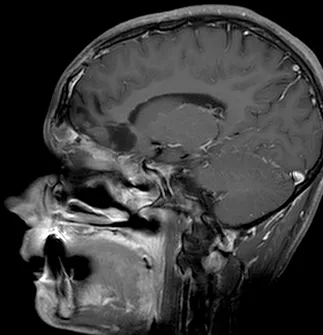
图8:矢状位T1加权钆增强MRI扫描,显示鼻旁窦和前颅窝肿瘤的大体全切。注意额叶无占位效应,肿瘤腔内无对比增强。
04
PART
讨论
由于病例稀少,对于SNUC的治疗尚无共识。目前的文献倾向于采用多模式方法,包括手术切除、辅助放疗和化疗的结合。最初仅用放疗或放疗结合化疗治疗SNUC的研究报告了令人沮丧的患者结局,平均生存期为一年。最近评估手术联合新辅助或辅助放化疗疗效的研究得出了更乐观的结果。在涉及弗吉尼亚大学治疗的19名成年患者的最大病例系列之一中,标准治疗方案包括诱导化疗(顺铂和依托泊苷或环磷酰胺、多柔比星和长春新碱),随后进行术前放疗(25次分割,5000-5400 cGy)和手术切除。健康状况不佳或患有被认为无法手术切除的肿瘤的患者接受了姑息性放疗或放化疗。十名接受放化疗后手术的患者两年生存率为64%,而九名非手术治疗的患者为25%。在文献中唯一报道的另一例儿科病例中,治疗包括大体全切术后放疗。该患者在诊断后六个月无症状。我们的患者接受了类似的治疗,并增加了化疗,在诊断后六个月无临床或影像学肿瘤复发证据。
我们的病例可能代表了一个罕见的、散发的儿科SNUC病例,其病因和发病机制尚不清楚。可以说,更多病例的报道将有助于阐明病因学关联。我们呈现了一例罕见的伴有症状性颅内延伸的儿科SNUC病例。据我们所知,这是迄今为止报道的仅第二例儿科SNUC病例,其发病机制仍然难以捉摸。由于诊断的罕见性,这些肿瘤的治疗仍然是一个挑战。为了实现局部疾病控制和最大化生存期,我们推荐采用多模式治疗方法,包括根治性手术切除辅以辅助或新辅助化疗或放疗。SNUC的罕见性意味着需要多中心努力来确定这种疾病的最佳治疗方法。
05
PART
关于作者





