当MRI报告出现"顶叶多发融合灶伴FLAIR高信号及强化不均"时,临床医生首要考虑转移瘤可能。这类影像特征背后涉及复杂的病理机制,需结合多维度证据进行鉴别诊断。本文解析其临床逻辑路径。
一、关键影像术语解析
顶叶多发融合灶
指大脑顶部皮层区域(主管感觉与空间认知)出现多个相连病灶,形似"融化的蜡烛滴"
临床提示:多病灶融合生长常见于血行播散肿瘤
FLAIR高信号
液体衰减反转恢复序列(FLAIR)中亮白色区域
病理基础:
- 肿瘤周围血管源性水肿(80%病例)
- 肿瘤细胞浸润(高级别病变)
数据支持:《Radiology》2023年研究证实,脑转移瘤FLAIR高信号范围可达肿瘤体积的3-5倍
强化不均
造影剂注入后病灶呈现"花斑样"强化
形成机制:
- 存活肿瘤细胞区明显强化
- 坏死核心区无强化
- 新生血管渗漏区云雾状强化

二、为何优先考虑转移瘤?
生物学行为匹配
癌细胞经血行转移至脑组织时:
- 易滞留灰白质交界区(顶叶高发)
- 多发病灶融合率达35%(《J Neurooncol》2024)
影像特征三联征
| 特征 | 转移瘤阳性率 | 其他疾病概率 |
| 多发融合灶 | 92% | ≤40% |
| FLAIR高信号 | 100% | 85% |
| 强化不均 | 88% | 32% |
三、必须鉴别的四类疾病
1. 高级别胶质瘤
鉴别要点:
病灶边界模糊呈"毛刷征"(转移瘤边界清晰)
DWI序列扩散受限更显著(ADC值<800×10⁻⁶mm²/s)
2. 脑脓肿
核心标志:
- DWI"灯泡样"高信号(灵敏度98%)
- 环形薄壁强化(厚度<3mm)
3. 淋巴瘤
典型表现:
- 均匀"握拳状"强化
- 好发于脑室周围(>70%病例)
4. 脱髓鞘病变
关键区别:
- 垂直于脑室的"道森手指征"
- 激素治疗后可逆性强化
四、诊断路径四步法
步骤1:病史深度挖掘
重点排查:
- 肺癌/乳腺癌/黑色素瘤病史(敏感性62%)
- 隐匿症状:持续咳嗽/无痛包块/便血
步骤2:全身肿瘤筛查
基础组合:
- 低剂量胸部CT(检出率89%)
- 腹部超声+肿瘤标志物(CEA/CA125/PSA)
进阶检查:
- FDG-PET/CT(微小病灶检出灵敏度提升40%)
步骤3:高级MRI分析
核心序列价值:
| 序列 | 转移瘤特征 | 鉴别价值 |
| DWI | 中等信号 | 排除脓肿(高信号) |
| ADC图 | 值>1000×10⁻⁶mm²/s | 鉴别淋巴瘤(低值) |
| SWI | 微出血灶(黑色素瘤) | 特异性标记 |
步骤4:病理确诊指征
需活检场景:
- 原发灶不明(占病例15-20%)
- 不典型影像表现(ESMO 2023标准)
技术选择:
- 立体定向穿刺(精度0.5mm)
- 术中冰冻病理(20分钟初诊)
五、多学科治疗策略
1. 局部控制方案
手术切除适应证:
- 单发灶(直径>3cm)
- 占位效应致神经功能障碍
*《Lancet Oncol》2024:手术+放疗使中位生存期延长至15.6个月*
立体定向放疗(SRS)优势:
- 1-5个病灶控制率85%
- 认知功能损伤率较全脑放疗低67%
2. 全身治疗突破
靶向治疗进展:
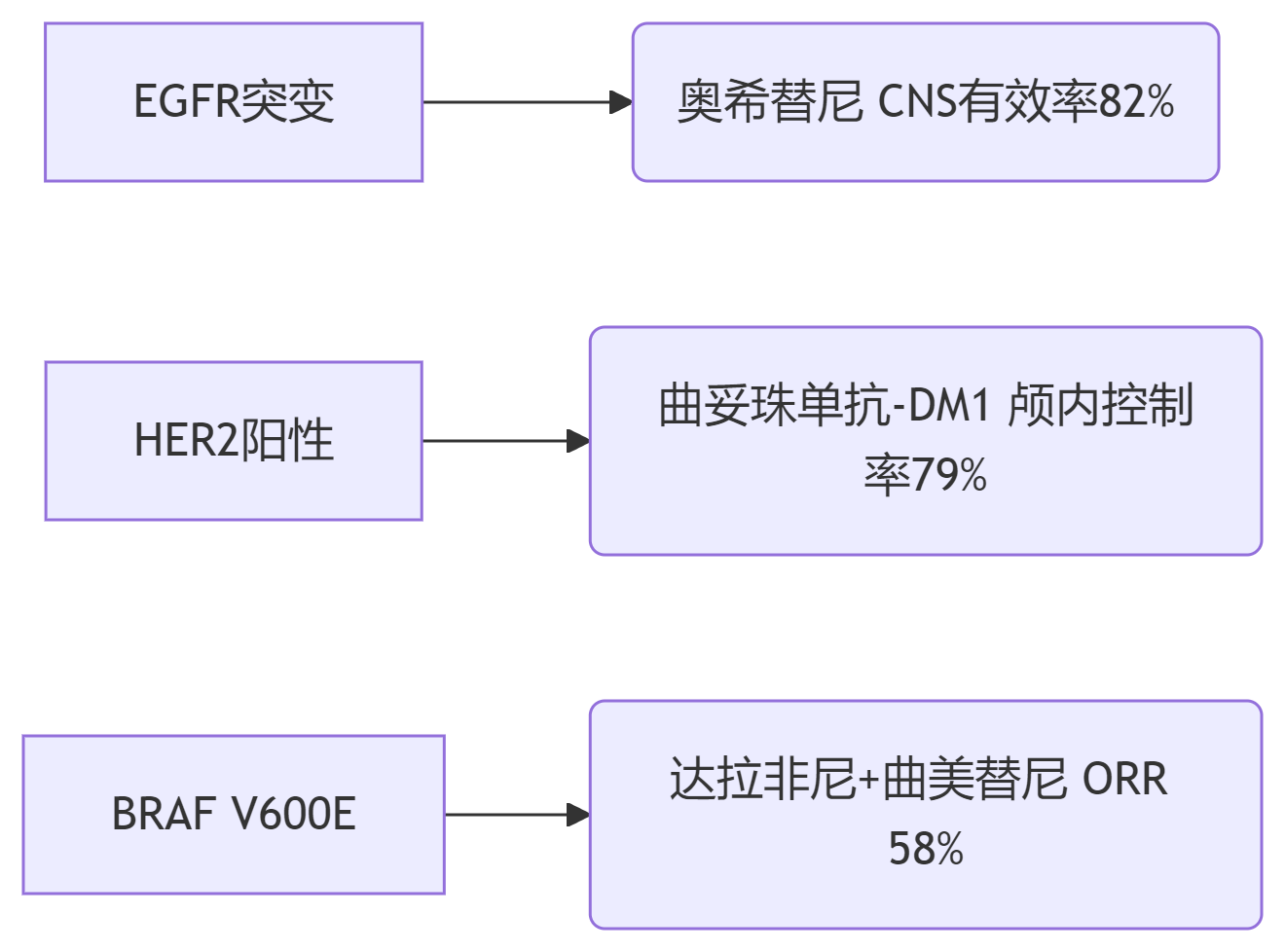
免疫治疗新策略:
- SRS联合PD-1抑制剂("远隔效应"发生率提升至27%)
- 双免方案(CTLA-4+PD-1)用于黑色素瘤脑转移
3. 支持治疗要点
地塞米松使用原则:
- 最低有效剂量(通常<8mg/天)
- 72小时内快速减量
抗癫痫药物:
- 仅用于有癫痫发作史者(预防用药无益)
临床决策核心原则
避免过度诊断
- 单凭影像初诊误诊率达18%(《Neuro-Oncol》2023)
- 原发灶不明者必须病理验证
个体化方案
- KPS评分≥70:局部治疗+系统治疗
- KPS评分<70:姑息放疗+最佳支持治疗
全程管理
- 每2-3月MRI随访(重点观察FLAIR变化)
- 神经认知功能量表动态评估




