忙碌之中突感“头痛炸裂”,医院一查竟是隐藏多年的“不定时炸弹”动脉瘤破裂,很快就人事不醒,进入ICU,颅内出血严重,瞳孔放大……人到中年,上有老,下有小,但因为突发一场疾病,疾病拿走你生命的全部,没有任何预兆,让你猝不及防,触目惊心。这类疾病中除了心血管病以外,另外一个的凶手,就是颅内动脉瘤。
高患病率、高破裂率、高死残率的“不定时炸弹
脑动脉瘤不是"肿瘤",而是脑血管畸形病变。脑动脉瘤的发生,是因为各种原因导致脑动脉壁薄弱,动脉壁像"吹气球"一样鼓起来,形状像"瘤",但实质上不是肿瘤。脑动脉瘤血管壁薄,在压力很高的动脉血的冲击下,这样的薄弱部分容易破裂,被称为装在脑袋里的“不定时炸弹”,一旦发生破裂出血,会引起剧烈头痛、呕吐或者颅压增高等症状,而且存在二次出血的风险,严重的时候可以引起昏迷,甚至生命危险。
国际脑血管搭桥手术专家——川岛明次教授

▪日本东京女子医科大学神经外科主任
▪脑血管搭桥手术专家
▪日本杰出的脑血管病手术专家
▪独自成功完成颅内外血管搭桥手术1100例,动脉瘤超900例,颈内动脉内膜剥脱术(CEA)超350例
STA-PCA搭桥术治疗PCA动脉瘤精彩案例交流
大脑后动脉(PCA)动脉瘤是一种少见的病变,在全部颅内动脉瘤中所占比例不到2%,大多数呈梭形。PCA动脉瘤(PCAA)由于独特的形态和位于大脑深层结构而形成。PCA起源于基底动脉(BA)末端,通过后交通动脉(PCoA)提供前循环的侧支血液供应。根据所涉及的节段,由于PCA动脉瘤的解剖位置较深。正确认识和理解PCA的显微外科解剖和血管区域是顺利合适治疗动脉瘤的基础。因此,选择最佳的治疗方式对于较顺利、较合适的治疗过程同样重要。
通过血管内介入或显微手术阻断近端载瘤动脉是一种治疗选择。但是,可能带来较高的缺血性卒中的风险。如果结合血管重建则可以合适防止并发症的发生。INC国际神经外科医生集团旗下组织世界神经外科顾问团(WANG)成员、国际脑血管搭桥手术教授、日本东京女子医科大学神经外科主任Akitsugu Kawashima(川岛明次)教授报道施行大脑后动脉P2段动脉瘤孤立术加与颞浅动脉(STA)搭桥术治疗PCA动脉瘤的经验,《Superficial Temporal Artery:Distal Posterior Cerebral Artery Bypass through the Subtemporal Approach:Technical Note and Pilot Surgical Cases》文章发表于2017年6月的《Operative Neurosurgery》杂志上。
川岛明次教授所在医疗中心自2012年9月至2014年10月期间收治3例位于大脑后动脉P2段的梭形PCA动脉瘤患者,均行颞下入路动脉瘤孤立术,加PCA远端血管搭桥重建术。
对于未破裂PCA动脉瘤患者,术前常规服用阿司匹林100mg/d1周。采取颞下入路开颅,腰大池引流50-100ml,可减少对颞叶牵拉。使用多普勒超声引导并标出颞浅动脉的额支或顶支位置;分离出10cm长的STA主干移植段后,延长切口至耳廓上方(图1)。将皮肌瓣上抬暴露Henle棘和颧弓根部。随后,向STA主干移植段插管,用肝素盐水冲洗。接着,颞部开颅形成5-6cm的骨瓣。以曲线形切开硬膜,牵拉颞叶暴露环池并释放脑脊液,此时腰大池引流呈关闭状。然后,暴露颞后动脉(PTA)和大脑后动脉P3段的近端。STA主干移植段至少10cm长,以防其吻合后扭曲缠绕。将STA与PCA的P3段或PTA起始处吻合。动脉吻合使用10-0单丝线间断缝合或9-0聚丙烯线连续缝合。确定吻合后PCA远端血流通畅。然后使用动脉瘤夹在动脉瘤的近端和远端夹闭载瘤动脉,完成动脉瘤孤立。
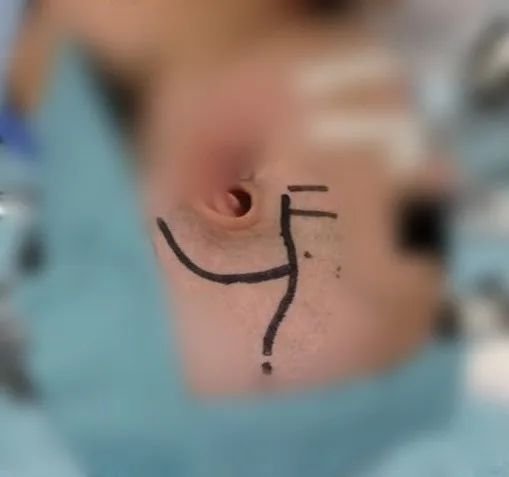
图1.皮肤切口。实线分别代表颞浅动脉顶支投影和耳廓上切口。
3例患者均成功实施动脉瘤孤立术和远端PCA血流重建术。3例患者STA-P3/PTA搭桥术后PCA远段血供充足,没有出现新的长期性神经功能缺损。术后1年随访时,STA-P3/PTA吻合口远段血供良好。
案例一:43岁男性--右侧梭形且部分血栓P2动脉瘤
43岁男性,诊断右侧P2梭形动脉瘤,伴有血栓形成,初期接受保守治疗。在随后11年的随访中,动脉瘤扩大至15毫米。尽管动脉瘤压入内侧颞叶,但患者仍然没有症状。考虑是动脉瘤逐渐增大,破裂风险较高,建议手术治疗。
▼PTA在动脉瘤远端分支(图2A和2B)。予以右侧颞下入路手术,切除梭状回的一小部分被软膜,暴露动脉瘤顶端。随后,暴露动脉瘤的近端和远端颈,并识别PTA和P3段。
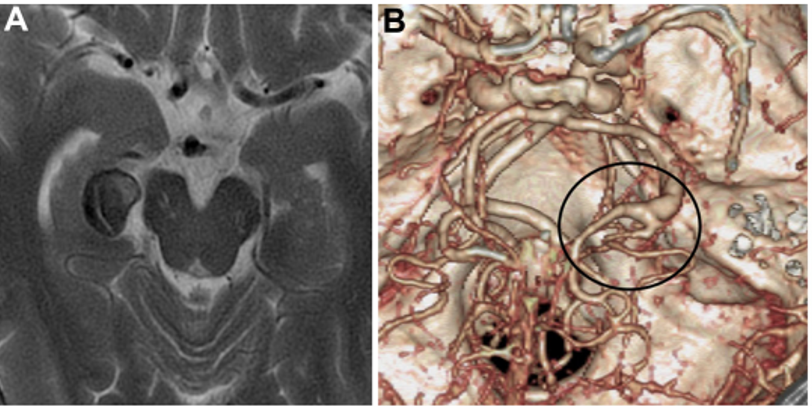
▼P3段被选为搭桥血管位置(图2C和2D)。如上所述,教授进行了STA-P3旁路手术并孤立动脉瘤。为了夹住动脉瘤,Kawashima教授使用了直长夹和有孔夹的组合,以避免P3段和PTA扭结。
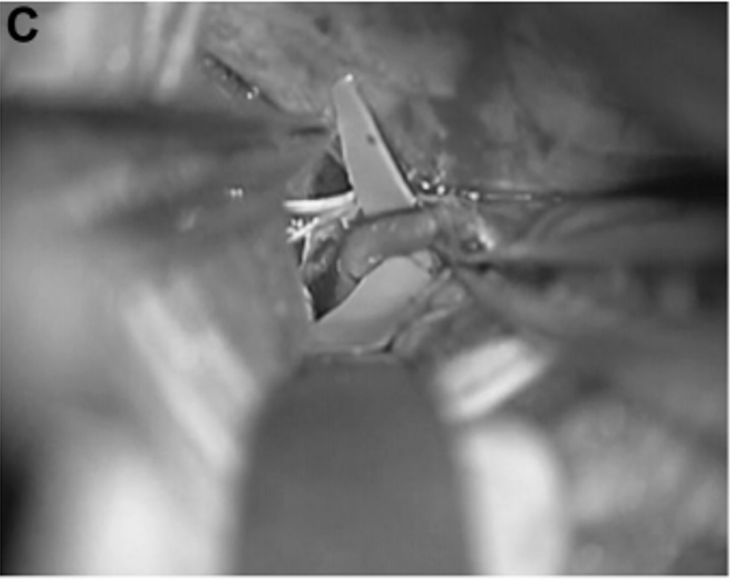
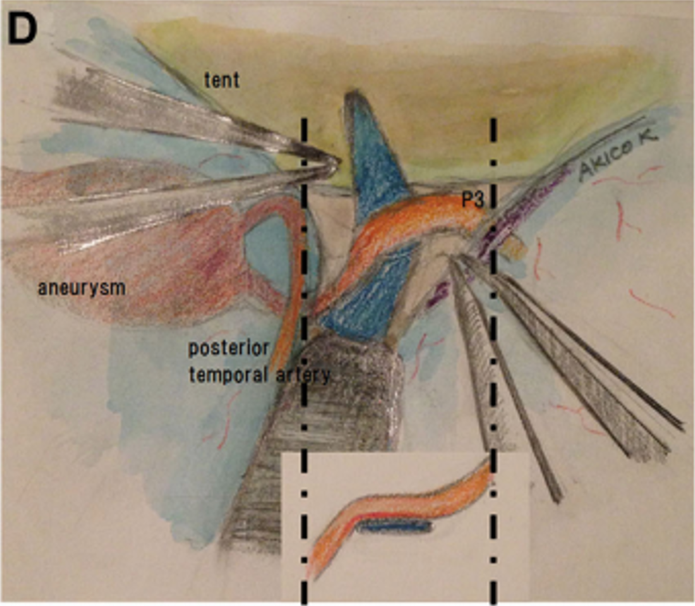
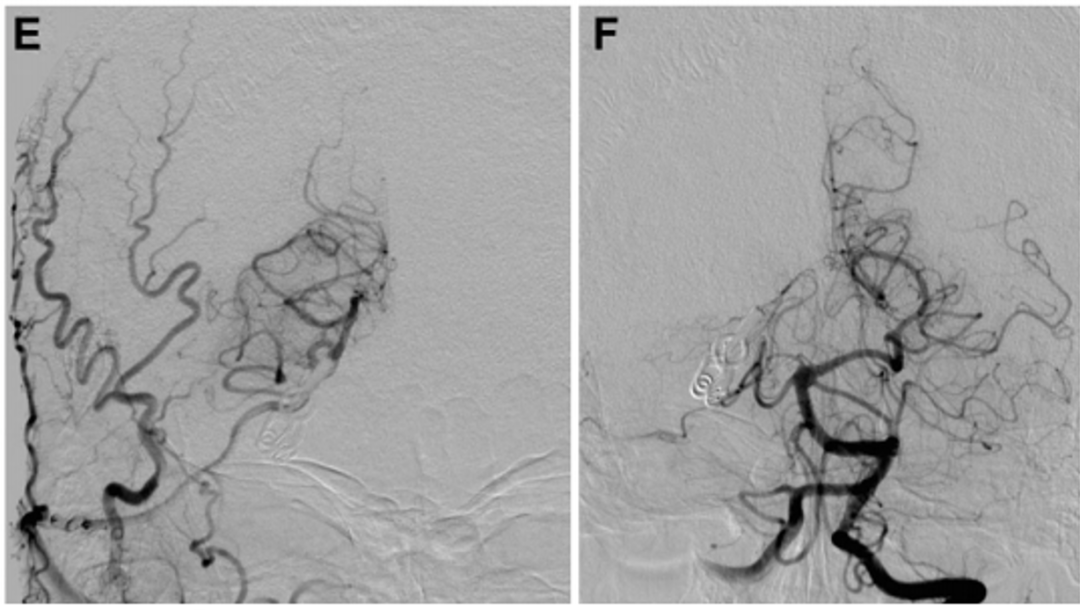
▼此后,通过吲哚菁绿荧光血管造影证实旁路、P3段和PTA的通畅。Kawashima教授打开动脉瘤以确保其完全闭塞并继续进行血栓切除术。患者出院时没有出现任何神经功能缺损,并且在1年随访时,旁路仍然通畅,并成功通过手术孤立了动脉瘤(图2E和2F)。
案例二:47岁男性--P1-P2夹层动脉瘤
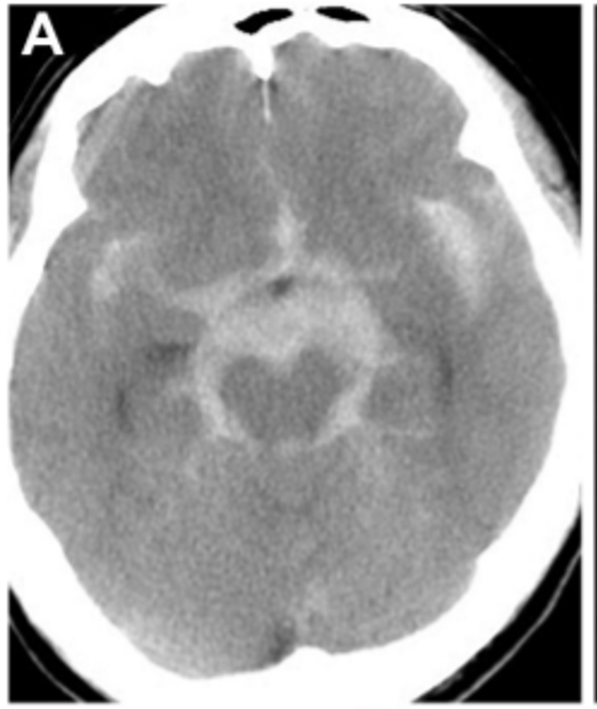
47岁男性,确诊蛛网膜下腔出血(Hunt-Hess和Kosnic 3级)(图3A)。初次就诊时,3D CTA或DSA未发现扩张或血管病变。
▼A、CT显示弥漫性蛛网膜下腔出血,是左侧脑桥前池增厚.
▼出血后18天的延迟血管造影显示左侧P1-P2段有一个不断增长的夹层动脉瘤,并具有狭窄特征(图3B)。
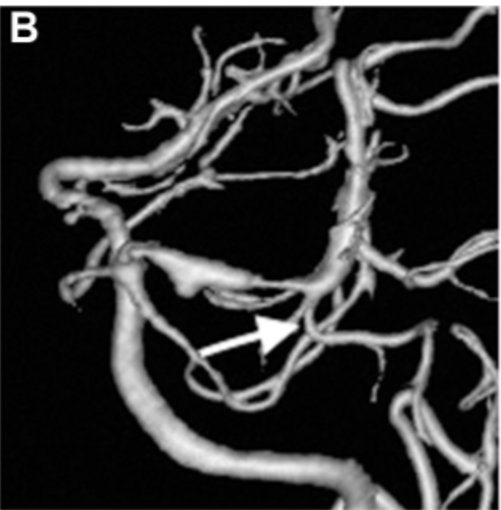
B,出血后18天,血管造影显示左侧P1-P2段扩张并具有狭窄征,PTA从狭窄病变的远端部分分支(箭头)。
▼20天,经左颞下入路进行动脉瘤鼓励术和STA-PCA搭桥重建手术。初期夹闭动脉瘤的近端部分,同时保留丘脑穿支动脉。动脉瘤的解剖区域延伸到P2段后部,就在PTA分支点之前。在本例中,选择PTA作为受体动脉,因为其口径和角度优于P3段进行吻合(图3C和3D)。
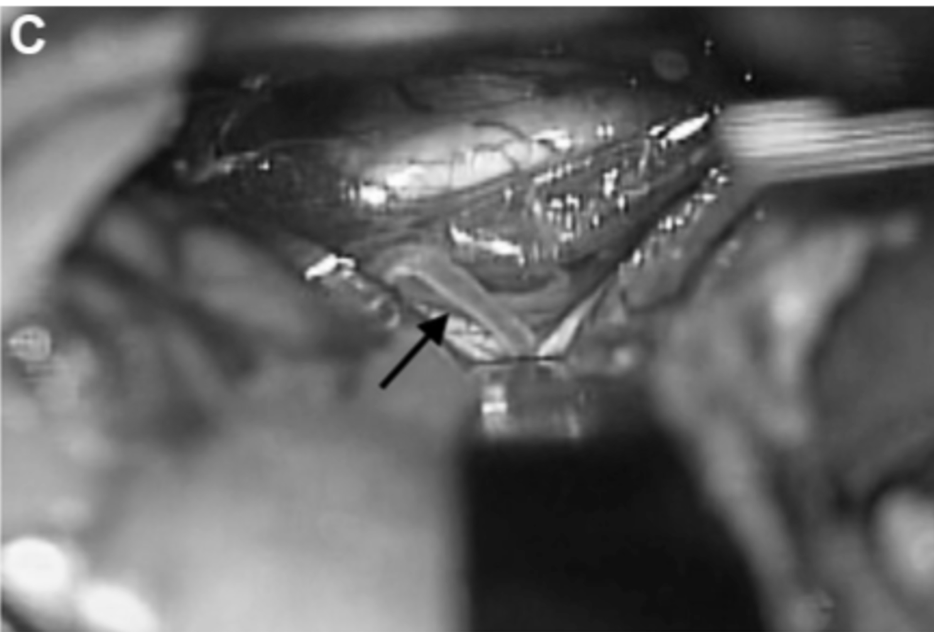
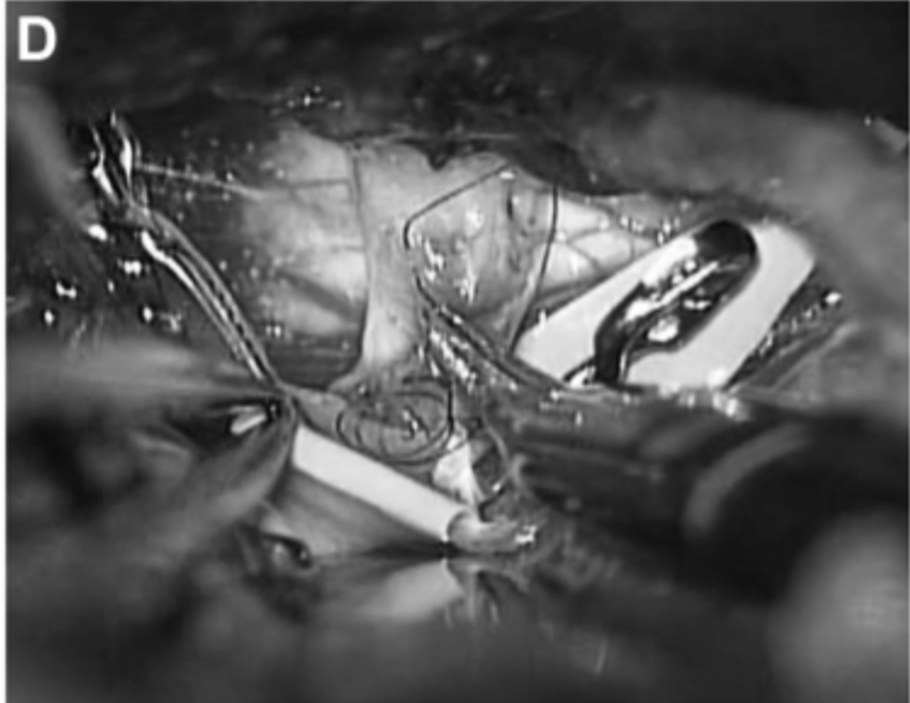
C、D,受体动脉的PTA(箭头)。通过左颞下入路缝合STA和PTA之间的吻合。
进行STA-PTA旁路手术后,Kawashima教授将远端夹子放置在夹层动脉瘤上,同时保留穿支。术后1周血管造影显示,通过旁路到达左侧PCA区域的血流良好,并且动脉瘤完全被排除(图3E)。两周后,患者出院回家,没有出现神经功能缺损。在1年随访中,患者改良Rankin评分为0,搭桥术仍然合适。
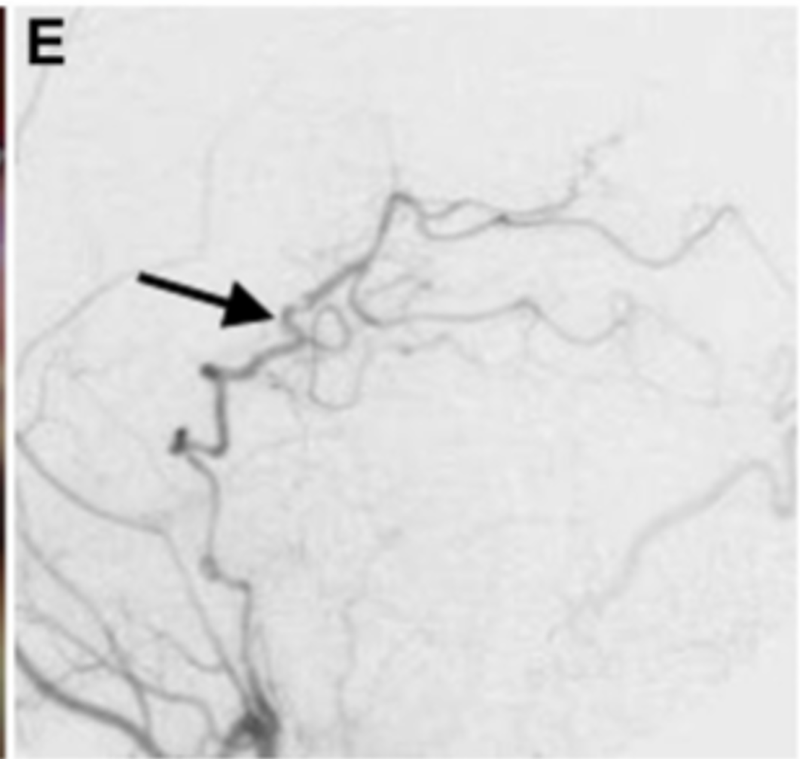
▼E:术后1周的颈外动脉血管造影显示整个左PCA的旁路血液供应良好(箭头)
案例三:55岁男性--左侧梭形P1-P2交界处动脉瘤
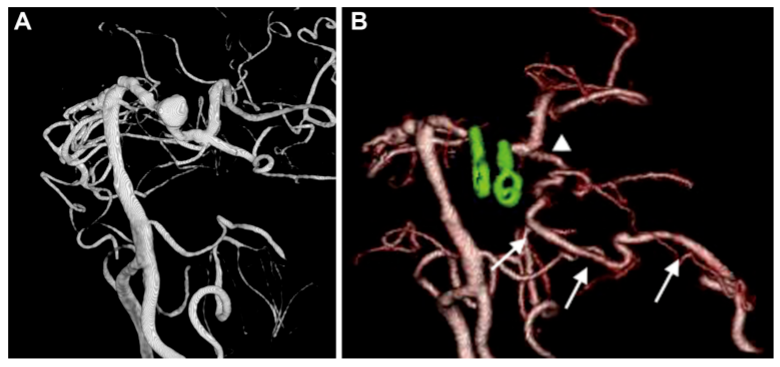
55岁男性,短暂性脑缺血发作和认知功能障碍,影像检查显示右侧颈内动脉严重狭窄,左侧P1-P2交界处梭形动脉瘤,大小10×12毫米。患者首先接受了右STA-MCA搭桥术,以预防血流动力学障碍。十月后,患者接受了梭形动脉瘤的治疗(图4A)。考虑到该患者的大小、位置、壁不规则性以及需要长期抗凝治疗等因素所致发生动脉瘤破裂的,予以进行二次手术。手术计划包括远端PCA的血运重建和通过颞下入路动脉瘤孤立术。鉴于P2远端段严重的动脉粥样硬化变化,选择PTA作为搭桥受体动脉。术后患者出现短暂性失语,1周后完全恢复。手术后1年进行的血管造影显示已排除动脉瘤且左侧PCA循环通畅(图4B)。
A,病例3术前3D-DSA显示位于左侧P1-P2交界处动脉瘤。B,术后3D CTA显示左侧PCA区血管穿支(箭头)和重建的PTA血管(箭头)的血流通畅。
动脉瘤的三种结局
其一为瘤破裂,就是动脉瘤破裂出血,导致蛛网膜下腔出血,神经损伤及死亡风险较高;
其二为瘤生长,就是动脉瘤在连续观察中发生动脉瘤大小上的明显变化,或形态上明显改变,具体说就是动脉瘤形态上一个方向上增长超过1mm,或二个垂直方向上各增长超过0.5mm,形态上由规则转为不规则;
其三为保持稳定,无破裂,无生长。
相较稳定而言,破裂与生长均为不稳定。稳定意味着,动脉瘤风险较低较小,它不会造成压迫症状,也不会破裂造成致命性、灾难性后果。而不稳定意味着,动脉瘤风险较高较大,它会造成压迫症状,有神经功能障碍,甚至会破裂造成致命性、灾难性后果。
大脑后动脉瘤破裂的影响因素较多:
蛛网膜下腔出血是大脑后动脉瘤破裂较常见的并发症,但并不是全部的动脉瘤都会破裂。普遍认为颅内动脉瘤的破裂与其位置、大小、吸烟及年龄有关,不同原因还能相互作用、相互影响。
①动脉瘤形态。动脉瘤形态是动脉瘤破裂的独自危险因素,对于瘤体形态不规则患者,破裂发生率越高;对于瘤体形态较为规则者,病情趋于稳
定,瘤体不易破裂。
②高血压。高血压是血流动力学改变的一种反映,血压增高将会增加颅内动脉分叉部位血管壁剪切力。同时,持续的高血压将会引起血管壁受损,增加动脉瘤的发生、发展。既往研究表明高血压能引起动脉壁结构发生变
化,引起血管活性物质失衡,增加机体炎症反应,影响受损血管修复,当血压达到的阈值后,则会引起动脉瘤破裂。
③脑血管病家族史。脑血管病家族史对动脉瘤破裂的影响相对较小,但是对于伴有脑血管病家族史患者动脉瘤破裂发生率高于无脑血管病家族史者。




