当脑内细胞异常克隆生长时,就会形成脑瘤。脑肿瘤可分为恶性(癌变)和良性(非癌变)。恶性肿瘤可以是原发性或继发性的;前者来源于中枢神经系统(CNS)内的细胞,而后者来源于癌细胞,癌细胞通过血液扩散从身体其他组织转移到大脑。中枢神经系统由两种主要细胞组成:神经元,作为神经系统的通讯器;神经胶质(或胶质细胞或神经胶质),为神经元提供支持和保护,维持体内平衡,并在其周围形成髓鞘。在中枢神经系统中,胶质细胞包括少突胶质细胞、星形胶质细胞、室管膜细胞和小胶质细胞。由胶质细胞或其前体细胞产生的肿瘤称为胶质瘤,组织学上与少突胶质细胞和星形胶质细胞相似的肿瘤称为“弥漫性胶质瘤”;这一术语包括星形细胞瘤和少突胶质瘤,分级为国际卫生组织(WHO)II级或III级,以及胶质母细胞瘤,分级为国际卫生组织IV级。
胶质瘤是成年人全部原发性恶性脑肿瘤中较常见的(75%);由于其局部侵袭性行为以及当前治疗无法治愈的事实,它们被认为是最具毁灭性的癌症之一。
2016年修订的国际卫生组织中枢神经系统肿瘤分类将胶质瘤根据综合经典组织学特征和分子生物标记物分为低级别胶质瘤(LGG;国际卫生组织I-II)和高级别胶质瘤(HGG;国际卫生组织III-IV)图1。
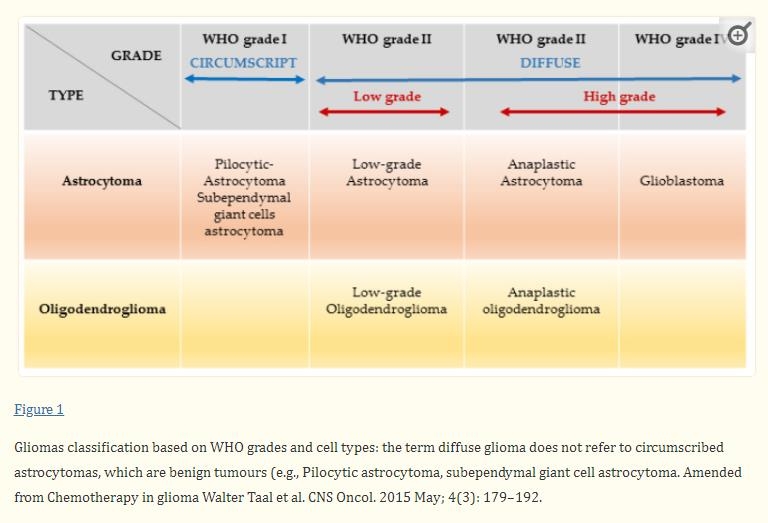
成人胶质瘤的流行病学和分类
在全部成人原发性脑肿瘤中,胶质母细胞瘤(诊断时的中位年龄为46.3岁)是较常见(56.6%)和最具侵袭性的肿瘤,目前尚无治疗方法。最近的证据表明,从1995年到2015年,英国胶质母细胞瘤的发病率增加,从每100000人中的2.4例增加到5.0例,增加了一倍多,而其余的胶质瘤保持稳定[5]。此外,预计在未来30年内,这种类型的肿瘤在美国将增加,而剩余的胶质瘤将保持稳定。
据推测,导致这一增长的因素包括人口老龄化、更广泛的神经成像和电离辐射暴露。尽管有最佳的手术和肿瘤治疗,与其他胶质瘤亚型相比,胶质母细胞瘤的生存率仍然较低(中位生存期为15个月)。美国胶质母细胞瘤的五年生存率为6.8%,而弥漫性星形细胞瘤为51.6%,间变性星形细胞瘤为30.2%,少突胶质细胞瘤为82.7%,间变性少突胶质细胞瘤为60.2%。
胶质母细胞瘤可能在没有恶性程度较低的前体病变(原发性胶质母细胞瘤或“新发性”胶质母细胞瘤)的情况下迅速发展,或通过从低级肿瘤(继发性胶质母细胞瘤)进展而发展。低级别胶质瘤(星形细胞瘤和少突胶质瘤II级)通常影响年轻人(II级星形细胞瘤的诊断年龄中位数为35岁,II级少突胶质瘤的诊断年龄中位数为34.8岁),星形细胞瘤患者的平均生存期约为7年,少突胶质瘤患者的平均生存期超过15年。
尽管与高级别胶质瘤患者相比,低级别胶质瘤患者的生存率更高,但全部低级别胶质瘤都是侵袭性的,最终发展为高级别胶质瘤(III/IV级),导致死亡。为了开发新的治疗策略,科学界已采取步骤,了解基因突变,揭开这些肿瘤起源细胞的神秘面纱,并确定免疫环境在肿瘤形成和进化的复杂相互作用中发挥的作用。
2007年,国际卫生组织(WHO)根据细胞类型和分级(I-IV级),使用组织病理学标准对脑肿瘤进行了分类,该标准涉及与假定起源细胞的相似性和假定分化水平[10]。基因组科学、分子病理学、免疫学和疾病建模方面的大量较新进展增加了对脑肿瘤神经生物学的认识,并定义了神经肿瘤学的新时代。因此,2016年,国际卫生组织分类进行了重建。
中枢神经系统恶性肿瘤现在不仅根据组织病理学结果,而且根据特定的分子遗传参数进行分类。
2007年,“弥漫性胶质瘤”的组织病理学分类包括四个等级:
(i)i级,指增殖潜力低的病变,通常在单独手术切除后即可治愈;
(ii)ii级,指弥漫性星形细胞瘤和少突胶质细胞瘤,浸润性病变,尽管增殖活性低,但经常复发并进展到更高级别;
(iii)iii级,指间变性星形细胞瘤和间变性少突胶质细胞瘤,它们是快速生长的肿瘤,通常是广泛的,扩散到附近组织;
(iv)iv级,表示胶质母细胞瘤,具有最具侵袭性的组织学和临床特征。相反,新的分类结合了组织病理学和基因型命名法,其中表型名称后接遗传分类(即弥漫性星形细胞瘤、IDH突变体)。
此外,国际卫生组织澄清,在基因型和表型之间不一致的情况下,前者优先。基因组特征优于组织病理学观察这一新概念,使我们能够慢慢走向基于客观基因型描述的新诊断和治疗方法。
在国际卫生组织2016年的分类中,“弥漫性胶质瘤”(II-IV级)根据一个标志性的遗传特征、异柠檬酸脱氢酶基因(IDH1和2)的突变状态、野生型(非突变型)与突变型(表1)分为两组。在近80%的低级别胶质瘤和继发性胶质母细胞瘤中发现了IDH突变,在约10%的原发性胶质母细胞瘤中发现了IDH突变。IDH突变被认为发生在胶质瘤发生的早期,较常见的杂合子突变是IDH1 Arg 132(R132H)。
突变的IDH酶将α-酮戊二酸(α-KG)还原为D-2-羟基戊二酸(D-2HG)。D-2HG被认为是一种肿瘤代谢物,可能通过竞争性inhi引起深刻的细胞修饰,包括组蛋白和DNA超甲基化,控制细胞分化和增加增殖,可能通过竞争性控制α-KG依赖性双加氧酶。

90%的胶质母细胞瘤(IV级)被称为原发性或新发性,大约30%的弥漫性和间变性星形细胞瘤(分别为II级和III级)包含野生型IDH基因。此外,在该组中也可以发现端粒酶逆转录酶(TERT)重要启动子内的突变,导致端粒酶活性增加,这是永生化过程中的一个重要步骤。肿瘤基因组图谱(TCGA)的数据发布后,胶质母细胞瘤显示出特定的肿瘤控制因子失活,例如TP53和视网膜母细胞瘤(RB)。
此外,这些数据还表明胶质母细胞瘤中存在促癌途径激活,例如受体酪氨酸激酶(RTK)、Ras和磷脂酰肌醇3-激酶(PI3K)途径的失调,通过激活生长因子受体(EGFR、PDGFRA)并通过神经纤维蛋白1(NF1)和磷酸酶和张力蛋白同源物(PTEN)缺失。IDH野生型“弥漫性”胶质瘤与较差的预后相关。
70%的弥漫性和间变性星形细胞瘤(II-III级)、全切的弥漫性和间变性少突胶质瘤以及10%的胶质母细胞瘤是IDH突变型。这些肿瘤还有两组诊断和预后亚组。一组是指弥漫性和间变性少突胶质瘤(II-III级),因为全切的患者染色体臂1p和19q[简称1p19q]共缺失,形成非平衡着丝粒易位t(1;19)(q10;p10)。这种协同作用与更好的结果和更好的烷化化疗反应有关。
虽然1p19q编码缺失在近二十年前被发现,但其在少突胶质瘤神经生物学中的功能影响知之甚少。到目前为止,已有证据表明,TERT启动子突变在突变体中普遍,导致TERT启动子转录活性增加,并随之产生端粒酶活性,最终决定了永生化的关键进展。此外,全外显子研究报告,capicua转录阻遏基因(CIC)在1p19q共缺失少突胶质瘤中经常发生特异性突变。
二组是指大多数II–III级胶质瘤,其转录调节因子ATRX和TP53发生突变,但没有1p19q编码缺失,包括弥漫性或间变性星形细胞瘤(II–III)和继发性胶质母细胞瘤(IV)。尽管有证据表明ATRX突变在细胞周期调节、组蛋白调节和染色质重塑中发挥作用,但迄今尚未确定ATRX突变对肿瘤神经生物学的具体作用。
2016年国际卫生组织分类的一项主要成就是(小计)遗漏了之前定义不清的少星形细胞瘤和间变性少星形细胞瘤诊断。通过使用基因型(即IDH突变和1p19q编码缺失状态)和表型作为诊断标准,该组的大多数(如果不是全部)肿瘤属于少突胶质瘤或星形细胞瘤。只有少数报告将肿瘤描述为“的”少突星形细胞瘤,由组织学和遗传学上离散的星形细胞(IDH突变体、ATRX突变体、1p/19q完整)和少突胶质细胞(IDH突变体、ATRX野生型和1p/19q共删除)混合肿瘤细胞群组成。
因此,根据CNS国际卫生组织2016分类标准,只有在诊断分子检测不可用时,或在根据组织学和分子遗传学特征进行诊断已确定肿瘤内混合有少突胶质瘤和星形细胞瘤细胞的少见真实病例中,才需要使用少突胶质细胞瘤诊断。
成人胶质瘤实验模型
人脑胶质瘤的体外和体内模型不有助于提高我们对胶质瘤生物学的理解,而且有助于开发新的治疗策略。目前的成人胶质瘤模型有优缺点。理想情况下,临床前神经胶质瘤模型应复制以下要求:与人类神经胶质瘤相似的遗传背景;类似于人脑胶质瘤的遗传、表观遗传和表型肿瘤内异质性;恶性基质细胞和非转化基质细胞(如免疫细胞、成纤维细胞、内皮细胞)之间的复杂相互作用创造了肿瘤微环境,应通过模型如实地表示出来;随着时间的推移,该模型应该是可复制和稳定的。
细胞系
一般来说,来源于人类肿瘤的细胞系是研究癌症个体特征的常用方法,例如持续增殖信号、激活侵袭和转移程序或抗凋亡。特别是,来源于具有不同恶性程度和各种遗传复杂性的人脑肿瘤的原代或永生细胞系是一种常见而有价值的工具,用于以可复制和受控的方式研究与胶质瘤形成、生长和进展有关的致癌细胞和分子机制。在小鼠模型中,这些细胞也可以随后作为异种移植物在皮下或原位繁殖。
此外,来源于人类肿瘤的细胞培养也可用于在快速和可重复的预筛选分析中同时跟踪多种药物的潜力,然后在适当的临床前模型中进行进一步测试。来自高级胶质母细胞瘤的常见细胞系,如U-87MG、LN-18和LN-229,为研究许多不同的药物方法提供了有用的工具,例如咖啡因如何使胶质母细胞瘤细胞对替莫唑胺(TMZ)的作用敏感,或肿瘤细胞如何克服接触控制。
然而,有文献表明,在有血清存在的情况下进行细胞的体外长期培养代表了一种选择压力。随着时间的推移,这可能会导致遗传畸变,从而导致癌细胞的基因表达和表型发生变化。这可能会影响对药物和其他刺激的反应,导致假阳性或阴性结果,例如,在研究的早期阶段可能会丢弃潜在有益的药物,相反,可能会将临床益处很少或没有临床益处的药物用于动物模型甚至临床试验。为了较大限度地减少脑肿瘤组织单层细胞系培养过程中发生的遗传改变,已经开发了新的培养方法,例如神经球培养。
为了形成神经球,新鲜切除的人脑胶质瘤细胞在含有碱性成纤维细胞生长因子(bFGF)、表皮生长因子(EGF)和神经细胞培养补充剂B-27的无血清培养基中生长。与单层培养相比,这些培养条件具有一些优势,例如从移植的胶质瘤中选择和扩增胶质瘤干细胞样细胞。事实上,与血清培养的细胞系相比,胶质瘤干细胞样细胞更紧密地保留了原发肿瘤的表型和基因型。然而,不可能从全部人类胶质瘤中培养出神经球,成功的培养取决于所分析肿瘤的组织学分级和遗传背景。
大脑类器官
在研究人脑胶质瘤生物学时,使用脑类器官正成为一种更具吸引力的方法。它们可以来源于人类多能干细胞,包括人类诱导多能干细胞(iPSC)和人类胚胎干细胞(ESC)。大脑类器官是一种体外生长的微型器官,包含多种类型的神经细胞,具有类似简化哺乳动物大脑的解剖学特征。
与其他体外和体内模型相比,脑类器官是一个更复杂的生理系统,用于研究脑癌。用于研究肿瘤发生的细胞系和患者来源的肿瘤异种移植物(PDTX)有其局限性:在体外培养和二维(2D)生长过程中获得的遗传变化可能使使用这些方法获得的结果不可靠;PDTXs模型价格昂贵,需要长期研究。脑类器官在3D培养系统中悬浮生长,这使它们能够更真实地代表体内细胞的行为,例如入侵,因为悬浮细胞可以向任何方向生长,不受培养皿的限制。
这使得大脑类器官对脑癌研究特别有价值。从人脑癌中分离出的胶质瘤干细胞也可以在3D细胞外基质中培养,以形成肿瘤球体。然而,嵌入Matrigel或等效物中的肿瘤球仅由癌症干细胞群组成,而大脑类器官遵循分化途径,使其表现出多种细胞类型和模式,类似于实际的大脑。这使类有机物比肿瘤来源的癌症干细胞具有更多优势。
最近,从人类ES细胞衍生的大脑类器官已被用于模拟胶质瘤发生的早期事件。通过使用CRISPR-Cas9技术进行同源重组,将HRAG12V IRES-TD番茄构建物靶向TP53位点,Ogawa等人能够同时损害TP53并获得HRas蛋白质的功能,从而形成肿瘤。与未经翻译的类有机物所代表的对照组相比,tdTomato reporter阳性的类有机物显示出标记物Ki67阳性的增殖细胞比例更高。
流式细胞术显示,在电穿孔后8周,5.7%的类器官培养物由致瘤细胞(TD番茄阳性)组成,在电穿孔后16周大大增加到86.8%。致瘤性脑类器官也显示出增殖和侵入其他健康类器官的能力。这项研究能够通过使用经过基因操作的健康类器官组织接近地模拟人类GBM的形成和侵袭。这项研究揭示了GBM侵袭周围组织时所采用的机制,并为未来对抗侵袭行为的药物研究铺平了道路。
其他研究采用了类似的方法来研究多个患者源性GBM样本的侵袭行为。Krieger等人描述了他们使用人类iPSC衍生的大脑类器官作为支架来研究GBM样本的生长和侵袭。将荧光标记的GBM样品与健康类有机物混合,并允许其生长3天。在此之后,全部测试的GBM样本都出现了广泛的入侵。事实上,这些样本是从单个肿瘤细胞中形成膜突起,这些细胞通过不同距离相互连接,从而形成GBM细胞连接网络。这种混合健康GBM类器官模型提供了对不同患者源性肿瘤之间异质性和侵袭行为差异的洞察,为个性化治疗提供了机会。
最近,Krieger等人研究了GBM培养物中的差异表达基因,结合/不结合来自iPSC的正常类器官培养物。通过使用单细胞RNA测序(scRNA-seq),他们确定了与健康类器官共培养的患者样本中差异表达的基因子集,与未进行共培养或单独进行健康类器官培养的患者样本相比。该基因集在全部共培养的GBM样本中上调,包括:编码连接蛋白-43的缝隙连接蛋白α1(GJA1),它允许GBM微管之间形成缝隙连接;编码细胞外基质成分的IV型胶原α5链(COL4A5)和之前与侵袭性相关的Wnt信号通路激活剂Glypican 3(GPC3)。
这些数据表明,患者来源的GBM与iPSC来源的大脑类器官的共同培养如何提供必要的细胞相互作用,以诱导转录组向侵袭方向的变化。这种混合类器官模型和scRNA-seq也描述了不同患者肿瘤之间的异质性,并提供了一种在临床相关时间尺度上测试单个肿瘤对靶向药物治疗敏感性的方法。
迄今为止,大脑类器官缺乏由血管和免疫细胞组成的现实微环境。然而,这些模型可能为研究胶质瘤生成机制、筛选候选药物和设计针对脑癌患者的个性化治疗提供了独特的机会。
器官型脑切片培养
体外培养的脑切片为研究胶质瘤细胞与脑微环境的相互作用,特别是研究肿瘤细胞浸润和迁移的机制提供了较好的机会。在这些模型中,将胶质瘤细胞体外原位微量注射到小鼠脑切片中,小鼠脑切片可以从年轻或成年啮齿动物中制备,并在培养物中保持数周。脑培养保留其三维结构,保留细胞结构、细胞功能和血管网络,允许胶质瘤细胞与其他脑细胞类型直接相互作用,包括神经元、星形胶质细胞、少突胶质细胞和大脑特异性细胞外基质。
最近,Marques Torrejon等人将表达GFP的患者源性胶质瘤干细胞或表达GFP的小鼠胶质母细胞瘤起始细胞植入成年小鼠冠状脑片培养物。这两种细胞都被植入培养物中,可以维持长达三周。植入的细胞对脑组织中不同的微环境表现出不同的反应,注射在神经干细胞生态位内的细胞甚至对内皮生态位信号作出反应。然而,3周后,培养物开始失去其结构,这表明器官型脑片培养物在超过这一时期的临床前药物研究中可能存在一些局限性。在另一项研究中,Eisemann等人通过植入小鼠或人类细胞系产生的肿瘤球体,使用器官型培养来研究胶质瘤的侵袭性。
他们发现,供体小鼠大脑的基因改变,如细胞表面蛋白的敲除,导致肿瘤细胞侵袭减少。这种体外实验表明,转基因小鼠可以与器官型培养相结合,以显示哪些细胞表面标记可以被胶质瘤细胞利用来驱动其侵袭。其他研究已经证明脑切片培养适合研究胶质瘤细胞对抗癌药物的反应。最近,Minami和合著者使用脑切片培养来测试顺铂、TMZ和紫杉醇对恶性胶质瘤模型的个体药理作用。
该模型是通过向成年小鼠注射Inka/Arf建立的−/− 用癌基因HRAV12转导的神经干细胞。进行的药物筛选显示,顺铂能够减小肿瘤大小,TMZ控制肿瘤细胞增殖,而紫杉醇则显示会引起肿瘤细胞的有丝分裂滑移。脑外植体培养可以研究胶质瘤组织微环境中的药理反应。然而,这也意味着在这些模型上进行的药物筛选不能解释由于血脑屏障(BBB)的影响而导致的大脑内药物浓度的变化。
事实上,血脑屏障限制了药物向脑肿瘤的传递,因此很难理解药物疗效的缺乏是由于缺乏药理作用还是由于传递受阻。增加血脑屏障的通透性可能是提高药物对大脑疗效的另一种途径。然而,脑切片培养系统通过使化合物能够直接从培养液中进入脑组织,在评估不穿过血脑屏障的药物(如紫杉醇)的作用方面具有优势。
人脑胶质瘤的体内模型
小鼠模型允许在生理环境中研究肿瘤发生,在生理环境中肿瘤遇到一致的血流和营养、多种细胞类型,通常还有完整的免疫系统。与在不太复杂的环境中生长的孤立细胞系相比,全部这些因素的结合提供了一个更加动态和生理准确的系统。
获得胶质瘤小鼠模型的方法有多种,包括(1)涉及改变已知影响胶质瘤形成和进展的特定基因的基因工程小鼠模型(GEMM)和(2)利用患者来源细胞/肿瘤片段的异种移植模型。异种移植模型是使用体外培养的胶质瘤细胞系或患者肿瘤样本生成的,随后直接插入小鼠大脑以诱导肿瘤形成,或通过将人类胶质瘤的小片段直接注射到大脑中,从而绕过培养样本的需要,这可能导致由于肿瘤细胞对培养条件的适应而导致基因改变的丢失/获得。
胶质瘤基因工程小鼠模型
在基因工程小鼠模型(GEMM)中,在小鼠模型的生殖系(敲除、敲入、转基因模型)或体细胞(通过病毒介导的基因传递)中引入在人类肿瘤中识别的特定基因改变,以产生新发肿瘤。在这些模型中,感兴趣的基因改变针对小鼠组织/器官内的特定细胞群,以及动物的特定发育阶段(胚胎、出生后或成年器官)。
GEMM是一种重要的实验工具,用于研究与肿瘤发生和发展相关的细胞和分子事件,并确定恶性转化所需的较小基因改变。GEMM代表的另一个重要优势是,它们已在免疫活性动物中建立,突出了微环境在肿瘤生物学中的重要性。GEMMs已用于检测生物标记物表达、药物释放方法和新的治疗策略,许多使用GEMMs的研究已成功转化为临床试验。
Reilly等人通过杂交两种小鼠株Nf1建立了星形细胞瘤模型+/− 和Trp53+/− 产生双杂合子小鼠。该模型产生的大多是低度弥漫性星形细胞瘤(国际卫生组织II级),在某些情况下进展为IV级胶质母细胞瘤。还有许多其他高级别星形细胞瘤模型的开发依赖于Ras、EGFR和Akt等基因的改变。一些模型,例如Marumoto和合著者建立的模型,使用慢病毒载体作为将所需基因改变传递到小鼠大脑的手段。
将慢病毒立体定向注射到皮层、脑室下区和海马,导致高级别星形细胞瘤(GBM)。不同级别的少突胶质细胞瘤的GEMM也被开发出来。丁和合著者通过将表达过度激活型EGFR(EGFRvIII)的小鼠与携带Ha-RasV12突变体的小鼠杂交,建立了少突胶质细胞瘤模型,这两种突变体均由GFAP启动子驱动。这些双突变小鼠产生的脑肿瘤与少突胶质细胞瘤的组织学相似,Nestin和GFAP均呈免疫阴性。一些EGFRvIII/Ha-RasV12双突变小鼠也表现出星形细胞瘤的组织学特征。
虽然GEMM是了解突变获取如何导致肿瘤形成的有用工具,但它们也存在一些局限性:产生的遗传改变仅限于一些基因,因此它们不能完全代表切除的人脑胶质瘤样本中常见的遗传复杂性和异质性。此外,它们的开发通常成本高、耗时长。
异种移植模型
在患者衍生的异种移植(PDX)模型中,以肿瘤细胞模型或整块活检的形式将人脑胶质瘤注射或移植到免疫缺陷小鼠中,以防止移植受到宿主的排斥。免疫系统控制程度不同的几株小鼠可用于这些研究:无胸腺裸鼠,其中T细胞数量大大减少;严重受损的免疫缺陷(SCID)小鼠,其中B细胞和T细胞均缺乏;NOD-SCID小鼠,其中B、T淋巴细胞和自然杀伤(NK)细胞发育受损;重组激活基因2(Rag2)-敲除小鼠,其中B细胞和T细胞的成熟均受损。
在这些小鼠中,可以将肿瘤样本异位植入与原始肿瘤部位无关的小鼠区域(通常为皮下)或原位植入肿瘤起源部位(即脑肿瘤的脑内)。异种移植模型中产生的肿瘤生长相对较快,并保留患者肿瘤的细胞和分子特征。保留肿瘤内的遗传异质性可以准确地表示来源样本。此外,PDX具有开发体内血管供应的优势。由于这些原因,它们代表了一种有用的临床模型,用于测试肿瘤细胞对治疗的反应,尽管在小鼠体内传代的数量有限。在此之后,开始对繁殖施加选择性压力,导致细胞中特定的遗传和表观遗传特征发生变化,使生成的肿瘤较难代表患者的原始肿瘤。
在异位异种移植模型中,将胶质瘤细胞注射到组织中,在该组织中,它们不会经历与起源组织微环境中相同的刺激和细胞间相互作用。脑肿瘤样本也将缺乏来自大脑特异性免疫因子的输入,例如小胶质细胞和巨噬细胞,它们既可以影响肿瘤细胞,也可以受肿瘤细胞的影响。为了减少这种限制,异种移植物中可以包括来自人类肿瘤微环境的基质。或者,原位异种移植代表了更好的实验选择。
在脑癌原位异种移植模型中,将肿瘤样本立体定向注射到小鼠大脑中,以便至少可以部分测量癌细胞对其微环境的影响。颅内模型还允许测试新药渗透血脑屏障的能力,并且仍然能够在脑组织内维持所需的药物剂量。在这些模型中,需要监测肿瘤生长和对药物治疗成像技术的反应,因此有时在颅内注射之前用荧光素酶标记胶质瘤样本。
最近,通过玻璃体腔注射将细胞植入小鼠眼睛中,产生了一种使用患者来源的胶质母细胞瘤细胞的不同异种移植模型。该模型允许在大约2周后产生肿瘤,持续发展到4周后形成最终肿块。这种PDX模型允许药物筛选在初次手术后仅6周开始,并允许潜在有益的额外治疗快速恢复。生成这些患者特异性PDX模型所需的6周窗口比患者初次手术和肿瘤复发之间的平均时间短,因此这有可能延迟甚至防止疾病复发。
“人源化”小鼠异种移植
使用人类肿瘤样本的异种移植模型可以很好地洞察人类胶质瘤生物学,但是这些模型依赖于免疫缺陷小鼠宿主。鉴于最近对免疫系统在癌症进展中的作用的关注,这些异种移植模型存在一些局限性,因为它们不能完全重现免疫和癌细胞相互作用的“真实”微环境。
在“人源化”NOD/SCID小鼠模型中,通过植入通常来源于人类胎儿组织、脐血或外周血单个核细胞(PBMC)的人类初级造血干细胞(HSC),生成功能性人类免疫系统。为了促进植入,HSC和PBMC的人类白细胞抗原(HLA)应与异种移植的组织相匹配[79]。然后将人脑胶质瘤移植到“人源化”NOD/SCID小鼠模型中。然而,目前,没有单一的“人源化”小鼠模型能够提供人类免疫系统的全谱,因为这些模型往往表现出较差的B细胞成熟度,并且缺乏形成T细胞库的HLA I类和II类选择元素。
不幸的是,这些小鼠也可以针对异种移植组织发展移植物抗宿主病(GVHD)。移植物抗宿主病是对异种移植组织的严重免疫反应,通常是因为异种移植组织与受体组织不匹配[82]。GVHD的发病率在使用PMBC移植模型开发的小鼠中明显。这可以通过使用同一患者的骨髓来提供要移植的组织来克服,尽管这很难大规模实施。
最近,将胶质瘤样本移植到免疫系统完整的小鼠体内的研究开始出现。Semenkow等人提供了免疫活性小鼠模型的证据,与在免疫缺陷宿主中生长的移植相比,该模型能够更真实地模拟GBMs患者的临床病理生理学。为了促进神经胶质瘤样本植入免疫活性小鼠,通过使用MR1(一种存在于T细胞表面的针对小鼠CD154的抗体)和abatacept(一种针对CD80/CD86的抗体)获得对T细胞激活的短暂药理学阻断,该抗体可阻止抗原呈递细胞传递一个T细胞刺激信号。
MR1和abatacept的四种治疗足以使新称为“免疫耐受小鼠”的异种移植物生长,与标准免疫缺陷小鼠的异种移植物生长相当。与免疫缺陷小鼠相比,这些免疫耐受小鼠的磁共振成像显示肿瘤对比度增强。这表明高级别胶质瘤中通常存在较高的血脑屏障通透性。免疫耐受小鼠还表现出小胶质细胞激活增加,T细胞和白细胞浸润,表明存在先天性和适应性免疫系统。
综上所述,这些结果是对具有功能性免疫系统的新型小鼠模型的一个有希望的见解。这可能为涉及免疫治疗和癌症疫苗的更具临床相关性的未来药物研究铺平道路,并允许对癌症进化与宿主免疫系统之间的复杂相互作用有更深入的了解。
成人胶质瘤的瘤内异质性和肿瘤演变
使用新型组织采样的肿瘤内异质性
肿瘤内异质性描述了同一肿瘤内不同细胞获得不同表观遗传和基因组改变的现象。这允许发展不同的形态和表型特征,并由此产生与祖癌细胞群不同的发展。肿瘤内异质性被认为是传统和靶向治疗维持缓解的主要障碍之一。弥漫性胶质瘤,是胶质母细胞瘤,已知表现出肿瘤内异质性(当该现象发生在同一肿瘤内时),以及肿瘤间异质性(当其发生在不同肿瘤之间时)。
在此之前,通过荧光原位杂交(FISH)在EGFR、PDGFRA和MET水平上证明了肿瘤内的异质性。Sottoriva A.等人一次表明,荧光引导下在同一患者体内进行客观多组织采样对于询问同一癌症样本(本例为胶质母细胞瘤)内的异质性至关重要[91]。这是基于这样一个事实,即单个活检不太可能出现全套突变,导致报告的基因表达存在偏差。肿瘤发展过程中基因表达的变化表明,单一疗法不太可能对每个亚克隆合适,这意味着虽然它可能对一个克隆合适,但其余肿瘤将能够通过具有固有耐药性[93]或治疗后获得耐药性而存活。
瘤种、亚型和治疗类型的肿瘤微环境变化
众所周知,临床试验未能显示“弥漫性胶质瘤”的生存益处。癌细胞与动态肿瘤微环境(TME)之间的复杂相互作用是肿瘤基因表达和转录组适应性的标志性“启动子”,影响其异质性和进化。了解基因改变和表达的关键驱动因素,以及基因表达与细胞表型的关系,将使我们能够制定合理的治疗干预措施,以改变肿瘤内进化的命运,从而改变耐药模式。
胶质瘤侵袭和进展的建模参数
脑外的胶质母细胞瘤转移很少见[124],而该肿瘤沿着血管和白质束弥漫性浸润大脑区域。事实上,GBM通常在原发肿瘤切除边界的1-2厘米范围内复发,通常治疗失败和肿瘤复发的主要原因是GBM细胞扩散侵入周围脑组织。胶质瘤细胞向邻近组织的迁移和侵袭是一个有趣的领域,虽然这两种机制相互补充,但它们是独自的过程,其中迁移是胶质瘤细胞从主要肿瘤块上分离和移动,而侵袭是指胶质瘤细胞在不脱离肿瘤肿块的情况下扩展到邻近的健康组织。由于胶质瘤具有高度侵袭性,因此能够在硅片中模拟和评估这种行为变得越来越重要。
血脑屏障通透性的建模参数
血脑屏障(BBB)的通透性是设计和测试新型脑癌疗法的较大障碍之一。血脑屏障由内皮细胞组成,内皮细胞通过紧密连接连接在一起,这使得大脑的毛细血管具有如此低的渗透性。这种通透性的缺乏对于维持间质液的组成和排除血液中的废物进入大脑重要。虽然这种低渗透性在生理条件下发挥作用,但在设计能够进入大脑并在所需浓度下积聚的合适化疗药物时,它是一个独特的障碍。BBB的电子模型允许研究人员在体外或体内验证之前筛选药物化合物。
发现进化模式并理解耐药性的出现
克隆进化是推动肿瘤进展的主要过程之一。肿瘤内异质克隆的出现是由肿瘤细胞在癌症进展过程中所经历的遗传、表观遗传和微环境选择压力引起的。克隆进化也是抗肿瘤药物治疗耐药的主要原因之一。了解单个患者癌症的进化过程可能对决定其最佳治疗计划和诊断以及随后的进展或复发点至关重要。
新药分子的虚拟筛选和虚拟临床试验
少突胶质瘤的特征是IDH1或IDH2突变并伴有1p/19q染色体臂的丢失。与其他弥漫性胶质瘤相比,它是一种生长相对缓慢的肿瘤,主要影响年轻患者,中位生存时间更长,对烷化剂的反应更好。尽管有可用的手术和治疗选择,它仍然是一种无法治愈的恶性肿瘤。对少突胶质细胞瘤的生长和治疗反应进行建模可能是一个有用的工具,可以确定新的适应性治疗方案在临床上是否有助于通过减少毒性和副作用来提高生存率和患者的生活质量。
最近提出了一种使用真实患者数据对胶质瘤生长和对TMZ反应的参数进行建模的模型。来自这些患者的数据用于生成一个“电子双胞胎”,在此基础上可以测试不同治疗方案的模拟。治疗周期之间的间隔时间增加了15天至6个月。这些数据表明,虽然不同治疗方案之间的肿瘤生长情况相似,但也有一些“硅双生”患者的替代方案提高了生存率。
模拟了2000名患者的临床试验,其中一半患者接受了真实患者所经历的随机数目的治疗周期(在5到18个周期之间),另一半患者接受了新提出的治疗方案。这项虚拟临床试验表明,新的治疗方案将中位生存期延长了3.8年,并为对真实患者进行临床试验以好转II级少突胶质瘤的治疗和管理铺平了道路。
神经胶质瘤内发现的表观遗传学改变,从识别新的生物标记物到评估临床结果和治疗方案
DNA甲基化是甲基共价转移到其中一个DNA核苷酸碱基上,通过DNA甲基转移酶进行靶向修饰或作为DNA损伤剂的作用。胞嘧啶(5-甲基胞嘧啶,5mC)碳-5位置的甲基化是一种有充分证据的表观遗传DNA改变,控制广泛基因的表达,并在染色质结构中发挥作用。TET家族双加氧酶氧化5mC产生5-羟甲基胞嘧啶(5hmC);这是DNA去甲基化的一步。
脱甲基过程继续形成衍生物,5-甲酰胞嘧啶(5fC),然后是5-羧基胞嘧啶(5caC)。5caC被碱基切除修复系统靶向,并被未修饰的胞嘧啶碱基取代,从而返回非甲基化的胞嘧啶碱基。5fC和5caC似乎具有优先于5mC或5hmC与其结合的蛋白质,这表明这些5mC衍生物可能具有自己的表观遗传信号级联和功能。在小鼠胚胎干细胞中测试时,一些转录和染色质调节因子与5fC结合,而DNA甲基转移酶DNMT1优先与神经祖细胞中的5caC结合。这表明,虽然5mC衍生物5fC和5caC在DNA去甲基化中发挥作用,但它们也可能具有表观遗传信号功能。
胶质瘤表现出与肿瘤发生、进展和治疗抵抗有关的几种致癌途径,与其他肿瘤一样,它们的发生和进展与表观遗传异常有关。因此,针对神经胶质瘤的表观基因组被认为是一种令人信服的治疗方式。
IDHWT和IDHmut胶质瘤的甲基化模式不同
IDH突变较常见于R132位,胶质瘤中较常见的突变导致R132H的改变。这种突变的结果是新形成的酶活性,它不是产生α-酮戊二酸,而是产生2-羟基戊二酸(2-HG)。2-HG作为双加氧酶(包括组蛋白脱甲基酶)的竞争性控制剂,导致基因组甲基化谱的变化。
对IDH突变体脑瘤进行的多项研究侧重于了解IDH相关胶质瘤发生的途径和机制,特别是表观遗传修饰的作用和对IDH突变体胶质瘤的影响。Park和Turcan[155]的综述讨论了IDH突变状态的改变,导致组蛋白修饰和染色质重塑。在这里,我们讨论了G-CIMP状态下原发性和复发性胶质瘤之间的甲基化转移,这是一种与IDH突变相关的现象。
复发性胶质瘤中的甲基化改变代表了向更具侵袭性表型的转变
胶质瘤中的IDH突变产生一种独特的甲基化模式,称为胶质瘤CpG岛甲基化表型(G-CIMP)。LGG可分为G-CIMP低或G-CIMP高,分别表示肿瘤的侵袭性更强和较弱。De Souza等人提供了原发肿瘤和复发肿瘤之间甲基化模式变化的证据。在表现和肿瘤复发方面,G-CIMP高的患者比原发肿瘤复发且甲基化改变为G-CIMP低的患者有更好的临床结果。
事实上,表现为G-CIMP高原发肿瘤但在复发时进展为G-CIMP低肿瘤的患者,在其复发肿瘤中显示出更高水平的“干性”,表明其恶性程度更高。G-CIMP低复发肿瘤的干细胞指数与高侵袭性IDHWT原发性GBMs的干细胞指数较为相似。De Souza等人提出,IDHmut原发性胶质瘤中的一小部分细胞可能已经具有G-CIMP低表型,因此作为更具侵袭性和抗治疗表型,有助于肿瘤的复发。
胶质母细胞瘤中一种新DNA修饰的鉴定
虽然胞嘧啶碱基的甲基化较常见于表观遗传学,但存在另一种形式的DNA修饰,即仲胺(N6-mA)腺嘌呤碱基的甲基化。N6-mA修饰已在细菌和哺乳动物中得到证实,但最近才在人类基因组中一次发现。通过使用斑点杂交试验和N6-mA特异性抗体,证明了原发性人类胶质母细胞瘤以及经验证的患者源性胶质母细胞瘤肿瘤干细胞模型中存在修饰。
人胶质母细胞瘤样本中N6-mA的水平高于正常健康组织,表明其可能具有致瘤作用。ALKBH1是一种去甲基化酶,被鉴定为N6-mA修饰的调节剂,当这种酶被控制时,肿瘤形成减少,胶质瘤干细胞的自我更新能力也降低。敲除ALKBH1导致参与缺氧反应的基因下调,表明以ALKBH1为靶点可能具有临床益处。与N6-mA修饰本身一样,与健康脑组织相比,ALKBH1在人胶质母细胞瘤中高表达,表明这种酶的治疗靶向性可以更特异地靶向胶质瘤细胞而不是健康细胞。
高ALKBH1水平的存在与较高的胶质瘤分级以及较差的生存率相关。这些数据表明,这种新型DNA修饰有可能成为治疗胶质母细胞瘤的临床靶点。
液体活检可以完全改变胶质瘤的检测和诊断
胶质瘤进展的诊断和监测涉及通过使用样本活检和/或使用神经成像技术(如磁共振成像(MRI)或计算机断层扫描)对患者肿瘤进行分子分析。然而,全部这些技术都有其局限性;总的来说,诊断过程需要时间、昂贵的设备和压力,如果是组织活检,也可能给患者带来脑肿胀和出血的风险。胶质瘤液体活检是一种微创技术,在胶质瘤治疗的各个方面都有很大的潜力。
从检测到监测肿瘤对治疗的反应和早期复发。可以确定潜在的生物标记物来衡量疾病进展。重要的是,随着时间的推移,可以定期获得液体活检,并可以提供有关分子异质性的较新信息,以及肿瘤从诊断到进展/复发的纵向基因组进化。
当前治疗和未来治疗
弥漫性胶质瘤的手术治疗
由于脑肿瘤成像、术中技术和神经外科技术的进步,胶质瘤手术在过去十年中发生了革命性的变化。顺利、较大限度地切除胶质瘤可以好转症状管理、生活质量以及无进展生存率和总生存率的治疗理念也不再那么虚无缥缈。目前,LGG和HGG的切除范围(EOR)与临床结果之间的关系尚不完全清楚。没有合适的指标来量化EOR,随机临床试验也不切实际,这阻碍了EOR一级证据的实现。
然而,越来越多的临床数据支持LGG和HGG全切除的预后重要性,并被纳入欧洲指南。在胶质瘤手术中追求较大EOR需要谨慎,并且需与功能结果相平衡。如果不能识别和保存有说服力的大脑区域,可能会严重影响患者的生活质量和表现状态,并可能使其不符合进一步的辅助治疗选择,从而产生严重的预后影响。
弥漫性胶质瘤的放化疗
手术后,弥漫性星形细胞瘤和少突胶质细胞瘤患者分为低风险和。值得注意的是,和低风险低级别胶质瘤的定义差异很大。被认为是低风险低级别胶质瘤的患者是那些接受了完全切除、年龄小于40岁、神经功能良好并被归类为IDH突变体的患者。根据欧洲癌症研究与治疗组织(EORTC)22845的分析,采用了定期MRI扫描的观察等待政策。
值得注意的是,除了回顾性比较(显示即时放射治疗与延迟放射治疗的生存率相等)外,没有任何前瞻性数据建议治疗。根据EORTC 22033-26033和RTOG 98023阶段试验,高危低级别胶质瘤患者是指年龄大于40岁、肿瘤较大(>5cm)、术后功能降低或未完全切除的患者。现在人们普遍认为IDH野生型低级别胶质瘤通常被视为,因为它们的行为往往与高级别IV级胶质母细胞瘤相似。在高危组中,目前的术后护理来自RTOG 9802试验,其中包括50-54格雷之间的放射治疗,然后是辅助性原卡巴嗪、洛莫司汀和长春新碱(PCV),共六个周期的治疗。
免疫治疗和靶向治疗
在过去,大脑被认为是一个免疫特权器官,这意味着免疫系统的影响或至少是全部影响预计不会发生。这是基于这样一个事实,即不存在淋巴管,血脑屏障(BBB)阻止免疫调节器和细胞的流入。尽管人们越来越认识到这可能并不完全正确。重要的是,人们认识到,脑肿瘤通过较小化主要组织相容性复合体(MHC)蛋白的表达、减少细胞活化(是T细胞)和表达促凋亡因子,逃避和控制免疫系统。
了解免疫逃避机制一直是一个新兴和令人振奋的新研究领域。克服免疫控制的三种主要方法一直处于研究前沿:
(i)细胞因子治疗,
(ii)主动免疫治疗
(iii)被动免疫治疗。
细胞因子治疗主要集中在激活免疫系统,希望它能对抗肿瘤。主动免疫治疗主要集中于通过疫苗接种和过继性T细胞治疗来启动针对已知肿瘤抗原的免疫反应。被动免疫疗法是指使用能够与肿瘤表达抗原结合的共轭抗体,这些抗原与能够控制通路或杀死细胞的物质相连。目前,有一些正在进行的三期疫苗试验(肿瘤裂解物-NCT0045968和树突状细胞疫苗-NCT02546102)。
最近,对原发性脑肿瘤患者进行免疫检查点控制剂治疗的临床试验并没有显示总生存率的好转。在3阶段研究CheckMate 143(NCT02017717)中,将Nivolumab(一种与程序性死亡-1(PD-1)受体结合的人类单克隆抗体)的合适性和顺利性与贝伐单抗(一种抗血管内皮生长因子(VEGF)的抗体)进行了比较。获得的数据表明,与贝伐单抗相比,nivolumab治疗患者的总体生存率没有好转;
然而,在具有甲基化MGMT启动子且未使用基线皮质类固醇的胶质母细胞瘤患者中,检测到使用nivolumab(nivolumab 17.0个月与贝伐单抗10.1个月)可提高生存率。这表明免疫检查点控制剂治疗该亚组患者具有潜在的临床益处[201]。英国正在对新诊断的GBM患者进行进一步的免疫治疗研究:Checkmate 548(NCT02667587)是一项研究TMZ和用nivolumab或安慰剂进行放射治疗的联合作用,而Checkmate 498(NCT02617589)比较了nivolumab和TMZ的合适性,每种药物都用放射治疗。
未来的试验和治疗
提供精确/分层医学的能力对神经胶质瘤患者来说是一个挑战。未来的治疗将受益于手术切除的“新鲜肿瘤组织”,这超出了诊断要求。组织需适合全基因组分析、表观基因组学、转录组学、甲基组学和蛋白质组学,以识别特定的肿瘤靶点、药物敏感性和免疫调节因子。英国的分子分层和靶向治疗可行性研究通过提高临床疗效、减少可避免的毒性来优化胶质瘤患者的临床管理,好转术后残留和复发疾病的管理并提高生存率是一项旨在优化该策略的国家平台研究。
BRAIN MATRIX的目的是检验以下假设:在英国,及时对胶质瘤进行多方位的全基因组测序和表观基因组分析是可行的,并且结果好转了患者对下一代(靶向)治疗的分层,以最终好转临床结果和生活质量。此外,优化的新鲜肿瘤采样管道可用于提供优质组织,以创建自体疫苗和潜在的免疫疗法。前沿的试验技术,如适应性设计,可以通过使用试验中积累的结果,根据预先指定的规则修改试验过程,使临床试验更加灵活。这些技术可以缩短试验时间,获得更精确的结论,但更为复杂,并在其他癌症(是肺癌)中取得了成功。
结论
神经胶质瘤治疗的未来发展需要患者、临床医生、科学家和临床试验单位之间更为综合的方法和密切的合作,以便将专注于精确医学和适应性临床试验的转化研究结合起来。使用单细胞RNA-seq方法和更广泛的体外和体内模型将使神经胶质瘤的分子事件得以进一步阐明。肿瘤微环境以及正常脑细胞的作用需要进一步关注,以了解这些脑特异性成分如何影响胶质瘤的发展、进展和复发,从而开发出更多方位的治疗方法。
借助于此,电子药物设计和测试使我们能够快速了解某种药物是否会通过血脑屏障,这是系统给药药物开发的主要障碍,以及一种新药是否会提供任何治疗益处。近年来,我们对神经胶质瘤发病和进展过程中的分子事件的理解有了很大的提高,遗憾的是,患者分层护理的临床方面没有与之匹配。临床医生、科学家和临床试验之间更大的合作将在未来带来更多的治疗选择,以对抗这种致命的疾病。




