前庭神经鞘瘤占颅内肿瘤的8%,是成人桥小脑角较常见的肿瘤。这些肿瘤起源于前庭耳蜗(八颅神经)神经前庭分支的髓鞘雪旺细胞。“前庭神经鞘瘤”一词比“听神经瘤”更准确。虽然前庭神经鞘瘤通常被认为是少见的,但最近的流行病学趋势显示,在500人中,其终生患病率超过1例。这些肿瘤不可评估的临床特点和有限的高水平研究证据,加上越来越被重视的生活质量因素,使目前的治疗备受争议。
一些研究及技术进步改变了该病的诊断和治疗模式。敏感的神经诊断影像学的广泛应用,使前庭神经鞘瘤的检出率提高;当肿瘤很小或病人年事已高时,越来越多的病例被诊断出来,通常是偶然性发现的;同时也出现了保守治疗策略的转变,即优先保护神经功能而非治愈。这篇综述重点在占95%以上患者的散发的单侧前庭神经鞘瘤。在较少的情况下,前庭神经鞘瘤发生于如神经纤维瘤病2型和神经鞘瘤病等肿瘤易感的遗传疾病的背景。
前庭神经鞘瘤发病率的明显增加和受影响患者的人口统计学特征的改变,主要是由于检查普及从而提高疾病检测率,而不是的生物学改变。从20世纪初到20世纪70年代,前庭神经鞘瘤的发病率保持不变,因为患者表现为大肿瘤,肿瘤生长了一段时间而未被发现。从1970年左右的历史发病率为每年每10万人1例,目前的发病率为每年每10万人3至5例,甚至在最近10年也持续增加。这一增长在70岁以上人群中较为,他们报告的发病率现在已接近每10万人年20例。如今,通常情况下,患者在60岁或70岁时被诊断出肿瘤,其较大直径仅为毫米。
疾病发病率的变化与对比增强MR(MRI)越来越广泛的使用,以及对不对称听力损失的更严格的筛查方案的采用相对应。丹麦国家注册中心的前瞻性数据分析显示,患者的平均诊断年龄从49岁增加到60岁,平均肿瘤大小从2.8厘米减少到0.7厘米,诊断时听力损失的严重程度降低。此外,在广泛使用MRI的地区,基于人群的数据表明,多达25%的新病例是在成像时偶然诊断的,而这些成像是由于不相关的适应症(如头痛)而获得的。然而,仅靠改进的检测手段并不能完全解释近年来发病率的增加。一些研究小组认为,环境暴露,如使用手机或长期接触噪音可能会增加肿瘤发生的风险;然而,大型病例对照研究未能证实这些关联。因此,除电离辐射暴露外,对暴露是否增加前庭神经鞘瘤的风险尚无共识。
增加疾病检测的一个重要后果是可能出现过度治疗,这可能导致不必要的并发症和卫生保健支出。几十年前,许多患者的肿瘤不会被检测出来,但现在他们正在接受治疗。虽然最初采用随访观察策略治疗的病例比例比以往任何时候都高,但自相矛盾的是,每一人群中接受放疗和显微手术治疗的前庭神经鞘瘤的总数可能比过去几十年都要多(图1)。然而,越来越多的患者现在通过连续影像检查进行主动随访观察,这标志着临床护理从早期的显微外科切除向慢性病的治疗转变。

图1。受前庭神经鞘瘤占位影响的显微神经解剖和结构情况。
图A(上部)显示了后颅窝的相关显微解剖结构。图A(下部)和图B显示肿瘤生长对邻近颅神经(CN)、脑干和小脑的占位效应。前庭神经鞘瘤的特征性表现为发生于内耳道(IAC),起源于前庭蜗神经的两个前庭分支之一。前庭蜗神经的腹侧是面神经,它传递主要负责面部运动的传出运动纤维。AICA:小脑前下动脉,EAC外耳道,PICA:小脑后下动脉。
疾病表现
较常见的症状包括超过90%的患者伴有同侧感音神经性听力丧失,多达61%的患者伴有头晕或不平衡。55%有不对称耳鸣。听力丧失最初通常很轻微,当病人使用电话或躺在床上捂住对侧耳朵时,听力丧失可能首先变得明显。随着时间的推移,许多人在背景噪音的存在下有越来越多的声音定位和言语理解的困难,这是由于双耳听力的丧失。耳鸣的特点和严重程度各不相同。耳鸣被认为是由耳蜗传导阻滞和皮层适应不良引起的——这一机制类似于传入神经阻滞性疼痛,见于幻肢综合征。因此,即使是严重的听力损失或显微手术导致的耳蜗神经损伤,耳鸣也可能持续。虽然前庭神经鞘瘤是由前庭神经引起的,在平衡测试中,前庭功能的客观丧失是常见的,但眩晕和持续头晕的症状分别只占8%和3%。这种差异可能反映了与肿瘤生长缓慢相关的前庭功能减退进展缓慢,这为大脑中枢代偿提供了机会。
大听神经瘤肿瘤压迫脑干和小脑的患者可出现三叉神经分布感觉减退、继发性三叉神经痛、小脑失调和共济失调,或在没有意识改变的情况下出现缓慢进行性脑积水。即使是较大的肿瘤通常也不会引起临床上明显的面神经、三叉神经运动支或后组颅神经功能障碍,尽管这些障碍也可能偶尔发生。如果有这样的发现,应考虑其他诊断,如源自其他神经的神经鞘瘤(如面神经神经鞘瘤)、脑膜瘤、其他部位原发肿瘤的转移,或是自发的,或是放疗后的新发生的或继发于已有的神经鞘瘤的恶性外周神经鞘肿瘤。此外,听神经瘤不同的肿瘤生长类型,包括大的囊性的和出血性前庭神经鞘瘤,可能有更具进袭性的病程(图2)。
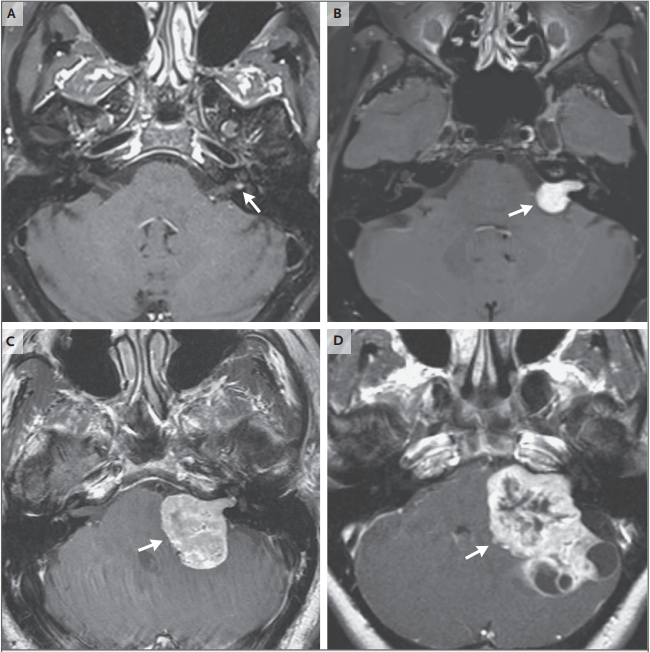
图2。诊断时前庭神经鞘瘤大小的变异。
前庭神经鞘瘤在注射增强对比剂前的T1加权 MRI序列显示为等信号,钆剂注射后呈强烈增强。根据大小不同,肿瘤可能完全局限于内耳道,也可能不同程度地延伸到桥小脑角。图A到图D分别显示轴向增强T1加权 MRI上左侧小、中、大和较大(箭头)的前庭神经鞘瘤。随着肿瘤的生长,它会在内耳道范围内扩张,并对邻近神经施加压力,然后向中间方向生长到桥小脑角。较大的肿瘤延伸至桥小脑角可压迫位于头侧的三叉神经、尾侧的后组颅神经、脑干和小脑内侧。进展性脑桥中间抹平可能导致四脑室梗阻和随后的脑积水。
肿瘤大小与诊断时听力损失、耳鸣或头晕的严重程度之间存在有限的相关性,而症状进展与肿瘤生长没有很强的相关性。
这些研究结果为保守治疗提供了重要的指导:听前庭症状恶化不是肿瘤生长的可靠指标,无论有无症状,应定期进行连续影像学检查。此外,与后颅窝占位效应相关的症状相比,肿瘤切除通常会好转(如三叉神经痛),感音神经性听力损失和前庭功能减退并不能通过肿瘤治疗逆转。
诊断性评价
颅脑薄层增强MRI检查是检测直径小至2毫米的前庭神经鞘瘤的标准诊断方法。影像学上的特征具有高度敏感性和特异性,在大多数病例中可以得到准确的放射诊断,而不需要活检证实(图2和3)。
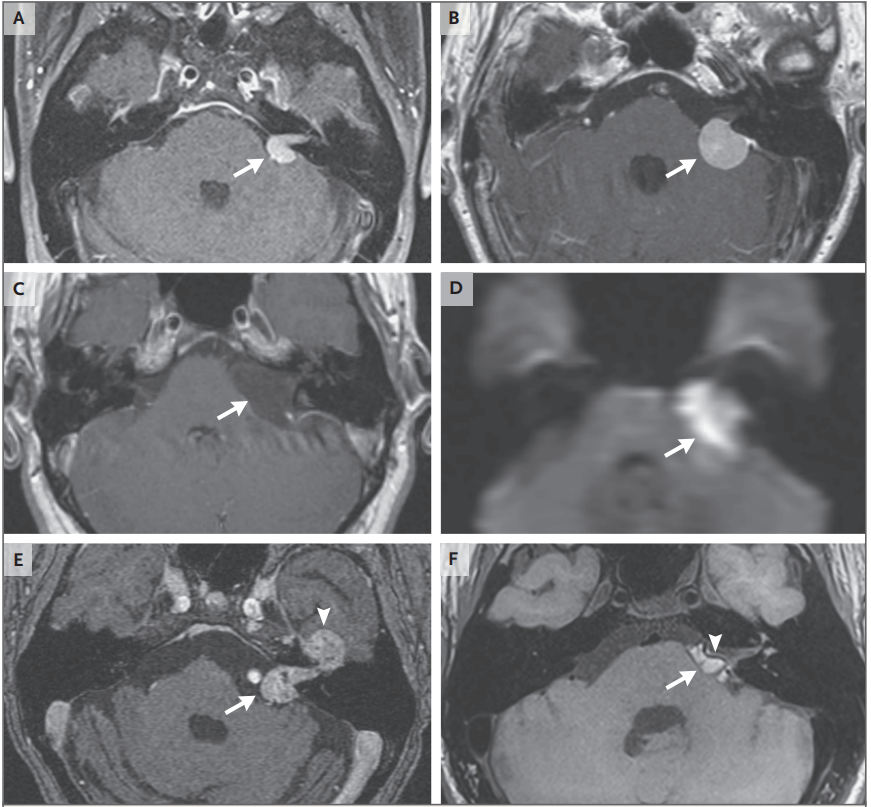
图3。CPA区桥小脑角肿瘤的影像学鉴别诊断。
图A为典型的左侧前庭神经鞘瘤,增强MRI检查示肿瘤充满内耳道,并侵犯至桥小脑角(箭头)。
图B(箭头)所示脑膜瘤是桥小脑角二常见的轴外肿瘤,典型表现为均匀的增强和较宽的硬膜基底,如。与前庭神经鞘瘤不同的是,后颅窝脑膜瘤较少累及内听道,通常向内侧耳道开口生长。
图C、D(箭头)表皮样肿瘤是桥小脑角三常见肿瘤,在T1和2加权上与周围脑脊液呈等信号,但在无回声平面弥散加权成像上特征性弥散受限。
图E(箭头)所示面神经鞘瘤可发生于面神经的任何部位,从脑干到支配面神经肌肉的末梢分支。面神经鞘瘤与此位置的前庭神经鞘瘤是很难区分的,除非肿瘤的横向延伸累及面神经管(箭头)。
如图F(箭头)所示桥小脑角脂肪瘤在增强MR表现为高信号,脂肪控制后信号消失。邻近神经和血管系统(箭头)通常穿过脂肪瘤,与此区域的大多数其他肿瘤不同,它沿着周围肿瘤包膜取代周围的神经血管系统。
提示需要MRI检查主要适应症包括通过纯音和言语测听检测到的突发性或不对称感音神经性听力损失有这样的病史,鉴别前庭神经鞘瘤的概率在1%到5%之间。
尽管不对称感音神经性听力损失的定义各不相同,但广泛采用的协议规定了纯音测听仪的任何耳间差异,即在两个相邻频率上大于或等于10db,或在任何单个频率上大于或等于15db(图3)。虽然不对称感音神经性听力损失的筛查方案已被广泛采用,但采用MRI检查单侧耳鸣或不对称前庭功能障碍的适应症尚未明确。
孤立性单侧前庭神经鞘瘤患者,如果没有2型神经纤维瘤的其他体征,且亲属没有相关体征,一般不需要进行基因检测,其家庭成员也不需要。2型神经纤维瘤病是一种少见的常染色体显性疾病,由NF2基因内的致病变异引起;将近一半的患者有阳性家族史,其余的病例是由新变异造成的。超过90%的2型神经纤维瘤患者会发生双侧前庭神经鞘瘤,尽管其他颅和脊髓神经鞘瘤、脑膜瘤、脊髓室管膜瘤、周围神经神经鞘瘤以及诸如青少年白内障和视网膜错构瘤等眼科表现也可能发生。
前庭神经鞘瘤治疗
前庭神经鞘瘤的治疗在过去的一个世纪中取得了进展,为大多数患者提供了多种合理的选择,这些选择与预期并发症发生率低和几乎没有死亡风险相关。治疗策略可分为观察等待-MR随访观察,显微外科手术,放疗,以及这些方法的组合。一些旨在阻止肿瘤生长的新药物疗法,包括阿司匹林和单克隆抗体,最近已得到探索,但仍在探索研究中。
到目前为止,没有高水平的证据表明一种治疗方法明确优于其他治疗方法。相反,每种策略都有其优点和局限性。此外,数据显示,诊断本身和患者相关因素对生活质量的影响大于治疗选择。肿瘤大小主要决定治疗建议;然而,决策也受到微妙的病人和提供者相关因素的指导。咨询到专科中心为患者提供了一个新的诊断机会,以获得有关肿瘤管理和疑难症状的潜在治疗的信息。鉴于各中心临床实践的差异,从较大的群体获得不止一种意见,并获得由独自的、全国性的患者支持组织提供的教育材料是值得鼓励的。
1、随访观察策略
这种随访观察的方法之所以受到欢迎,至少有两个原因:现在发现许多肿瘤是在症状轻微的老年人身上所发现的小的肿块;此外,过去15年的报告显示,在平均2.6 - 7.3年的随访中,有22 - 48%的肿瘤出现生长(通常定义为直径增加2mm)(文本S2)。在观察策略中,较一致的评估未来生长的因素是诊断时肿瘤的大小。通常,桥小脑角较大直径小于1.5 cm的肿瘤应考虑采取随访观察方法。
通常在诊断性MRI检查后6个月进行影像学和听神经评估,以识别快速生长的肿瘤或更具进袭性的病程的类似前庭神经鞘瘤。如果在6个月时没有生长,此后每年进行一次影像学和听力评估,直到5年,许多专家主张每隔一年进行一次评估鉴于肿瘤生长的不可评估性和跳跃或延迟生长的能力,建议终身随访。如果生长确实得到证实,大多数患者接受放射外科或显微外科手术的建议。为了最大水平地降低正在进行的肿瘤监测的成本和与对比剂相关的不良事件的风险,有些研究中心已经过渡到使用薄层、重T2加权的磁共振脑池成像而不使用对比剂,这种方法具有很高的准确性和评估者间的可靠性。
无论影像学上是否有肿瘤生长的证据,可在连续影像观察中发现听力下降的进展。尚不完全清楚导致未治疗肿瘤患者听力下降的机制,但可能包括耳蜗神经或迷路动脉的神经血管压迫、脑脊液循环受损和肿瘤介导的炎症。从丹麦的以人群为基础的数据分析显示,636例患者中有334例在诊断是有合适听力,语言辨别得分超过70%(表明病人70%的单词重复正确),但是经过十年的观察,只有31%保留的听力在这个阈值之上。值得注意的是,88%的患者在开始时的语言辨别得分为全切,但在10年之后仍然有超过70%的得分,这表明在诊断时出色的语言理解预示有良好的长期听力结果。
观察策略的一个重要问题是损耗。在一项涉及386例患者的法国研究中,16%的患者在随访观察策略的一年失访。遗憾的是,因为症状进展不是强烈与肿瘤生长相关联,且由于增长率是高度可变的,失访患者的风险增加,发展成一个大的肿瘤,而与有不良的最终治疗结果风险增加相关联。
2、放射外科
立体定向放射外科通常使用高度适形放射,定义为以1到5次分割向图像确定的靶区放射照射,且较大限度地保存周围组织。伽玛刀放射外科是适形放射治疗的一种。伽玛刀治疗包括192个同心排列的钴60放射源,以提供一个卵圆形等中心点的辐射。治疗通常包括立体定向头框和薄层、非对比增强计算机断层扫描和增强轴位MRI,以立体定向地在三维空间靶向肿瘤(图4)。基于直线加速器的平台也为许多中心所使用。这些系统大多包括一个单一的、准直的射线束和一个绕病人旋转的机架,形成一个聚焦的放射弧,立体定向地瞄准病灶并进行病变毁损。一般来说,整个治疗在门诊进行,放射外科治疗后的病人治疗后没有活动限制。
放射外科治疗神经鞘瘤的目的是防止肿瘤生长;放射外科治疗并不能治愈肿瘤,MR将无限期地显示肿瘤。虽然有超过一半的接受放射外科治疗后的患者最终会出现不同程度的肿瘤缩小,放射外科治疗后的头3年内,出现短暂的肿瘤增大是很常见的。患者在头3年每年进行一次听力评估和MRI检查,然后每隔一年直到10年,然后每5年无限期地进行一次听力评估和MRI检查。在当代放射外科研究系列中,超过90%的前庭神经鞘瘤患者在10年的随访中被报告得到肿瘤控制。放射外科治疗失败的典型特征是肿瘤持续生长3年以上,出现与进行性肿块占位效应相关的体征或症状,以及肿瘤迅速扩大。通常在放射手术失败后建议进行补救性显微外科手术,虽然在一些中心,在特定病例中重复放射外科治疗是成功的。
当患者肿瘤在桥小脑角的较大直径小于3.0 cm时,通常考虑采取放射外科治疗。然而,为了尽量减少放射性脑干水肿、三叉神经损伤或三叉神经痛、脑积水的风险,以及削弱对肿瘤的长期控制,较好选择小于2.5 cm的肿瘤。一些中心优先使用大分割或常规的多次分割的立体定向放射治疗,这可能允许治疗更大的肿瘤,而不是那些传统上认为是顺利的单次分割治疗。单次分割立体定向放射外科,瘤周剂量为≦13Gy,与取决于肿瘤体积的,有≦1%的长期性面瘫风险和<5%的三叉神经损伤病变风险相关。放射外科引起继发性肿瘤病变的风险接近0.02%。对放射外科对听力下降进展的影响仍存有争议,但许多中心报告在3 - 5年的随访期中,合适听力保存率为50 - 70%。合适听力指的是在使用或不使用助听器的情况下,仍然在功能上是有用的听力水平,由至少50%的语音辨别分数和≦50分贝(dB)的纯音平均阈值来定义。

图4前庭神经鞘瘤的放射外科治疗。
立体定向放射外科提供高适形放射照射影像定义的靶区,选择性地治疗肿瘤,较大限度地保留周围的正常脑组织(图A)。
目前迭代的(Elekta)伽玛刀,由192个钴60放射源同心排列,提供一个高度适形,卵圆形的辐射等中心点(图B)。治疗通常在放置立体定向头架后进行,患者在局部麻醉下,随后进行薄层、对比增强、轴位融合MRI计算机断层成像以靶向毁损肿瘤。根据治疗前听力状态和肿瘤体积,处方剂量通常为12 - 14Gy,50%等剂量线,以单次分割照射。右图所示的治疗计划要求将13Gy的处方剂量,50%等剂量线。即使是高度适形的计划,用洋红色标出的耳蜗,通常会受到不同程度的辐射。
大多数基于直线加速器(LINAC)的系统(图C)使用一个单一的、准直的辐射束和一个移动的机架来创建一个聚焦的辐射弧,使用无框架的立体定向;患者通常使用定制的软塑料面罩进行固定。治疗可以以单次或多次分割的形式给出。图中为Novalis LINAC系统(图C,上部),由TrueBeam STx 2018 (Varian Medical Systems and Brainlab)提供技术支持。治疗计划(右)处方12.5 Gy的剂量以单次分割照射到80%等剂量线。
Cyber-knife放疗(CyberKnife, Accuray)(图C,底部)是一种无框架、基于LINAC的放射治疗,通过具有6 df运动的高度机动的机械臂,并伴有实时动态图像引导。治疗计划(右)处方大分割放射,剂量为25Gy,分5次分割至80%等剂量线。
3、显微外科手术
显微外科手术可对各种大小的肿瘤进行切除,对于伴有症状性脑干压迫、脑积水、三叉神经痛或神经病变的大型肿瘤,或合并这些并发症的肿瘤,显微外科手术是优选的治疗方法。全部的手术都是在患者全身麻醉的情况下进行的,需要使用手术显微镜和术中神经监测。
用于切除前庭神经鞘瘤的三种主要显微外科入路是后乙状窦入路(retrosigmoid approaches)、颅中窝(middle fossa)和经迷路相关入路(translabyrinthine),每种入路都有优缺点(图5)。无论采用哪种入路,其主要目标是相同的:较大限度切除肿瘤,同时保留神经功能。术中常规使用面神经肌电图监测。当试图保留听力时,常用耳蜗神经监测,对于较大的肿瘤,可以考虑监测其他区域的颅神经。多数患者术后住院2 - 4天,出院时可走动。手术后的6 - 12周通常限制运动活动。在早期的恢复期,疲劳和持续的不平衡很常见,但通常在3个月内好转。大多数患者在手术后的头12个月内接受基线的术后MRI检查,术后定期进行MRI监测检查;检查的间隔时间取决于切除的范围和术后早期影像学的结果。大体全切除术后肿瘤复发的风险为0 - 2%。
初期主要外科手术的风险与肿瘤大小成正比,且大多与术后听力和面神经功能有关。40 - 70%的小肿瘤(直径<1.5 cm)患者的听力仍可维持,不到10%的患者的面瘫是长期性的。对于大于2.5 cm的肿瘤,术后保留听力的可能性小于5%,而大肿瘤全切除后长期性部分或完全性面神经麻痹的风险约为50%考虑到这样的风险,有意在面神经和脑干周围留下肿瘤残余已经流行起来。术后残留肿瘤生长的风险与残留肿瘤的体积成正比。但是一些一流的神经外科手术医者如德国INI Samii、Bertalanffy教授的研究和临床病例结果远远优于这样的结果,面听神经功能保留率在20年前就达到了国际较前沿,他们为世界各地复杂听神经瘤患者(复发、较大肿瘤等)手术数千台,肿瘤切除率达90%、面神经功能保留率达90%、听力保留率60%以上。总的来说,大约30%的肿瘤在肿瘤次全切除术后会有程度的再生长,通常采用放射外科治疗。幸运的是,发生其他主要神经血管并发症的风险,如对其他区域颅神经的长期性损伤或围手术期卒中,是少见的,即使是大肿瘤术后,脑脊液漏的患病率为9-13%,无菌性脑膜炎的患病率为2 - 4%,培养阳性的细菌性脑膜炎的患病率为1%。已发表的数据表明,大型医疗中心的短期疗效最佳,住院时间较短,成本较低。

图5.前庭神经鞘瘤的显微外科治疗。图示为切除前庭神经鞘瘤的经迷路的、后乙状窦和颅中窝显微外科手术入路。箭头表示进入的方向。
(图A)经迷路开颅切除肿瘤术是不可避免地需要牺牲听力功能,因为它需要磨钻内耳。该手术方法包括耳后切口,移除耳道和乙状窦之间的骨,移除半规管到达内听道(IAC)和桥小脑角(CPA)。该入路的优点包括减少回缩小脑的需要,充分进入IAC外侧的较大范围,以及早期识别面神经远端。理论上,任何大小的肿瘤都可以通过这种方法切除。在肿瘤切除后,移植腹部脂肪填补骨缺损,以减少术后脑脊液漏的风险。
(图B)乙状窦后入路开颅切除肿瘤术是一种通用的治疗选择性肿瘤的方法,它为CPA提供了一个广扩的视野和保留听力的可能性。该手术需要一个曲线的、垂直方向的枕骨切口,以及分别位于乙状窦和横窦后方和下方的开颅术。一旦硬脑膜被打开,就要磨除内听道IAC的后界,以暴露延伸到这个骨性管道的肿瘤。磨钻通常受到后半规管和前庭的限制,如果要保留听力,这些部位不能被损害。与经迷路入路一样,任何大小的肿瘤均可经后乙状窦入路进入。
(图C)中颅窝入路通常仅用于局限于IAC的小肿瘤或向CPA内侧延伸小于1cm的肿瘤,当保留听力是主要目标时。入路包括颞切口和正中颧骨根上方的开颅术。然后在颞硬脑膜下进行硬膜外剥离,移除覆盖IAC的骨头以进入肿瘤。这种方法的优点是它允许术中处理整个IAC内的肿瘤,并与小肿瘤患者的听力保存率相对较高有关。一个潜在的缺点是需要颞叶牵拉,与其他治疗类似大小肿瘤的方法相比至少是发生暂时的面瘫的风险略高。
4、康复
在大多数前庭神经鞘瘤患者中,长期的面神经功能仍然良好,并且对单侧听前庭神经功能障碍有足够的补偿。然而,一些患者需要康复干预,较常见的如有长期面神经麻痹、双侧听力下降或慢性头晕或不平衡的患者。
对于患有前庭神经鞘瘤,但同侧耳朵仍能维持合适听力的患者,观察(即不需要额外的听力康复)或使用传统助听器通常是足够的。然而,在大多数患者中,非合适听力最终会在受累的耳朵中发展,导致声音定位受损和在背景噪音存在下理解言语的困难。如果进行听力康复,大多数可用的选择包括通过外科手段(如骨传导植入)或非手术手段(如对侧信号路由[CROS]助听器)将声音从聋耳传到听力较好的耳朵。散发性前庭神经鞘瘤患者接受人工耳蜗植入术以恢复听力目前仍在研究中。初步数据显示,经过精心挑选的植入人工耳蜗的患者中,有50 - 85%能够理解语言。然而,这一策略仅适用于耳蜗神经未受到显微手术或放射外科严重损伤的患者(图4)。尽管有这些选择,但只有不到三分之一的前庭神经鞘瘤患者最终接受了听力设备的试用,只有大约20%的人经常使用这种设备,部分原因是这些技术的局限性,但也因为大多数人能够充分地适应严重听力障碍。
慢性头晕或不平衡,伴随跌倒风险,很少与疾病进展或肿瘤治疗相关,通常是多因素导致的。可能加剧头晕的常见情况,包括周围神经病变、年龄相关的对侧前庭功能丧失、视力丧失和前庭性偏头痛。因此,严重头晕或不平衡的患者应该接受多方位的平衡评估,以准确识别任何并存的疾病,并评估和减轻跌倒的风险。哺乳动物的外周前庭系统再生能力有限。因此,平衡疗法是治疗慢性前庭功能减退相关症状患者的主要方法。
总体上,长期性面神经麻痹并不常见,但在接受显微外科手术切除的大肿瘤患者中,其风险接近50%。松弛性麻痹和眼部干燥是术后早期的主要问题。虽然许多面神经损伤的红斑(the stigmata)可以选择性处理,但需治疗闭眼不完全,以减少通常表现为视力模糊、眼痛和发红的暴露性角膜病的风险。眼部润滑剂(Eye lubricants)和眼睑保湿(moisture chambers)通常在术后早期可提供足够的保护。然而,如果预期长期瘫痪或出现眼科并发症,则应考虑咨询眼科医生将上睑配重闭合(uppereyelid weight placement)、泪管堵塞(punctal plugs)或睑缘缝合术(tarsorrhaphy)。显微手术后面神经恢复的速度和程度是可变的。一般情况下,面瘫起病后6个月内有最大水平的好转,但对持续18个月的长期性面神经麻痹的治疗很复杂,而且可能对时间敏感。因此,对于严重面神经麻痹患者,如果在头6个月内没有好转,应考虑专科诊所就诊。
结论
随着神经诊断影像学检查手段的增加,偶发性、无症状性前庭神经鞘瘤患者近年来日益增加。如今,通常在肿瘤很小的情况下,以及在轻微或偶然出现症状的老年患者中,就能作出诊断。治疗策略已经进化到优先考虑神经功能结果而不是最终切除肿瘤。显微外科手术通常是治疗直径大于3cm的肿瘤的优选。然而,在缺乏高水平来指导决策因素的情况下,对于大多数小或中等大小的前庭神经鞘瘤患者,有多种合理的治疗选择,包括随访观察、放疗和显微外科手术。同时治疗中心或手术医师的经验、技术水平对患者的治疗决策建议、治疗预后结果起着较关键的作用。
资料来源:DOI: 10.1056/NEJMra2020394




