James T.Rutka(鲁特卡)教授曾任世界神经外科学院院长,30多年来深耕儿童神外研究,带领团队不断突破,从脑瘤分子分型、精准治疗、新药治疗、微创治疗,为全球神经外科疑难病患儿带来希望,他发表了研究《PINK1 Is a Negative Regulator of Growth and the Warburg Effect in Glioblastoma》(PINK1是胶质母细胞瘤生长和Warburg效应的负调控因子),以下是研究简述(本篇将重点介绍研究方法及设计)。

01
PART
摘要
增殖的癌细胞具有高糖酵解率、高乳酸生成和改变的线粒体代谢的特征。这种代谢重编程为肿瘤细胞(包括胶质母细胞瘤)的增殖提供了重要的代谢产物。然而,这些生物过程会产生氧化应激,必须通过清除活性氧来平衡。
我们在非转化的人星形胶质细胞中使用一种无偏的逆转录病毒功能缺失筛选,证明线粒体PTEN诱导激酶1是Warburg效应的调节因子和胶质母细胞瘤生长的负调控因子。我们报告,PINK1的缺失通过ROS依赖性的缺氧诱导因子-1α稳定化和丙酮酸激酶肌肉同工酶2活性降低(两者均为有氧糖酵解的关键调节因子)来促进Warburg效应。
从机制上讲,PINK1通过FOXO3a(氧化应激和超氧化物歧化酶2的主要调节因子)来抑制ROS和肿瘤生长。这些发现突出了PINK1和ROS平衡在正常细胞和肿瘤细胞中的重要性。
在大量人脑肿瘤(包括胶质母细胞瘤,n>900)中观察到PINK1缺失,并与患者不良生存相关。PINK1过表达在原位小鼠异种移植模型和果蝇转基因胶质母细胞瘤模型中减弱了体内胶质母细胞瘤的生长。
02
PART
引言
胶质母细胞瘤是所有胶质瘤中十分常见和致命的,平均生存期约为12-16个月。通过受体酪氨酸激酶激活的Ras信号通路激活和p53缺失是驱动人类疾病和小鼠胶质母细胞瘤模型中肿瘤形成的两个关键胶质母细胞瘤改变。癌症基因组图谱进一步验证了这些通路以及先前在胶质母细胞瘤中未知的新改变。然而,这些改变中的绝大多数很可能是“乘客”改变,即不参与癌症发展的改变。功能基因组学策略通常用于识别驱动癌症发生、进展和治疗耐药的重要基因,这最终补充了大尺度测序策略。基因插入策略(包括Sleeping Beauty转座子方法)的实施已导致鉴定出几种新的癌症基因。我们假设,在相关胶质母细胞瘤通路(包括Ras或p53信号)中存在改变的非转化星形胶质细胞,可以通过随机逆转录病毒插入来灭活参与起始和/或进展的基因,从而实现转化。
使用逆转录病毒筛选,我们鉴定出PTEN诱导激酶1是肿瘤细胞利用的众多细胞过程的负调控因子。PINK1是一种线粒体丝氨酸/苏氨酸激酶,在家族性帕金森病患者中发生突变,并调节从线粒体自噬到活性氧产生和氧化磷酸化等多种生物学功能。众所周知,肿瘤抑制基因和癌基因的失调经常影响细胞内ROS水平。癌细胞不断面临平衡氧化应激和控制ROS水平的挑战,因为ROS同时发挥促生长和抗生长作用。我们报告,PINK1通过调节线粒体氧化磷酸化、有氧糖酵解和ROS来抑制胶质母细胞瘤生长。
03
PART
材料与方法
01细胞培养
如先前所述,从p53-/-(1周龄)、NMA-P0(CD1小鼠)建立和表征星形胶质细胞培养物。胎儿人星形胶质细胞购自Lonza。U87和T98G细胞系购自ATCC。SF188细胞系由Chris Jones博士(英国伦敦癌症研究所)惠赠。所有细胞先前均已于2011年通过短串联重复序列分型进行过表征和鉴定。细胞系在DMEM中生长,并补充10%胎牛血清。如先前所述培养胶质瘤干细胞。
耗氧量和糖酵解通量测定
使用Seahorse XF96分析仪测量耗氧量。细胞在其常规生长培养基中培养,并用无缓冲培养基重铺于XF96板中。在转移至XF96分析仪之前,将细胞在无CO2的37°C培养箱中平衡至无缓冲培养基90分钟。我们测量基础OCR,然后依次注射1.2μmol/L寡霉素、1.0μmol/L FCCP和1.0μmol/L鱼藤酮。通过Seahorse XF96分析仪测量细胞外酸化率作为糖酵解通量的指标。
蛋白质印迹分析和免疫组化
如先前所述进行蛋白质印迹分析和免疫组化。抗体使用以下稀释度:β-肌动蛋白、PINK1、半胱氨酸次磺酸、HIF1A、PKM2、纽蛋白、V5、PDHK1、磷酸化PDHE1a、PDHE1a、HK2、LDHA、磷酸化FOXO3a ser294、FOXO3a、HA-Tag、SOD2。免疫组化用抗体:PINK1 1:100和ki67 1:100。
体内小鼠模型实验
按照SickKids医院的动物护理规范饲养小鼠,并在审查提交的方案后获得批准。在NOD-SCID小鼠中进行立体定向引导颅内注射。通过在裸鼠NOD-SCID小鼠侧腹注射与Matrigel混合的2 x 10^6个细胞进行侧腹注射。监测小鼠肿瘤生长,并用卡尺测量肿瘤体积。
果蝇研究
所有实验果蝇杂交在25°C的昼夜节律培养箱中维持,用于产卵和幼虫发育。在游走期晚三龄幼虫阶段解剖果蝇幼虫脑用于肿瘤体积比较和免疫组化。包括:小鼠抗Repo和兔抗磷酸化组蛋白3。如先前所述进行荧光成像和体积测量。
其他方法
溴脱氧尿苷细胞增殖实验、caspase活性实验、克隆形成实验、己糖激酶活性和PKM活性实验均如先前所述进行。
统计分析
所有实验重复三次,适当时报告均值和标准误。多组比较采用ANOVA,随后进行事后Dunnett检验(与一个对照组比较)或事后Tukey检验(识别亚组间差异)。直接比较使用非配对双尾学生t检验。使用对数秩生存检验进行生存分析。显著性设定为*,P<0.05。
04
PART
结果(其三)
研究最终发现9个结果,由于篇幅限制,本篇将先展示其中三个,其余将在明天的文章中展现,敬请关注。
逆转录病毒基因捕获及捕获克隆的功能表征
从正常CD1-ICR小鼠、新生超活化Hras小鼠和p53缺失小鼠建立原代星形胶质细胞培养物。为了鉴定导致早期传代星形胶质细胞转化的功能缺失事件,我们用含有剪接受体(紧接在荧光素酶报告基因和IRES嘌呤霉素抗性标记上游)的逆转录病毒基因捕获载体转导星形胶质细胞。通过嘌呤霉素筛选,我们选择了32个抗性克隆,其中14个表达荧光素酶。在这14个不同背景的表达荧光素酶的基因捕获克隆中,有9个在软琼脂糖中生长(转化能力的衡量指标)。尽管产生了5个嘌呤霉素抗性的表达荧光素酶克隆,但NMA未被转化。反向PCR鉴定了9个锚定非依赖性基因捕获克隆中7个的基因插入位点。GT-15和GT-16先前在胶质瘤生物学中有报道。我们鉴定的四个基因先前未涉及胶质母细胞瘤发病机制,并进一步表征了其细胞生长、抗凋亡和侵袭能力。
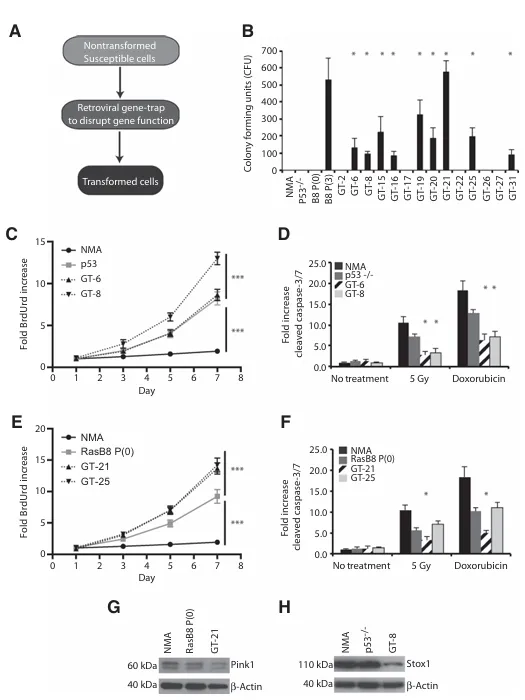
图1:逆转录病毒基因捕捉技术与受困克隆的功能特性分析。A,逆转录病毒基因捕捉的总体策略。B,表达萤火虫荧光素酶的受困克隆在软琼脂培养试验中表现出显著的生长优势(9/14)这与未转化的星形胶质细胞形成鲜明对比。从5000个细胞进行播种后第14天开始计数克隆形成单位。C,基于p53背景的基因捕捉克隆的BrdUrd增殖试验。D,针对基因捕获克隆的激活型裂解型Caspase-3和-7ELISA检测。E,基于RasB8背景的基因捕捉克隆的Brdurd增殖试验F,对来自RasB8星形胶质细胞的基因捕获克隆进行了激活的裂解型Caspase-3和-7 ELISA检测。G-H,Nestern印迹分析显示,与亲代细胞相比,捕获的克隆中Pinkl和Stoxl的表达水平有所降低。上方的条带代表完整长度的Pink1,下方的条带则代表Pink1在整合入线粒体后所形成的成熟形式。P<0.05;***,P<0.001
在p53-/-背景下,我们在以下基因中鉴定出插入:GT-6和GT-8。与亲本p53-/-细胞相比,通过7天的BrdUrd增殖实验测量,GT-8细胞而非GT-6细胞增殖增加。与亲本p53-/-细胞和未修饰的小鼠星形胶质细胞相比,GT-6和GT-8在暴露于5 Gy辐射或1μmol/L阿霉素后均表现出caspase活性降低。与对照细胞相比,GT-6和GT-8在用5 Gy辐射处理时集落形成增加。
在Ras-B8 P0背景下,我们表征了GT-21和GT-25。与对照相比,通过7天的BrdUrd掺入测量,GT-21和GT-25细胞增殖增加。与对照细胞相比,GT-21和GT-25在暴露于5 Gy辐射和阿霉素处理后显示caspase活性降低。与对照细胞相比,GT-21在用5 Gy辐射处理时集落形成增加,并且GT-21细胞是唯一侵袭性增加的细胞。总之,GT-21在所有四个测试实验中均有改变。蛋白质印迹分析证实,这些基因捕获事件改变了我们两个顶级候选基因PINK1和STOX1的蛋白质表达。
PINK1缺失改变正常人星形胶质细胞代谢
为了研究我们的顶级候选基因PINK1在人类细胞系统中对细胞生长、氧化应激和线粒体功能的作用,我们在正常胎儿人星形胶质细胞和几个已建立的人胶质母细胞瘤细胞系中进行了功能验证。在原代人胎儿星形胶质细胞培养物中检测到PINK1表达,但在大多数胶质母细胞瘤细胞系和外植体培养物中呈低表达或阴性。细胞分级分析表明PINK1主要定位于线粒体。由于PINK1缺失对正常人星形胶质细胞的影响尚不清楚,我们通过两个靶向PINK1的混合shRNA构建体以及一个将V5表位标记的PINK1重新导入敲低细胞的PINK1拯救细胞系,生成了稳定的PINK1敲低克隆。与乱序对照和PINK1拯救细胞相比,PINK1敲低导致7天内细胞计数测量的增殖增加。我们在PINK1敲低和对照细胞中未观察到线粒体拷贝数或细胞大小的变化。接下来,我们使用细胞可渗透的荧光探针测量氧化应激和ROS。PINK1敲低细胞具有升高的内源性ROS水平,与胶质母细胞瘤细胞相当,而对照和PINK1拯救细胞的ROS量显著较低。
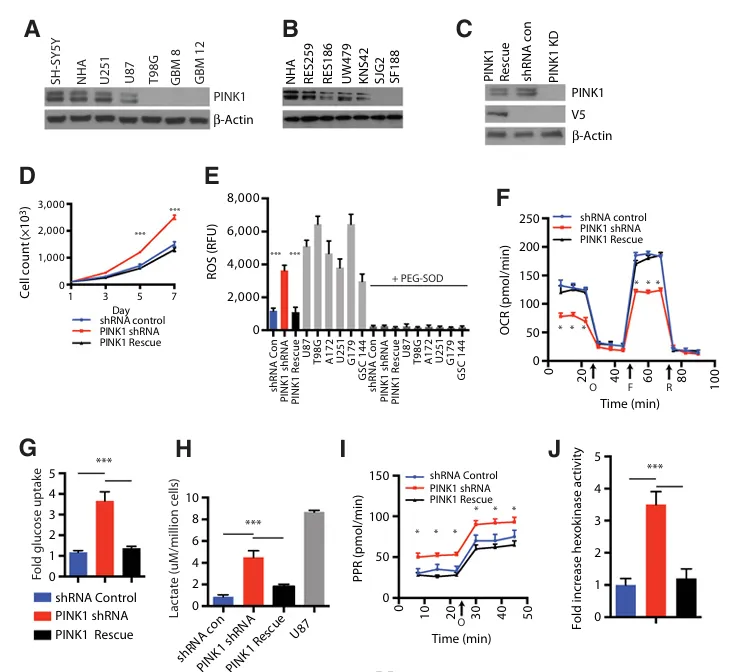
图2:PINK1的缺失会改变星形胶质细胞的正常代谢。
A,Wester印迹分析显示NHAs、胶质母细胞瘤细胞系和胶质母细胞瘤组织样本(GBM8和GBM12)中PINK1的表达存在差异。
B,针对儿科胶质母细胞瘤细胞系中PINK1的Westem印迹分析。
C,对NHAs中通过稳定shRNA敲低PINK1的结果进行Western印迹分析,与shRNA控制的NHAs和带有V5标签的PINK1恢复NHAs进行比较。
D,对PINKIshRNA NHAs与对照shRNA NHAs进行细胞计数分析。
E,对NHA的对照shRNA、PINK1敲低细胞和胶质母细胞瘤细胞进行了内源性ROS检测。测量工作是通过使用一种对ROS敏感的探针(1umolL氯甲基-H2DCFDA)来进行的。荧光ROS信号在加入100u/mL PEG-SOD后被猝灭。F,NHAs与带有PINK1敲除的NHAs在暴露于不同生物能量调节剂(如寡霉素(O)、碳酰氰基4(三氣甲基)苯基踪(FCCP/F)和罗丹明(R))后所呈现的OCR比较。箭头标记化合物添加的时点。
G,通过用荧光葡萄糖类似物2-NBDG进行孵育来测量细胞中的葡萄糖摄取量。U87细胞被用作阳性对照。
H&D中描述的细胞中的细胞外乳酸含量是通过一种NADH耦联酶反应方法进行测量的,并于第3天以490 nm的吸光度值进行测定,同时将其与细胞数量进行归一化处理。U87细胞被用作阳性对照。
I,糖酵解通量分析测量。在U87空载体对照细胞与U87PINK1过表达细胞之间比较,测定了质子生成速率(PPR,pmol/min)。
J,总HK活性的倍数增加情况,以细胞中的随机shRNA为参照进行归一化处理。
为了将探针氧化的变化归因于ROS,当实验重复并添加100 U/mL PEG-SOD时,荧光信号被阻断。作为荧光信号的附加对照,我们用氧化不敏感类似物探针重复实验,未观察到组间荧光变化,支持我们基于DCFH2的ROS测量是由于探针氧化。用线粒体抗氧化剂mito-TEMPO处理PINK1敲低细胞可抑制ROS,但用NADPH氧化酶抑制剂处理时则不能,支持PINK1抑制线粒体ROS。在PINK敲低细胞中过表达HA标记的线粒体超氧化物歧化酶2可抑制ROS,并完全拯救了由PINK1敲低诱导的几种表型,即细胞生长、葡萄糖摄取、乳酸、己糖激酶和丙酮酸激酶活性。
与对照相比,PINK1缺失导致基础耗氧率显著降低,最大基础糖酵解显著降低,当用寡霉素处理时糖酵解能力更高。在敲低细胞中观察到己糖激酶活性增加和几种糖酵解基因的表达增加,但在对照细胞中未观察到。
PINK1缺失促进PKM2失活并稳定HIF1A
丙酮酸激酶M2亚型、HIF1A及其靶基因已知对有氧糖酵解至关重要。多项研究表明,与非转化细胞相比,癌细胞具有升高的糖酵解和降低的PKM2活性,这与乳酸增加相关。在高糖酵解细胞中观察到PKM2活性降低的一种机制是由ROS介导的。与对照和拯救细胞相比,PINK1敲低细胞的总丙酮酸激酶活性降低。我们的NHA细胞表达PKM2而非PKM1,使得我们的测定对PKM2活性具有特异性。
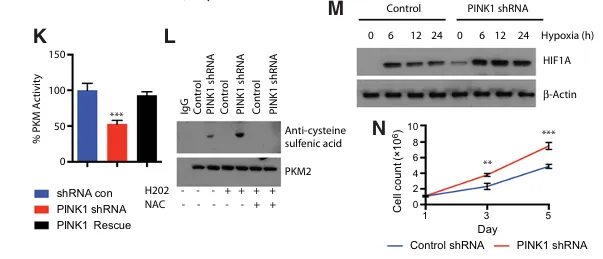
续图2:K,对盟shRNANHAs与PINK1 shRNA NHAs的丙酮酸激陶活性测定结果对比。PKM活性测定于第3天进行,并以10克细胞裂解物为参照进行归一化处理。
L,1%65DS中PKM2的免疫沉淀分析,通过标准Westerm方法与抗半胱氨酸砜抗体进行印迹,显示在有或无H202(1mmolL)、氧化剂及N乙酰半胱氨酸(NAC,5mmoUL)存在的情况下PKM2上的氧化半跳氨酸残基。
M,Westem印迹结果显示,在暴露于正常氧环境和不同时间点的缺氧(氧分压为1%602)条件下,对照细胞和PINKI敲低细胞中HIF1A的稳定性均得到维持。
N,对PINK]shRNA NHAs与对照shRNA NHAs在1%缺氧环境下的细胞计数进行对比分析的结果,P<0.05;*,P<0.01;**,P0.001
ROS是PKM2的负调控因子,可氧化PKM2上的半胱氨酸残基,阻止其有效活性所需的四聚化,并假设PINK1敲低细胞中升高的ROS可能通过氧化半胱氨酸氨基酸降低PKM2活性。我们在来自PINK1敲低细胞的PKM2免疫沉淀物中检测到氧化的半胱氨酸氨基酸,但在对照中未检测到。用过氧化氢处理进一步增加了PKM2中氧化半胱氨酸的水平。这种增加被强还原剂N-乙酰半胱氨酸的添加所消除。升高的ROS水平也显示可增加和稳定HIF1A信号。我们还在常氧条件下在PINK1敲低的NHA中观察到HIF1A蛋白水平增加,但在对照细胞中未观察到。在1%低氧条件下处理的PINK1敲低细胞在多个时间点维持显著增加的HIF1A蛋白水平,并且在低氧期间增殖增加。作为验证,调节向糖酵解代谢转变的HIF1A靶点LDHA、PDK1和PKM2在PINK1敲低细胞中上调。当PINK1敲低细胞在常氧和低氧下用HIF1A siRNA处理时,细胞增殖和侵袭得到部分拯救。用NAC处理的PINK1敲低细胞在常氧和低氧条件下HIF1A水平降低,导致ROS减少和细胞倍增时间增加。




