帕金森病是什么病?帕金森病(PD)是比较常见的,全世界大约有1000万人患有这种疾病,而中国就有大约300万帕金森病患者,并且每年新发人数达10万以上。帕金森病是什么病呢?INC国际神经外科医生集团旗下世界神经外科顾问团成员Joachim K. Krauss教授表示,帕金森病(PD)是一种神经退行性疾病,它是以伦敦医生詹姆斯·帕金森的名字命名的,他在1817年一次报告了这种症状。帕金森病主要影响中老年人:患者静止时,手和嘴常发生不自主的震颤、行动缓慢、肌肉僵直,此外还伴随着认知和精神障碍、抑郁等。较重要的是,帕金森病情发展只能尽量控制,无法逆转。
每个帕金森患者都有不同的症状,但常见的症状是震颤、肌肉僵硬和行动迟缓。全部与运动有关的症状,被称为运动症状。许多帕金森患者还会经历其他与运动无关的问题,如疼痛、焦虑和抑郁。这些被称为非运动症状。
我们的运动是由大脑中的神经细胞(神经元)控制的,它们利用一种叫做神经递质的化学物质,将信息传递给其他细胞和身体的其他部位。大脑中一个叫做黑质的区域产生一种控制运动的神经递质:多巴胺。在帕金森氏症患者中,70-80%的产生多巴胺的细胞逐渐恶化并消失--这被称为神经退行性变。多巴胺产生神经元的缺失导致大脑中控制运动和平衡的部分多巴胺水平降低。当神经细胞不能很好地传递大脑信息时,运动就不能很好地控制,帕金森氏症就会出现。
帕金森病是什么病?该怎么治疗?帕金森病会影响人的一生,但不会降低患者预期寿命。针对帕金森病额治疗,虽然目前还没有治愈帕金森氏症的方法,但是西方发达国家在过去的半个世纪,帕金森病(PD)的治疗取得了较大的进展。由于实验治疗学的进步,许多有前途的PD治疗方法正在出现。
在西方发达国家,主要使用左旋多巴仍来控制PD症状。在进行药物治疗之前,需对帕金森病作出正确的诊断,并确定患者的运动、感觉、自主和心理障碍程度(表1)。每个病人的治疗都是个体化的,目前除左旋多巴外,还有其他多种药物可用。其中包括多巴胺激动剂(DA)、邻苯二酚-甲基转移酶(Cmt)控制剂和非多巴胺能药物(图1)。
表1:帕金森病治疗指南

图1:可供PD使用的药物治疗方案
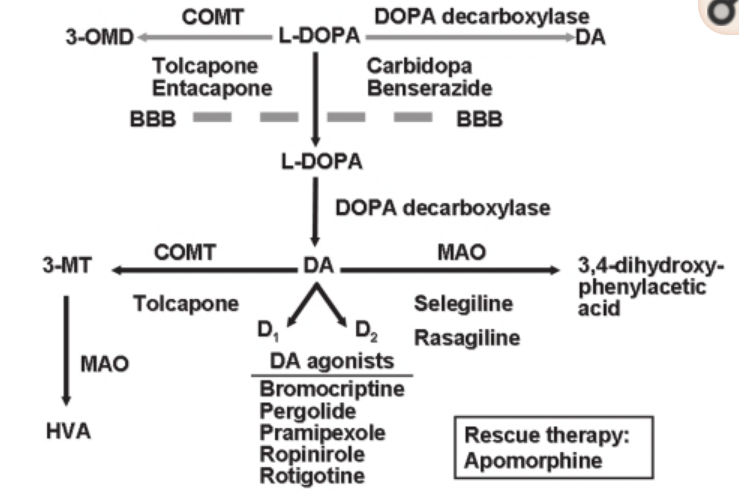
缩略语:BBB,血脑屏障;COMT,邻苯二酚O-甲基转移酶;DA,多巴胺;L-DOPA,3,4-二羟基-L-苯胺;HVA,高香草酸;3-MT,3-甲氧基特拉明;MAO,单胺氧化酶.
左旋多巴是控制PD症状较合适的药物,特别是与运动迟缓相关的症状。然而,由于左旋多巴治疗常与运动并发症相关,如波动和运动障碍,因此在PD过程中何时较适合开始左旋多巴治疗仍存在争议。外周多巴脱羧酶控制剂卡比多帕的加入,增强了左旋多巴的治疗效果。对恶心、呕吐等周边副作用特别敏感的患者,可在常规卡比多帕/左旋多帕制剂中添加卡比多帕。
大多数接受左旋多巴治疗的患者在5年治疗后出现运动波动、运动障碍或其他并发症)由于运动波动和运动障碍主要与左旋多巴治疗的剂量和持续时间有关,大多数帕金森病学家主张采用旨在延迟左旋多巴治疗的治疗策略,以延迟左旋多巴相关运动并发症的发生。
对于一些药物已经不能控制帕金森病病情的患者,西方发达国家常会采用深部脑刺激(DBS)来治疗帕金森病。DBS也是目前治疗帕金森病的非药物合适疗法,1990年代初,Jean Siegfried在苏黎世创立了深部的脑电较刺激DBS手术疗法,作为治疗帕金森氏症的替代疗法。在后续的运用中,Joachim K. Krauss教授和法国的Coubes教授在上世纪90年代末将其好转,并具有提出性的运用在治疗肌张力障碍上。最初,Joachim K. Krauss教授的方式遭到了医学界的质疑,然而在随后的多次研究中,DBS手术疗法被证实在治疗肌张力障碍上发挥了重要的作用,可作为肌张力障碍患者选择的靶点之一。Joachim K. Krauss教授也是目前国际上擅长治疗帕金森病的教授之一。
在国内,对于帕金森病的治疗,也主要是以上疗法,左旋多巴和DBS,药物主要靠进口,新的技术也是向西方发达国家学习。对于帕金森病的新药、新疗法,也是需要很长一段时间才能引进到国内,所以患者想要及早的享受的新药、新疗法,出国治疗也是一个新的选择。比如Joachim K. Krauss教授所在的德国汉诺威医学院(MHH),对于帕金森病的研究已经走在国际,患者在这里可以提前享受的新的治疗。由于Joachim K. Krauss教授是INC国际神经外科医生集团旗下世界神经外科顾问团成员,对于想寻求Joachim K. Krauss教授及其所在医院的国际前沿治疗的帕金森病患者,可通过INC国际神经外科医生集团获得国际远程咨询及出国治疗的相关帮助。
参考文献:Allain H, Cougnard J, Neukirch HC, et al. Selegilene in de novo parkinsonian patients: the French selegiline multicenter trial. Acta Neurol Scand. 1991;136:73-8.
Anderson VC, Burchiel KJ, Hogarth P, et al. Pallidal vs subthalamic nucleus deep brain stimulation in Parkinson disease. Arch Neurol. 2005;62:554-60.
Assal F, Spahr L, Hadengue A, et al. Tolcapone and fulminant hepatitis. Lancet. 1998;19:958.[PubMed] [Google Scholar]
Barone I, Rektor I, Bares M, et al. Pramipexole and pergolide in the treatment of depression in Parkinson’s disease: a national multicentre prospective randomized study. Eur J Neurol. 2003;10:399-406.
Baronti F, Davis TL, Boldry RC, et al. Deprenyl effects on levodopa pharmacodynamics, mood and free radical scavenging. Neurology. 1992;42:541-4.
Bejjani BP, Gervais D, Arnulf I, et al. Axial parkinsonian symptoms can be improved: the role of levodopa and bilateral subthalamic stimulation. J Neurol Neurosurg Psychiatry. 2000;68:595-600.[PMC free article]




