10年内病人反复手术、放疗,为何肿瘤仍然越长越大还恶变升级,症状越来越严重,为何会造成无效治疗?本文对这样的病例进行了详析。
前庭神经恶性肿瘤较为少见,既往诊断为前庭神经鞘瘤的恶性变更为少见,迄今为止只有少数的病例文献报道。关于小到中等大小的前庭神经鞘瘤(VS)的理想治疗方法仍然存在争议,在过去的十年中,伽玛刀放射外科治疗变得越来越流行,并且已经有肯定的临床结果的报道。在这个病例报告中,我们描述一例对前庭神经鞘瘤(VS)接受肿瘤切除后的残余肿瘤进行放射外科治疗后10 年恶性变为伴有腺性分化(glandular differentiation)恶性周围神经鞘肿瘤(malignant peripheral nerve sheath tumor ,MPNST )。

听神经瘤怎样合适治疗?
前庭神经鞘瘤(VS)在伽玛刀放射外科手术(GKS)后的恶性变较为少见,但潜在的严重并发症会导致预后不良。已经有少量病例报道,但仅限于单个病例报告。本文提供了一例54岁男性桥脑小角肿瘤患者,主诉右侧听力障碍持续11 年。患者于2004年5月在另一所医院经乙状窦后入路(retrosigmoid approach)行肿瘤切除,并行次全切除。病理诊断为前庭神经鞘瘤(VS)。一年后,伽玛刀放射外科手术(GKS)控制残留肿瘤。伽玛刀治疗两年后,病人咨询至该医院,进行二次手术切除,行次全肿瘤切除,病理显示为前庭神经鞘瘤(VS)。临床和放射影像学随访按每 6个月进行。2014年4月出现临床症状恶化,肿瘤生长,经乙状窦后入路三次肿瘤切除,达到次全切除。病理证实为恶性周围神经鞘瘤(malignant peripheral nerve sheath tumor,MPNST)。虽然这种情况很少见,但在治疗前庭神经鞘瘤时应注意伽玛刀放射外科治疗后的前庭神经鞘瘤恶性变。
该病例明确涉及伽玛刀放射外科(GKS)治疗后的前庭神经鞘瘤( VS)的恶性变,且经多次组织病理学分析证实。前两次组织病理学分析显示为良性前庭神经鞘瘤,最后一次组织病理学分析显示恶性(恶性周围神经鞘瘤MPNST)。在该病例中,MIB-1指数为4%,Ki-67染色指数可作为部分或次全切除的听神经鞘瘤的再生长的指标。MIB-1指数>2%与肿瘤倍增时间(tumor double time,TDT)呈相关。
病例介绍
54岁男性患者,右利手,没有神经纤维瘤病的家族病史,有11年的右侧听力障碍和眩晕病史。神经系统检查显示右侧听力障碍,纯音听阈58.5 dB(分贝)。一边耳朵听不清,这导致他跟家人的沟通慢慢地出现了困难,经常头晕目眩让他每天都感到疲惫,他的脾气渐渐也变得不好,家人都说原来那个亲切和蔼的他不见了。

放射影像学发现
最初的MR影像,轴为钆剂增强T1加权MR影像显示右侧小脑桥角肿瘤异质性强化,肿瘤侵袭右侧内耳道(IAC),怀疑前庭神经鞘瘤。
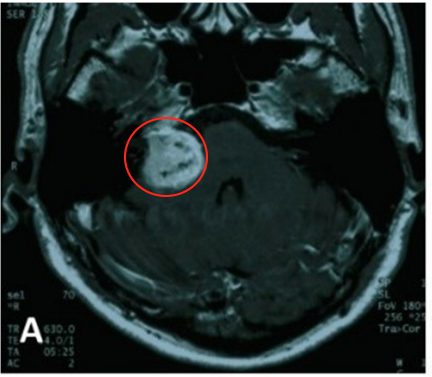
图1. A.2004年4月最初等 MR图像,轴位钆剂(Gd)增强T1加权MR图像显示右侧小脑桥角肿瘤不均匀强化。

B.在2005年8月1日一开始手术后SRS治疗之前的轴位钆剂(Gd)增强T1加权图像MR图像。

C. 2007年5月二次切除术前轴位钆剂(Gd)增强T1加权MR图像。D.二次切除术后1 个月轴位钆剂(Gd)增强T1加权MR图像。

E. 2008年5月随访的轴位钆剂(Gd)增强T1加权MR图像。F.2009年11月随访的轴位钆剂(Gd)增强T1加权MR图像。

G. 2010年11月轴位钆剂(Gd)增强T1加权MR图像。H. 2011年11月随访的轴位钆剂(Gd)增强T1加权MR图像。I.2012年11月随访的轴位钆剂(Gd)增强T1加权MR图像。J. 2013年11月随访的轴位钆剂(Gd)增强T1加权MR图像,显示肿瘤开始生长。

K和L.2014年4月轴位钆剂(Gd)增强T1加权MR图像,显示不均匀强化伴有脑干受压,行三次手术切除。M和N.在三次手术切除后2个月随访的轴位钆剂(Gd)增强T1加权MR图像。

图2所示。伽玛刀放射外科治疗计划。肿瘤治疗时的边缘剂量为10Gy(50%isodose等剂量线)。
治疗过程总结
2004年5月,采取右侧乙状窦后入路切除肿瘤。术中肿瘤质地坚实(solid),血管相对丰富,易出血,部分切除肿瘤(图1A-B),于2005年8月行伽玛刀放射外科治疗(GKS)(图2)以控制当时的残留肿留。2007年5月转我院行二次手术切除,因蛛网膜边缘不清,与面听神经和后组颅神经粘连严重,残留部分肿瘤囊壁(图1C-D)。病人每 6个月定期随访脑部MRI(图1E-I),最初的残留肿瘤的大小是稳定的。2013年11月,常规随访MRI显示肿瘤开始生长(图1J)。2014年4月出现进行性头痛、眩晕、和恶心,MRI显示肿瘤肿块增大。2014年6月(图1K-L)进行次全肿瘤切除,术中发现显示,肿瘤有两个部分,也就是说,有一部分是软的且相对容易切除,另一部分有弹性伴有纤维组织,蛛网膜边界不清楚,与面听神经和后组颅神经严重粘连。本病例的二次及三次手术均由同一位神经外科医生完成。
以前的一些病例报告说,伽玛刀放射外科治疗后有一个较短的恶变潜伏期。这些病例,可能在接受伽玛刀放射外科治疗前就有恶性成分存在。我们只找到2篇报道前庭神经鞘瘤自发性恶性变(spontaneous malignant transformation VS)的文献(表1),但在McLean等报道的一例病例中,最初切除的病理显示为前庭神经鞘瘤,但肿瘤的一小部分有恶性退化(malignant degeneration)的迹象,且潜伏期相对较短。我们假设该患者也有可能是原发性恶性前庭神经,这表明自然原因引起的前庭神经鞘瘤自发性恶性变(spontaneous malignant transformation as a natural caused )是较其少见的。存在潜伏期至少表明放射治疗在控制肿瘤方面是合适的,除了大的和有症状的良性肿瘤会有高的并发症发生率。本例的潜伏期是122 月,这么长时间静止时间较有可能是良性的行为。
辐射诱发恶性肿瘤的机制尚不清楚。辐射暴露后,有两种可能的结果。一种是确定性效应(deterministic effect),它有一个剂量阈值和与剂量相关的效应的严重程度。另一种可能的结果叫做随机效应(stochastic effect),也就是致癌作用(carcinogenesis),遗传效应(hereditary effect )就是这一类型的一个例子。一种前沿的适形放射技术,如伽玛刀放射外科(GKS),可以向肿瘤提供高剂量的辐射,而正常组织受照低剂量。这可能只会减少确定性效应,但随机性效应仍然是未知的。由伽玛刀放射外科(GKS)引起的继发性肿瘤的发生率较低,但在伽玛刀放射外科(GKS)期间给予单次高剂量照射倾向于导致细胞毒性(cytotoxicity )而非致突变性(mutagenicity)。这也许可以解释为什么前庭神经鞘瘤(VS),传统上使用低剂量治疗与较高的继发性肿瘤的发生率有关。
以前的文献显示,全部组的中位生存期 < 12个月。这表明,与其他病因所致恶性周围神经鞘瘤(MPNST)或继发性肿瘤相比,放射治疗后的恶性变肿瘤可能具有更强的进袭性(aggressive)。预后差,生存期相对较短,使与放射外科治疗相关的恶性变后的治疗处理面临很大的挑战。外科手术切除、放射外科手术和化疗等多种联合治疗已被用于控制恶性前庭神经肿瘤。Chen等提出切除颅内恶性周围神经鞘瘤(MPNST),包括显示存在肿瘤侵袭和颅神经功能失调的证据的周围组织,如肌肉、脂肪、硬脑膜和骨。只有当颅神经(CN)被压迫而不被肿瘤侵袭时,才应考虑保留颅神经(CN)。如果肿瘤残留在脑干、主要血管或其他重要结构上,则应余留下肿瘤。Husseini等指出,放射治疗后完全切除前庭神经鞘瘤(VS)更为困难,且面神经预后相对较差,几乎不可能保留听力。随着得到更多的数据,关于延长生存期的较合适治疗的讨论将继续发展。
许多已发表的研究结果表明,伽玛刀放射外科(GKS)是一种合适的、无创的治疗前庭神经鞘瘤(VS)的方法,是对小型肿瘤肿瘤控制率较令人满意,但在没有明确的肿瘤生长证据的情况下,放射治疗不应被认为是前庭神经鞘瘤的一种较优化的治疗方法。Hasegawa,等解释说,伽玛刀放射外科(GKS)是一个超过10 年的顺利合适的治疗前庭神经鞘瘤的方法。是年轻的患者和神经纤维瘤病2型(NF2)患者,应了解其并发症和失败的风险。
因为数目少,且局限于单一的病例报道,相当多单位情况下随访< 10 年,与放射外科治疗相关的恶变的问题很难回答。前庭神经鞘瘤放射外科治疗后发生恶变的风险较低,但有潜在的严重风险,因此我们建议患者在接受伽玛刀放射外科(GKS)治疗前应了解发生这种并发症的可能性。由于对治疗的长期效果尚未完全了解,放射外科治疗应谨慎使用,特别是对年轻的个体。放射线诱发的恶性肿瘤发生在足够的潜伏期之后,因此强烈建议全部接受放射外科治疗的病例进行长期随访。
听神经瘤手术策略
听神经瘤治疗方法根据主要患者临床症状、听神经瘤生长情况而定,大致包括显微手术切除、立体定向放射治疗以及随访观察。
当患者临床症状明显,肿瘤较大或生长迅速时,优选手术切除,只有手术才能及时制止肿瘤占位引起的神经功能缺损,并争取颅神经功能的恢复。一次手术对效果至关重要,听神经瘤患者只要条件许可都建议优选手术切除,如今显微技术的发展,开颅手术已经越来越微创化,创口小,术后,很多并入术后当天就可以如常下地行走。
传统听神经瘤手术主要是以切除肿瘤,提高患者生存率为准则,但有时可能是以牺牲听力和面神经功能为代价而进行的。随着技术的发展和相关手术设备突飞猛进的进步,听神经瘤手术的成功衡量标准已变成了“尽可能全切”、“不面瘫”、“保留听力”三要素并存。这些都对神经外科医生都提出了较大的挑战。
功能保留逐渐成为治疗的首要目标,在听神经瘤手术中,正常的面神经因肿瘤挤压、推挤后形态及位置发生改变,面神经保留率不高。而选择高超技术手法的手术专家,采用术中全程监测可明确面听神经与肿瘤的相对位置,从而明确肿瘤切除的边界在哪里,或可争取顺利、无损伤且尽可能地完全切除。听神经瘤手术难度较大,开展听神经瘤手术的医疗机构或科室建议达到相应资质和技术水平,并配备术中电生理监测、术中神经导航等必要设备。
INC世界神经外科顾问团是由国际各发达国家神经外科宗师联合组成的教授集团,囊括了神经外科各细分领域的国际教授。INC一直致力于中外神经外科技术的交流、合作、促进和提高,同时针对国内追求更高质量手术、更佳预后的疑难神经外科疾病患者,提供国际前沿咨询意见及手术治疗。对于听神经瘤手术,INC有国际颅底肿瘤手术教授、世界神经外科联合会WFNS教育委员会主席德国Helmut Bertalanffy(巴特朗菲)教授、当今世界神经外科顾问团WFNS颅底手术委员会主席Sebastien Froelich教授、神经外科领域较高难度的中央颅底手术入路Dolenc入路的提出者Vinko Dolenc教授、神经外科领域高难度手术入路Kawase入路的创始提出者Takeshi Kawase教授等较为擅长。
参考文献:
Malignant transformation of a vestibular schwannoma to malignant peripheral nerve sheath tumor 10 years after Gamma Knife Surgery: Case report. Interdisciplinary Neurosurgery . 2019




