脑干胶质瘤可以手术治疗,由于脑干不同部位的功能特点和部分肿瘤呈现弥散型改变,手术治疗及其结果尚存争议。
脑干胶质瘤分型和诊断
脑干胶质瘤的分型对手术治疗有意义。从1985年Epstein到2000年Choux先后有7~8种分类标准l4J。早期根据肿瘤的形态学观察和CT扫描特点,如肿瘤是局限性还是弥散性,是囊性还是实体性,向背外侧生长还是向脑干内浸润性生长进行分类;后来根据肿瘤所在的解剖学部位、病理学特征、MRI特点等进行分类。由于成人和儿童脑干胶质瘤生物学特性和预后不同,产生不同的分类方法,成人分为:弥散内生型、局限型和延颈髓型;儿童分为:弥散内生型、局限型、背侧外生型和神经纤维瘤病I型伴发脑干胶质瘤。这是目前常用的分型方法,分类的目的是为了选择适宜的治疗方案。目前MRI检查是诊断脑干胶质瘤的可靠方法。MRI序列检查如波谱分析(MRS)、功能Mill(fMRI)、PWI、Blood—fMRI、DWI、DTI等相关技术的应用,可以了解脑干的功能状态,确立肿瘤和传导束的关系,提高诊断的准确率。MRS是目前在活体内检测物质代谢及生化物质含量的惟一无创性检查技术,对诊断脑干胶质瘤及其鉴别诊断有价值。通过检测Cho、Cr、NAA等代谢产物及其比值,达到鉴别肿瘤和其他病变的能力,成为诊断脑干肿瘤的重要工具,也使影像诊断学逐步深入到细胞生化代谢水平。
脑干胶质瘤手术干预
脑干肿瘤的手术更具有挑战性。手术适应证选择重要。从理论上讲,只要不是弥散内生型,且MRI没有强化改变的,都可以手术治疗。但是为什么很多确诊的病人,却不能手术治疗,更多是从脑干功能角度考虑,如肿瘤位于脑干中心且没有突入到脑干表面、肿瘤完全在腹侧等,成为手术相对禁忌证。关于手术切除的范围,原则上旨在保留神经功能的前提下尽量全切,但是由于脑干生理解剖学特点,实际操作可能会出现问题。
NCCN神经系统肿瘤治疗指南中,在手术切除肿瘤方面进行了调整,将较大切除改成较大顺利切除。其含义是强调对神经功能的较大保护。目前显微神经外科辅助设备和技术的发展,好转了手术质量,提高了手术的顺利性。如MRI指导下神经导航技术(MRI—GuidedNeuronavigation)、术中MRI技术(IntraoperativeMRI)及术中超声定位技术的应用使手术进入脑干内更加精确;术中应用荧光造影术(Fluoreseenee—GuidedSurgery)可以在手术显微镜下确定肿瘤的边缘,达到较大范围的肿瘤切除;术中电生理监测和功能MRI应用,可以了解脑干、神经核团及神经传导束的功能,避免不必要的神经功能损伤。
对于局限型,手术是主要治疗手段,术后效果较好。手术切除程度会影响预后生存期。肿瘤位于脑干不同解剖部位,神经功能的关注点不同,中脑肿瘤手术可能更关注意识状态,同时也需注意肢体运动和眼球活动,当中脑顶盖部肿瘤合并有脑积水,术前或术后需要脑室一腹腔分流或内镜三脑室底造瘘术。桥脑肿瘤多为侵袭性生长,对于MRI有强化效应的可以考虑手术,但肿瘤全切率较低,这部位神经核团较多,会引起如面瘫、复视等神经功能障碍,所以桥脑手术更应注意神经核团的功能。延髓肿瘤手术应该关注吞咽和呼吸功能,也不能忽视顽固性嗝逆。
脑干胶质瘤手术入路
手术入路的选择首先考虑合适到达肿瘤的部位,根据肿瘤的发生部位和发展情况,选择不同的手术入路,如颞枕入路、Poppen入路、枕下后正中入路等。但是脑干手术入路较重要的是选择进入脑干点,也称为脑干顺利进入区。术后神经功能改变与术中选择脑干切开的部位有直接关系,如何选择脑干进入点,可以借助神经电生理刺激器,确定脑干表面神经核团较少的区域进入,有条件的可以使用显微神经外科辅助设备和技术,如MRI辅助导航下纤维传导束融合技术,可以清晰分辨出肿瘤和脑干传导束之间的关系,选择顺利进入区。
脑干进入点选择的基本原则
脑干进入点选择的基本原则是:在神经核团较少的区域;避开影响肢体运动功能传导束;如果需通过神经核团,应选择可以耐受的神经功能损伤,如涉及动眼神经核和滑车神经核时应该保护动眼神经核;不要涉及更多的核团和传导束,能够从单一核团进入的,不干扰其他核团和传导束;对肿瘤突破脑干表面,也要应用神经电生理监测仪探测表面,选择没有核团、组织较薄弱处进入。肿瘤切除过程中要实时监测核团和脑干功能,手术过程中需要与麻醉师和神经电生理人员密切配合,当波形有变化时,注意分析是技术操作问题还是肿瘤本身问题,评估手术对核团和纤维的损害程度。可以参照Paul术中肌电反应分级标准,如果手术中出现Ⅲ、Ⅳ级等毁损性肌电活动时或肿瘤切除后2h内没有波形复现,即使出现较小波形但是潜伏时明显延长,提示术后神经功能可能为不可逆性损伤。术中监测生命体征变化,特别是心率和血压波动有意义。手术操作时要轻柔,尽量减少对脑干的持续性牵拉,注意双极电凝输出功率的选择,进入脑干内操作应选择较小功率。显微吸引器及CUSA的应用,都是减少神经功能损伤必不可少的。对于脑干胶质瘤立体定向活检问题,争议的焦点集中在没有活检结果,是否可以放化疗。特别是有些肿瘤影像学特点不典型,易与炎性反应、脱髓鞘病变及肿瘤放射性坏死相混淆。
目前MRS分析等特征性检查可以避免活检。由于活检有其局限性,不能作为主要诊断依据,目前不主张进行常规活检。因为活检不能起到治疗作用,还可能出现下列情况:(1)损伤脑神经和锥体束,使病情加重;(2)肿瘤的异质性使取到的组织不能代表肿瘤病理性质。
脑干-顶盖胶质瘤患者赴德手术治疗之路
“八月的时候生病了,原以为人生会戛然而止,抱着较虔诚较奢侈的期待,也做了较坏的打算上了手术台,最后的结果是翻盘成功,向阳而生。感谢伟大的巴特朗菲教授,感谢INC的工作人员,让我的生命得以延续......”
——INC患者周老师
2020年8月,核磁共振检查结果显示中脑背侧占位,病变大小约1cm,考虑为低级别胶质瘤可能大。而且医生还告诉他,脑干的位置“险要”,是人体的生命中枢,这个病变不止会造成头部和眼部的疼痛,随着肿瘤的生长还会压迫到更多脑部组织,甚至造成肢体无力,无法站立行走甚至控制呼吸、神志不清等,但在此处手术的风险太高,术中稍有差池都可能直接造成高位瘫痪,建议周老师一家谨慎考虑后续治疗方案。于是选择直接远程咨询INC德国巴特朗菲教授,并与妻子做出决定“如果巴教授愿意为我做手术、还能不致残,那我们无论如何都要去德国治疗”。
德国巴教授肯定的回复,远赴德国。
术者:德国INI Bertalanffy教授及其手术团队
手术地点:德国汉诺威国际神经科学中心INI
诊断:左侧脑干(中脑顶盖区)的低级别胶质瘤
手术结果:半坐位,经显微镜下全切肿瘤,术中全程电生理监测,手术顺利无神经缺损。
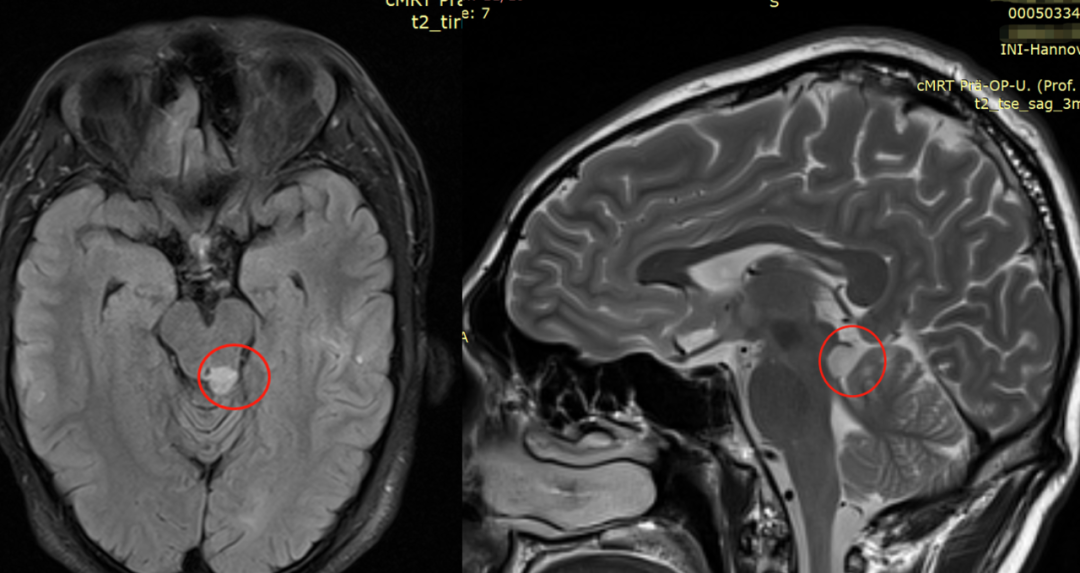
术前影像
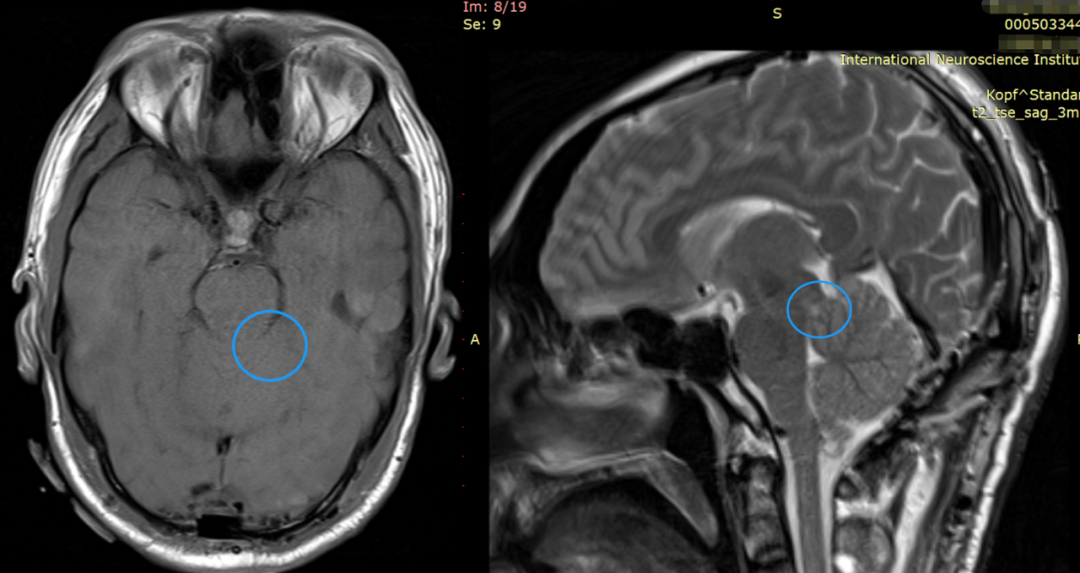
术后影像
术后1天迁出ICU,回到普通病房,周先生为巴教授的医术竖起大拇指
术后2天,周先生在医护人员的帮助下下床行走

术后5天,周先生出院并与教授合影
脑干胶质瘤不同的类型,手术治疗效果不一。单纯手术治疗不能好转病人的生存期,需要综合治疗。儿童型绝大部分不能手术治疗,即使有手术适应证,术后神经功能障碍较多,围手术期治疗和护理更为复杂。
脑干胶质瘤治疗目前仍然存在许多困惑,手术虽不是惟一的治疗方法,但是综合治疗的基础。脑干肿瘤多为恶性,尽管手术、放疗和化疗,肿瘤依旧复发。虽然现在手术技术改进,放疗设备前沿和不断更新的化疗新药的出现,对于复发肿瘤是否可以再次手术,再次手术前要评估全身状态特别是KPS评分和脑神经受损的数目重要,根据评估结果决定是否再次干预。北京天坛医院脑干胶质瘤病例中再次手术不到3%。
脑干肿瘤的研究和治疗是一项复杂的工作,应该作为一个系统工程来考虑。建立脑干胶质瘤的规范化治疗还需要多学科的参与。




