丘脑海绵状血管瘤能治好吗?丘脑位于脑干侧脑室的中心。由于它是由重要的神经血管结构围绕而成的,因此手术方法具有挑战性。丘脑与基底节、内囊、中脑、丘脑静脉和大脑内静脉密切相关。那么,丘脑海绵状血管瘤能治好吗?丘脑海绵状血管瘤有哪些手术策略呢?

丘脑和基底节的海绵状血管瘤(CMs)是相对少见的病变,可导致发育性泌尿系统缺陷。由于这些病变的少见性,对其自然病史、理想治疗、手术方法、并发症和结果的描述仅限于病例报告和小系列。丘脑CMs的初始手术入路和切除与产生新的或恶化的神经功能缺损的风险直接相关。手术的益处需与这些风险权衡。
最近,基于两点法的颅底入路被描述为脑干CMs。
相比之下,基底节和丘脑的CMs很少受到关注。一些神经外科医生仍然认为这些病变不能手术,或者需要更多的解放来选择最佳的手术方法。对深部血管病变的广泛经验帮助我们重新定义了丘脑CM的传统方法。
在丘脑内。我们发现丘脑的每个部分都有一个特定且不同的手术方法和通道。在本文中,我们根据解剖和该区域较合适的手术入路将丘脑分为6个不同的区域(图1)。该分类已应用于46例丘脑CMs患者,以系统化我们对这些病变的手术方法,并展示我们的手术结果和患者的长期结果。
手术治疗研究:丘脑海绵状血管瘤有哪些手术策略呢
6个丘脑解剖区域区域1(前-后)
区域1包含丘脑的前下核和前腹核。该区域的上边缘和内侧边缘由区域2形成,后缘由区域3形成。前外侧边缘由内囊的膝部和后边缘形成。下缘由直接位于颈内动脉分叉上方的前穿孔物质形成(图1和图2)。
区域2(中间)
区域2包含丘脑的上前核、内侧核和中央内侧核的内侧部分。它由上部(丘脑)和下部(下丘脑)组成,分别伸入侧脑室和三脑室。这两部分由海波丘脑沟分开。上孔前方被位于Monro孔后面的丘脑纹状体静脉限制;其内侧边缘由脉络膜上静脉、脉络丛和Monro口形成;其外侧边缘由髓内板和区域3组成。区域2的下孔伸入并形成三脑室的侧壁。这部分可以在穹窿之间或通过Monro孔或telachoroidea孔进入。丘脑髓质纹沿丘脑内侧缘从孟罗孔延伸至缰连合。中间块连接丘脑的相对表面,其存在是可变的。穹窿柱在Monro孔下方的三脑室侧壁形成优势,并向下沉入表面下方(图1和3)
区域3(横向)
区域3包含外侧核(即腹外侧、腹外侧、腹后、背外侧和后外侧核)。内侧受内髓板和区域2的限制,外侧受内囊的膝和后肢的限制(图1和4)。
丘脑后部(枕)与3个不同的腔室密切相关,使其手术方法更具挑战性。因此,我们将丘脑枕空间分为3个不同区域(区域4、5和6)。


患者群体
在5年的时间里,由同一神经外科医生在亚利桑那州凤凰城巴罗神经生物学研究所对310例幕前CMs患者进行了手术治疗,并记录在前瞻性数据库中。在数据库中搜索丘脑CMs患者,确定46名患者并纳入本研究。有24名女性(52%)和22名男性(48%),年龄为36岁(7-64岁)(表1)。在46例患者中,27例(59%)出现出血,其中21例(78%)为实质内出血,6例(22%)为脑室内出血。10名患者(22%)表现为对侧肢体麻木和或感觉异常。三名患者(6%)表现为与动眼神经、滑车神经或展神经的颅神经衰弱有关的复视。2例(4%)表现为对侧神经麻痹。19名患者(41%)出现头痛。5例脑室出血患者也表现为脑积水,需要脑室腹腔分流术。12名患者(26%)曾在其他中心接受过手术,由于切除不全而被咨询给我们。对于那些出现出血的患者,在急性发作后立即进行了手术。
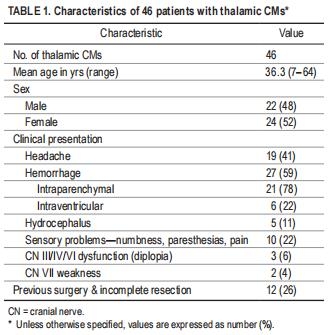
CMs的特点
我们系统地回顾了患者的CT和MRI研究、手术报告。术中视频和外科医生注释,根据6个不同位置对丘脑CMs进行分类。占据一个以上区域的大型CMs根据病变中心的位置进行分类。一些CMs伸入脑室,侧向伸入内囊,或向下伸入中脑或脑梗。26个CMs(57%)位于左侧。平均CM直径为21.23mm(范围5-45mm)。丘脑内(无软脑膜表面或可触及表面)的无症状小CMS(5mm)通过随访影像学保守处理。


结果评估
使用改良Rankin量表(mRS)评估神经结果。神经病学评估由神经外科住院医师和脑血管研究员在高级神经外科医师的监督下进行,包括术前、术后和治疗后一年。通过常规临床访视和KOR电话访谈获得随访信息。良好结果定义为最终mRS评分0-2,不良结果定义为最后mRS评分大于2。术后24小时内进行MRI检查,以评估残余畸形,并每年评估复发。根据CM中心的位置分配这些大型或巨型CM的位置(表2)。
治疗策略和方法
同侧前房间隔隔隔离性经舌(包括经室、经口和经脉络膜变异);对侧前半球经舌入路;后半球间经舌入路(PT):顶枕经腹入路;和枕下小脑上幕下入路AnOZ。区域1(5cm,11%)采用开颅术并经外侧颈动脉额下解剖。AIT方法用于区域2(9厘米,20%)。在2区的ALTA方法中,位于丘脑内侧上部的2个CMs(使用了IT跨室变异,AlT跨孔3个CMs,6%)和AIT跨室dal(4个CMs,9%)变异用于访问三脑室外侧壁的CMs。ACT方法是较常见的程序(17个CMs,37%),用于区域3的CMs。
根据CM中心的位置分配这些大型或巨型CM的位置(表2)。
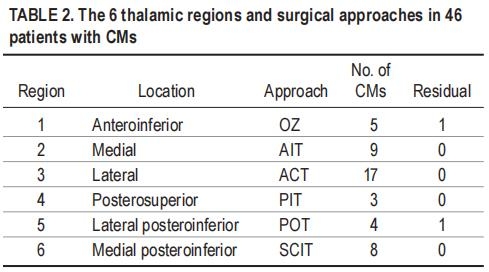
手术结果
全部患者在术后24-48小时内立即进行了MRI检查。除2例患者外,患者的丘脑CMS完全切除。这2名患者有较大(25mm)的CMs,术后MRI上观察到意外的残余畸形。这2个较大的CMs位于外侧后下(区域5)和前后丘脑(区域1)。两位患者均接受了二期手术以完成切除;获得大体全切除术(GTR)
在二次手术的两名患者中,没有与手术相关的主要并发症。发生4例小并发症,包括1例保守治疗的小硬膜外血肿、1例需要长期抗生素的伤口感染和2例需要手术修复的假性脑膜膨出。
患者预后
术后对全部患者进行至少6个月的临床和影像学随访。平均随访期为1.7年(6个月-9年)。没有死亡。10名患者(22%)术后暂时出现术前症状。术前对侧偏瘫和/或再狭窄的患者有10例症状恶化;6例在术后6-8周内复发。全部患者术后均无偏瘫。两名动眼神经功能障碍患者的症状也在恶化,8周后恢复到基线水平。此外,1名面部无力的患者(House-BrackmannII级)暂时恶化(HouseBrackmannV级)。在研究结束时,40名患者(87%)有良好或良好的结果(mRS分数为0-2),6名患者(13%)有较差的结果(mRS分数为3-4)。相对于他们的操作条件。42例(91%)未改变或好转,4例(9%)更差。术后神经系统疾病在全部区域和入路分布均匀。没有一种单一区域或方法具有较高的术后短暂神经功能缺损发生率(表3)。
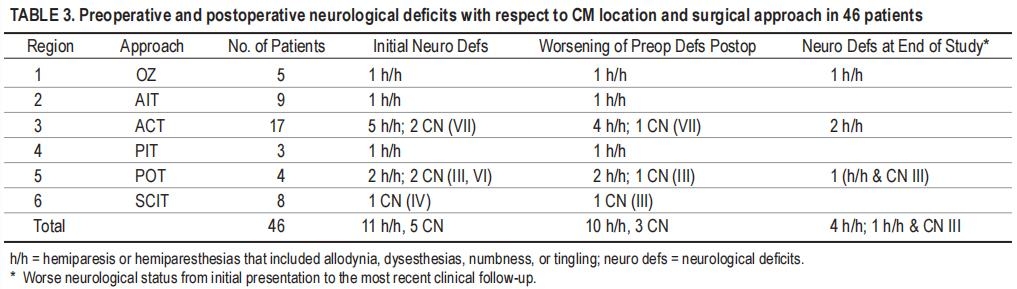
讨论
我们对丘脑CMs的经验表明,充分暴露病变和显微手术切除可以获得令人满意的结果。在本系列中,除2例(4%)需要通过相同方法进行二阶段手术外,全部病变均在一次手术中完全切除。12例患者(26%)出现短暂的新缺陷和术前神经功能障碍恶化。这些暂时性缺陷在手术后6-8周内得到解决。有4名患者(9%)因手术后恶化的CMB出血而出现神经功能缺损,但在最后一次临床随访中没有恢复(表3)。平均1.7年后,42名患者(91%)的症状没有改变或好转。这些结果证明了一种针对丘脑CMs的ag-g手术方法的合理性。
在本报告中,我们描述了46例丘脑CMs的手术经验。到目前为止,没有丘脑CMs的解剖学分类。李等人报告了一系列27个丘脑CMs,并提到了不同的方法。斯坦福研究小组最近更新了他们的一系列基底神经节、丘脑和脑干CMs(包括16个丘脑病变);然而,区别并不是基于位置。我们根据解剖位置和丘脑内每个特定位置的相应手术方法提出了丘脑分类。这些方法之前已经被美国或其他经验丰富的血管神经外科医生描述过。
区域1(前后)
丘脑前内侧的病变位于尾状核、壳核、苍白球附近。内囊和前丘脑。该区域很难通过经皮质、经外侧裂跨沟和经胼胝体跨室等途径到达,因为它们分别需要大量的额叶、岛叶皮质和健康的丘脑。在当前系列中,5个CMs(11%)位于区域。这些CMs都是通过经侧裂颈动脉上额叶下解剖通过臭氧颅切术接近的。该路径暴露颈动脉上三角,然后将三角穿过额叶,从下方进入病变。.开颅手术至关重要,因为进入三角的手术轨迹是在与视神经走行平行的眶上线中额叶的上方和后方。一旦西尔维安问题被广泛打开,就会定义和选择一个合适的轨迹,以较大限度地减少大脑越界,避免出现失误。这些穿支是分开的,不受手术走廊的影响。这种方法较关键的缺陷是可能损害穿通动脉,导致随后的内囊卒中。
我们系列中的一名患者发生了小范围内帽状沟卒中,可能是因为穿通动脉受伤。该患者有短暂的偏瘫恶化,并在术后6周内恢复。有学者发表了他们对5名患者的治疗经验,这些患者在前-后基底节患有CMs,并接受了颈动脉上-额下入路;其中2例术后出现短暂的神经功能缺损。小心处理射孔血管至关重要。解剖三角内这些穿支的蛛网膜下段以增加其活动度。入口点可以在A或M侧;无论选择哪个入口点,都需移动和保护穿孔器。这种方法的一个潜在限制是难以到达CM的上较,这位于曝光盲点。从神经学角度来看,这个部位是较敏感的部位,因为病变较靠近内囊。我们的一名患者有残留病变,需要在二天通过相同的方法进行二期手术。二次手术后,患者没有任何缺陷,2天后出院回家。在这种情况下,OZ开颅术和术中导航有助于解决这一局限性。
区域2(中间)
内侧丘脑是二常见的位置。全部病例均采用AIT方法。其中两例位于该区域的上部,侧脑室内。在进行胼胝体切开术后,确定CMS周围的含铁血黄素环,并切除病变。其他7个部位位于二区下部,位于三脑室内,需要进一步解剖进入三脑室。这些病变有2个主要手术通道:经口(3例)和经脉络膜(4例)。经口走廊使通道更靠前;Monro孔向脉络膜裂开放。经脉络膜入路是通过脉络丛的侧面进行的,这与以前的描述不同。我们更喜欢在脉络丛外侧切开,因为它可以作为穹窿和器械之间的缓冲。对于AlT入路,大多数神经外科医生仍然让患者仰卧或坐姿,头部和颈部处于中间位置,矢状中线垂直。我们更喜欢横向旋转颈部,以水平定位中线。水平位置对外科医生的手更容易,使他们能够在同一平面上工作。这一立场要求就偏侧性作出决定。
区域3(横向)
外侧丘脑是目前为止较常见的位置。该区域的全部病变均通过ANCT方法切除。与其他方法相比,这种方法有许多重要的优点。它避免了经皮质切开,重力收缩大脑半球以打开大脑间裂。开颅和半球间入路与病变对侧,经心室入路与病灶同侧。与区域2(内侧)相反,区域3(外侧)的病变需要收缩半球,这会损伤副镰刀回和扣带回。ACT方法提供了一个更好的角度,可以增加横向暴露,并较大限度地减少主题半球所需的收缩。此外,重力将上部病变从内侧拉入外科医生的视野。该方法适用于全部3区CMs(17CMs,37%),且不存在与该过程相关的神经并发症。在全部情况下均获得技术法规。
区域4(后上)
区域4周围区域包含关键的解剖结构,包括内侧枕叶、后胼胝体、丘脑、大脑后动脉和Galen静脉。后内侧丘脑的手术入路包括SCT或经幕入路、PIT入路、枕经幕入路和枕双经幕/假电影入路。我们认为PIT入路为丘脑后上区提供了一条优越的通路;它提供了比幕下方法更广泛的曝光,因为后者受到两侧幕陡倾角的限制。在4区的3例丘脑CMs患者中均采用PIT法。在这种方法中,患者被置于外侧,侧枕叶处于依赖位置,使用重力作为回缩,类似于AIT方法。潜在的神经系统并发症是新的或恶化的视野缺损,这种情况在这种方法中常见。有学者报告了他们使用这种方法的经验,并在一半患者中观察到了这种并发症。当使用侧卧位时,这种并发症不那么严重,并且通常是可逆的。胼胝体及其脾的分裂可引起断开综合征。我们的任何患者均未出现这些并发症。
区域5(外侧后下)
丘脑的5区伸入侧脑室心房的前壁。经顶上叶的POT-ap入路是通向脑室此区域的优选途径。皮质切口应足够高以避免视觉辐射,位置应足够高,以避免语言区域。其他12条心房入路包括跨颞入路和跨半球顶枕楔前区入路。然而,前者患双侧象限失语和失语的风险很高,而后者则需要更宽的大脑回缩和更窄的手术通道和入路角度。全部CMin区域5的患者均采用POT方法治疗。一名患者术后再次出现失语,几周后部分缓解。没有与手术相关的手术并发症。
区域6(内侧后下)
SCIT方法用于区域6中的全部病变。描述了SCIT入路的三种不同变体,它们包括中间变异、旁正中变异和侧向变异。我们更喜欢ParamedianSCIT变异;由于小脑表面从内侧向外侧向下倾斜,因此需要较少的回缩。患者可以仰卧,头旋转,也可以坐在公园长椅上,病变侧朝上。打开硬脑膜后,小脑表面轻轻回缩,露出小脑裂,周围水池,以及更进一步的中间四边形水池。桥静脉是可以遇到的,尽管这种方法比正中SCIT更不常见。需注意识别和预防加伦静脉、大脑内侧静脉、罗森塔尔基底静脉和脉络膜后动脉中脑支的损伤。滑车神经的识别和活动较低(滑车上入路)。上丘暴露在中线,松果体下方。
在这些结构的外侧,内侧下枕变得明显。根据后切迹的宽度,后海马旁回向中间延伸至十个环自由边缘的后部上方。该切迹可能部分遮挡了尺骨的上部,因此需打开天幕。1例患者需要切除小脑幕以更好地显示枕叶和CM。该组患者存在非手术并发症或新的长期性神经功能缺损。丘脑的这一区域对手术操作的耐受性。两名患者先前存在的动眼神经无力和对侧偏瘫恶化,并在术后6-8周得到缓解。
结论:丘脑海绵状血管瘤能治好吗?
丘脑海绵状血管瘤是相对少见的病变,由于其位置深在,并且毗邻重要的解剖结构,手术切除挑战较大、术后并发症风险很高,有可能导致毁灭性的神经功能缺损。但丘脑海绵状血管瘤与丘脑胶质瘤不同,其是良性病变,并且与正常丘脑、中脑有相对的界限。尽管手术难度很大,如选择适合的手术入路并结合娴熟的显微神经外科手术技巧是可以全切肿瘤并获得良好疗效的。而且早期手术可提供良好的临床效果,并消除未来出血的风险。数十年来,随着神经影像学、显微外科手术和术中辅助技术的进步,手术切除程度正在逐渐提高。除了技术设备因素,丘脑海绵状血管瘤的手术切除程度还跟神经外科医生的经验相关,灵活的手术策略、熟练的手术技巧、耐心细致的手术操作,以及对于多种手术入路方式的熟练掌握,都是手术全切的关键。
参考文献:The 6 thalamic regions: surgical approaches to thalamiccavernous malformations, operative results, and clinicaloutcomes




