脑干肿瘤占成人全部颅内肿瘤的1.5%至2.5%,而占儿童肿瘤的10%至20%。这些肿瘤在成人中不常见,因此,更多的临床研究已经在患有脑干肿瘤的儿童中进行,特别是脑干胶质瘤,因为他们在这类患者群体中更常见。患有脑干胶质瘤的成人的中位生存期为5到7年,比儿童要长。以往,脑干肿瘤被当作一组均匀的病灶进行放射治疗,而放射治疗通常没有组织病理学的证实。这些肿瘤的手术很少见,通常仅限于活检,摘除囊性病变,以及为梗阻性脑积水放置分流管。然而,Pool在1968年记录了一例位于脑导水管区域的脑干肿瘤的手术切除。这个报告的病例带来了对治疗脑干病变的进一步研究和外科技术的发展。
脑干肿瘤的分类
脑干肿瘤较早的分类方案是基于CT图像和手术观察。后来的方案依赖于磁共振成像,这使得更好的神经解剖学细节得以获得。最近开发的分类系统依赖于CT和MRI。全部这些方法将肿瘤分为局灶性或弥漫性生长模式,而更复杂的分类进一步将肿瘤细分为脑干内位置、有无外生性成分、有无脑积水或出血。更复杂的方案是为了评估肿瘤的行为并指导手术和非手术治疗。一般来说,与弥漫性生长模式的肿瘤相比,局灶性生长模式的肿瘤被认为更适合手术切除。
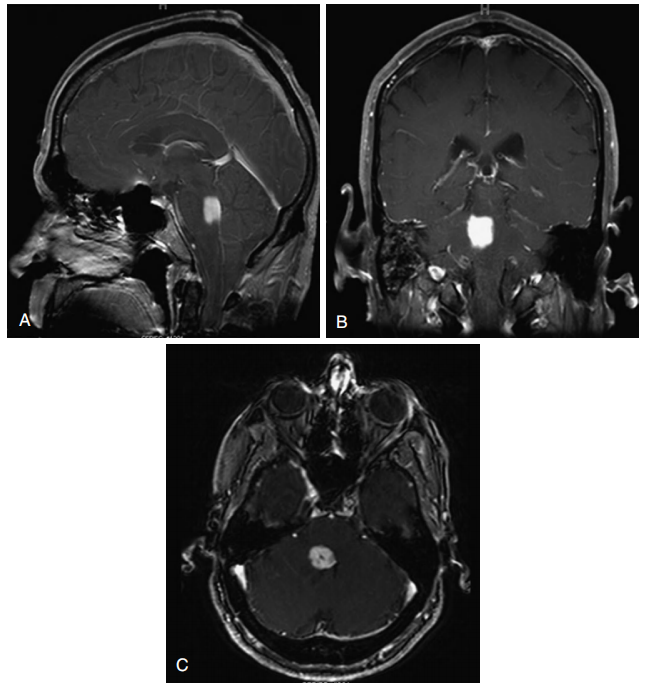
图13-1局灶性桥脑胶质瘤。A,矢状面MRI显示脑桥强化肿块。B,造影后冠状核磁共振成像。C,对比后轴向MRI。
局灶性肿瘤
局灶性肿瘤是脑干固有的,可以是囊性或实性的(图13-1)。它们通常与水肿无关,对比度增强可能是可变的。这些肿瘤中的大多数是低级别胶质瘤,但一些恶性肿瘤,如国际卫生组织(WHO)的Ⅳ级星形细胞瘤,可能会模仿局灶性肿瘤,即假性局灶性肿瘤。在假性局灶性肿瘤中,MRI和CT表现为局灶性增强,与瘤周区的正常信号特征相似。
此外,大多数颈髓神经胶质瘤是低级别的非浸润性肿瘤,其生长通常受到皮质脊髓束和内侧丘系白质的限制。
外生型肿瘤
具有外生生长成分的局灶性脑干肿瘤通常是低级别的,界限清楚(图13-2)。它们通常是生长到四脑室的背侧外生肿瘤或外生生长到大池和四脑室的颈髓肿瘤。值得一提的是,除了局灶性肿瘤外,一些弥漫性肿瘤可能引起四脑室、桥小脑角、前脑池和其他脑池的膨出。
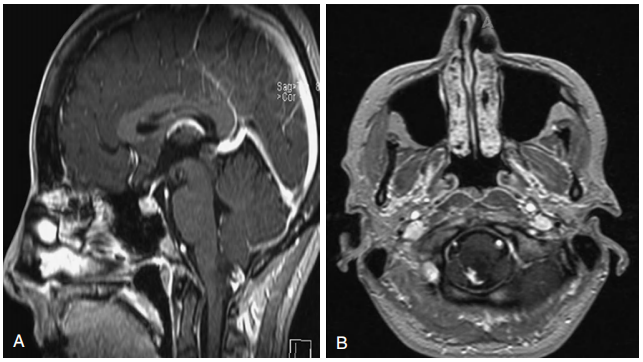
图13-2背侧外生性颈髓胶质瘤。A、 矢状位磁共振造影后显示一低信号病灶,在后尾部有强化。
B、轴位磁共振造影后。
弥漫性肿瘤
弥漫性脑干肿瘤在T1加权和T2加权MR图像上分别表现为低至等信号和高信号(图13-4)。对比剂注射后有不同程度的增强,这些肿瘤的对比剂增强可能提示恶性变性。此外,肿瘤边界无法在MRI上描绘,脑干通常增大和变形。
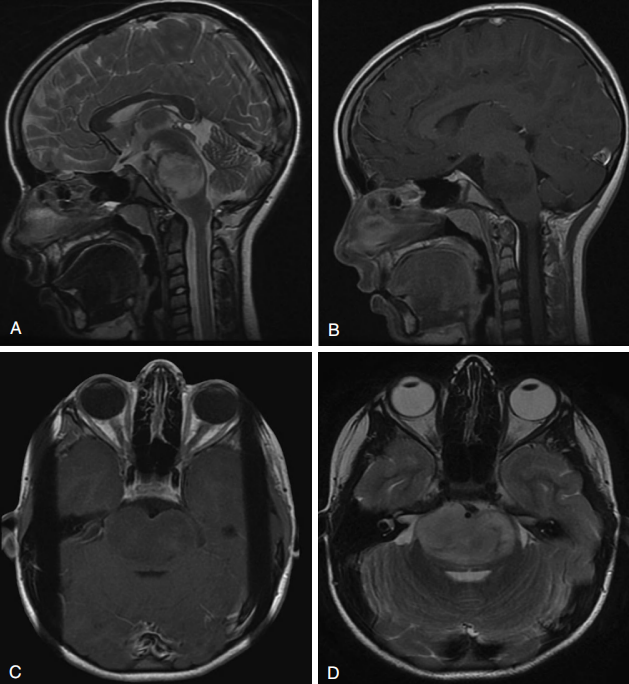
图13-4弥漫性桥脑胶质瘤。A、 T2加权矢状位MRI显示桥脑高信号肿块。
B、 对比后矢状位T1加权MRI显示低信号、无强化的脑桥肿块。
C、 低信号,无强化的桥体肿块在轴向T1加权磁共振造影后。D、 T2加权轴位MRI显示桥脑高信号肿块。
手术适应证
一般来说,临床表现和影像学表现与弥漫性胶质瘤一致的患者不会从外科手术中获益,尽管目前正在进行治疗剂在颅内局部给药的实验研究病灶。局灶性脑干肿瘤可以手术切除,这通常是优选的治疗方法。背侧中脑肿瘤,如顶盖胶质瘤,在临床和影像学上多年来被认为是惰性和稳定的,最初可以通过连续成像以非手术方式进行治疗,并且在肿瘤进展的情况下进行手术核磁共振。阻塞性脑积水,如果有的话,可采用内镜下三脑室造瘘术治疗,肿瘤可随后进行连续磁共振成像。
脑干肿瘤如何顺利手术?
术中神经生理监测与标测
脑干复杂的神经解剖结构对神经外科医生在处理这种复杂、小结构的病变时提出了较大的挑战。在脑干内,颅神经核和上升和下降的路径包含在这里。肿瘤可以扭曲脑干的正常解剖结构,如四脑室底部的解剖标志,如面丘和髓纹,使手术更具挑战性。术中神经生理学监测和标测的引入使得手术更顺利,有助于制定手术计划,同时较大限度地降低对关键脑干结构的风险。
脑干听觉、体感和运动诱发电位在手术中被用来监测其相应的通路。这种形式的监测无助于防止重要脑干结构的损伤,因为在手术过程中没有进行功能定位来识别危险区域。
四脑室底功能标测有助于识别脑干颅神经运动核及其与心脏的关系肿瘤颅神经VII,IX,X支配的肌肉的反应,当神经外科医生用手持式单较探头刺激四脑室底部时,可以在手术过程中记录XII。为了防止在刺激过程中对四脑室底部造成损伤,探头为圆形,尺寸约为0.75mm。利用肌电图可以记录眼轮匝肌、口轮匝肌、咽后壁和舌肌的动作电位。应确认肌肉松弛剂不会干扰肌电图记录。此外,脑干受压的程度、病理学和到颅神经运动核的距离对决定阈值强度起着重要作用,血肿的阈值强度可低至0.2ma,而脑干肿瘤通常需要更高的阈值强度,高达2.0mA。在记录肌肉反应后,利用阈值强度允许通过每1 mm移动刺激探针定位细胞核。这一信息为切口提供了一个顺利的位置,并试图在肿瘤切除过程中尽量减少损伤。如果没有检测到肌肉反应,刺激器和/或记录系统可能存在技术问题,或者颅神经运动核可能位于病理的腹侧。如果细胞核位于脑干病理学的腹侧,则需要通过病变反复刺激来检测细胞核。
此外,皮质脊髓束可以在脑脚的水平上进行定位,Kartush手持式刺激器(medtronicxomed,Inc.)通过对特定肌肉的肌电图监测,对中脑进行局部刺激。这种术中方式允许外科医生确定上述路径相对于肿瘤的位置,并顺利地在中脑切开。皮质脊髓束的定位有助于外科医生在病灶周围的解剖和活动中保护皮质脊髓束。
外科手术入路
脑干的大小和手术入路决定了脑干的位置。在制定手术策略时,需考虑脑干及其周围血管的复杂神经解剖结构。磁共振成像是用来定位肿瘤,并计划较理想的路线,肿瘤,将尽可能减少损伤神经血管结构的风险。
对于脑桥背侧、四脑室底、延髓背侧和颈髓后交界处的肿瘤,我们倾向于患者俯卧位的枕下入路。小脑幕下入路可以到达顶盖中线区的肿瘤,我们也对俯卧位的患者进行此手术。后外侧桥、外侧小脑中脚、上外侧髓质和桥小脑角的病变可通过乙状窦后入路进入,远外侧入路提供脑干的前外侧轨迹,用于下外侧桥和前外侧髓质的病变。我们在乙状窦后入路和远外侧入路中都使用park-bench位置。
颞下入路可进入外侧中脑病变。眶颧入路除了外侧中脑外,还提供了到头端脑桥、脚间区和脑桥-头关节的额外通路。对于腹侧桥较低部位的病变,这些入路可结合岩骨前切除术。
外科技术
脑干复杂的神经解剖结构在切除肿瘤时需要仔细的显微外科技术。脑干的小尺寸要求精确的运动和良好的术中判断。一个功能最佳的手术显微镜对脑干内部和周围的手术至关重要。内生性肿瘤需要在脑干表面开一个切口,并需要对解剖学有透彻的了解。虽然许多肿瘤可以在较接近表面的地方进行探查,但需记住,在某些情况下,这可能不是最佳途径。切口通常小于1cm,为切除大肿瘤提供了足够的空间。脑干皮层脊髓束附近的肿瘤可以被定位为一个顺利的切入点。对于经由四脑室底入路的肿瘤,对四脑室底的定位对于切口的放置重要,以避免颅神经核,如VII、IX、X和XII。此外,有些脑干区域可以相对顺利地进入。经四脑室底入路的脑桥背肿瘤可经面丘上方正中沟、面表面、面下及听神经区进入。顶盖中脑肿瘤可经滤泡上、滤泡下和外侧中脑沟进入,而髓质和颈髓肿瘤可在obex下的后正中裂、后中沟和后外侧沟行纵向脊髓切开术。
一旦肿瘤已经到达,它的一致性将被评估,并将决定切除的方法根据外科医生的偏好。肿瘤标本应尽快提交,以确定组织学。组织学将决定是否可行的全切除,这在良性肿瘤的情况下更有可能。根据外科医生的喜好,可以使用微牵开器。肿瘤应该一点一点地切除,而不是整块整块地切除。如果囊肿与肿瘤相关,切除囊性液体可以提供额外的操作空间,从而有助于肿瘤的减容。低强度、低抽吸率和/或微剪超声抽吸对实体瘤更合适。微双较凝血术和同时抽吸凝血组织可用于软组织肿瘤。手术切除需局限于肿瘤内部,以避免损伤周围正常结构。在大部分肿瘤去瘤后,寻找肿瘤和正常脑之间的正常边界。当肿瘤和正常脑之间的界限被确定时,在大多数情况下全切除是可行的。当无法看到两者之间的界面时,应停止肿瘤切除,因为决定继续对病灶进行减厚可能会增加术后神经系统并发症的机会。此外,一些肿瘤可能具有高血管密度,在肿瘤减容时血管需凝固,这可能会对周围正常大脑造成缺血性损伤。
对于具有外生性成分的局灶性肿瘤,肿瘤的这个突出的方面为手术进入肿瘤提供了一种途径。此外,穿透蛛网膜下腔的肿瘤可接触或包住重要动脉,穿透脑干腹侧的肿瘤可接触椎动脉或基底动脉及其分支;因此,需小心地接触这些肿瘤。脑桥或髓质室管膜下的肿瘤,没有或很少侵入脑干,突出四脑室,是一组良性的背侧外生性肿瘤,可以成功切除。
手术后护理
在接受脑干手术后,患者需要在术后立即进行密切观察。患者至少应在重症监护室插管过夜,并可进行CT扫描以确定出血和/或脑积水。外科医生应准备好放置脑室导管以防止梗阻性脑积水的发生,特别是对四脑室肿瘤。当CT无异常、患者恢复意识、通气参数显示患者能够自主呼吸时,可进行拔管。一些接受中脑损伤手术的病人在完全恢复意识之前可能会经历长期的昏睡或昏迷状态。下脑干肿瘤的手术可能会导致吞咽困难、声带麻痹和/或咳嗽和咽反射丧失,这是可以预料的。一些患者术前可能有吞咽困难,术后可能恶化。需高度警惕地观察这些病人,因为他们可能有误吸的危险。
结论
脑干手术对神经外科医生来说是一个较大的挑战,但影像学、手术方法和术中神经生理监测的进步降低了与这些手术相关的风险和发病率。局灶性内源性脑干肿瘤,有或没有外生性成分,主要是外生性病变是指适合手术切除。尽管脑干手术的显微外科技术已经取得了进展,但这些技术的持续发展仍需要为患者提供尽可能好的护理。此外,由于成人脑干胶质瘤占胶质瘤的比例不到3%,因此人们对其知之甚少,与儿童相比,相关研究也很少。然而,很少有研究报告表明,成年人的存活时间比儿童更长。需要更多的研究来评估这些肿瘤的自然史和手术结果。




