35岁女士,2020年2月在A医院确诊为左顶凸面占位脑膜瘤,大小约3cm,6月实行全切切除。病理分析为who1-2级,Ki67为15%,建议咨询放疗专家。
她随后咨询B医院放疗科。B医院认为ki67有15%较高需要放疗,但建议根据A医院切片重新到镜下做病理分析后再决定。结果肿瘤医院结论为1级, Ki67为5%。
由于感觉两个医院分歧较大,随后请C医院、D医院、E医院的病理专家再做了分析。C医院同A医院,认为分级为1-2级,ki67为10%,建议按照二级治疗,而D医院同认为分级为1级。
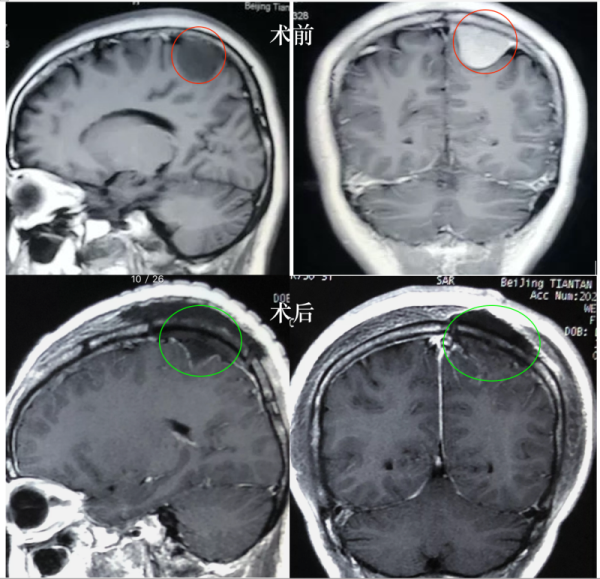
为什么同样的肿瘤不同地方病理分析结果这么大差异?患者到底要不要放疗?应该按照何种分级治疗呢?
解析一:关于脑膜瘤
脑膜瘤是起源于脑膜成分的肿瘤,其内主要含有蛛网膜细胞或蛛网膜细胞分化的细胞。纤维型脑膜瘤是脑膜瘤常见的病理亚型,属于较少出现复发和侵袭的脑膜瘤2007年WHO根据脑膜瘤复发倾向和侵袭性对其进行分级和分型,分为3级15种病理亚型。
WHO I级为良性脑膜瘤(Benign meningioma,BM),包括脑膜上皮型、纤维型、血管瘤型、砂粒体型、过渡型、微囊型、淋巴细胞丰富型、分泌型及化生型
WHO II级性质介于良恶性之间,包括非典型性、透明细胞型及脊索样型;约占脑膜瘤的4.7%~7.2%,其性质介于良、恶性脑膜瘤之间,同I级脑膜瘤相比有较高的侵袭性及复发率,以非典型性脑膜瘤(Atypical meningioma,AM)为主。
WHO III级为恶性脑膜瘤(Malignant meningioma,MM),包括间变型、横纹肌样型及乳头样型。少见,约占脑膜瘤的1%~3%,具有很高的侵袭性及复发率。间变型脑膜瘤(Anaplastic meningioma)可由I、II级脑膜瘤演变而来,也可一开始即为恶性生长方式。
淋巴细胞丰富型脑膜瘤LPRM (Lymphoplasmacyte-rich meningioma)
富于淋巴细胞浆细胞型脑膜瘤于1971年一次被英国学者BaneIjee和Blackwood报道,其发病率为约为1.7%,此型肿瘤内可见以淋巴细胞为主的慢性炎细胞浸润,可伴有生发中心结构,此类肿瘤也可见脊索样的组织学表现,但多出现于儿童和青少年。富于淋巴浆细胞型脑膜瘤多不具 备良性脑膜瘤典型影像特征,如脑膜尾征、脑外肿瘤 镶嵌征、宽基底实性肿块等,常易误诊为炎性肉芽肿、淋巴瘤、静脉性梗死及其他恶性肿瘤等疾病
影像特点
典型MRI表现为等或稍长T,信号、等或长R信 号,形态不规则,瘤周水肿明显,增强后明显均匀强化,周围 脑组织受压。有文献报道,儿童脑膜瘤的特征性MRI表现 为缺乏“脑膜尾征”。本例中肿瘤边界清楚,周围可见“脑 膜尾征”,DWI无扩散受限,表现为等信号,提示为良性肿瘤。肿瘤的不规则形态及明显的瘤周水肿有助于其与星形 细胞瘤、幕上原始神经外胚层肿瘤及髓母细胞瘤相鉴别。
解析二: Ki67指数意义
在肿瘤病理报告中,经常会看到ki67阳性细胞的比例。临床医生知道这是判断肿瘤恶性程度的,但往往并不明白其中的缘由。肿瘤的较大特点是生长失控。很多人误认为肿瘤的生长失控是细胞分裂加快、细胞周期缩短的结果。但实际上肿瘤细胞的分裂减慢,细胞周期甚至比正常的细胞周期长,只是处于增殖期的细胞数量增多了,肿瘤才生长迅速,超越了周围的组织。
在正常组织中,绝大部分细胞处于非增殖状态,细胞学上称为G0期。要构建良好的组织结构并执行特定的功能,需依靠这些增殖周期外的G0期细胞。打个比喻,G0期的细胞就像工蜂、工蚁一样。那些增殖的细胞就像蜂后、蚁后一般。当工蜂、工蚁的比例减少时,劳动效率必然会下降,导致组织结构不良。而处于增殖状态的细胞是难以执行特定功能的,也就是常说的没有分化。病理医生常看到肿瘤的死亡细胞增多。按照新说法,这可能迫使更多的周围细胞进入增殖周期,G0期细胞的比例减少,从而导致肿瘤组织的结构紊乱,病理学上称之为分化差。
多年以来,病理医生常用细胞的有丝分裂像作为判断肿瘤增殖速度、恶性度的指标。但在实际应用中这一指标的使用受到很大的限制。免疫组织化学解决了这一问题。Ki67单克隆抗体是在位于德国Kiel市的一所大学建立而得名。Ki67免疫组化染色可将大部分G0期以外的细胞标记,因而也被称为细胞的增殖指数。Ki67的阳性率越高,说明处于增殖周期的细胞比例越高,肿瘤生长越快;而G0期细胞自然就越少,组织分化越差。
有意思的是,Ki67的阳性比例常与细胞死亡的频度成正比。那么是细胞增殖多导致了死亡多,还是细胞死亡多导致了增殖多呢?如果是前者,应该是细胞死亡越多,则患者预后越好。但事实是,细胞死亡越多,患者的生存期常越短。所以,死亡增多导致增殖增加的推测更为合理。 这样看来,Ki67是一个预后不好的标记。但话分两头说。对肿瘤化疗敏感的常是处于细胞增殖周期的细胞,那些G0期的细胞一般对化疗没有什么反应。所以,Ki67比例高的肿瘤往往对化疗敏感,化疗效果好。 简单地说,Ki67标记的是处于增殖周期中的细胞。该标记阳性率越高,肿瘤生长越快,组织分化越差,对化疗也越敏感。一般来说,预后较差。
Ki-67 与瘤周水肿的关系
脑膜瘤瘤周水肿是一种常见的继发性病理改变,发生机制目前尚不完全明确,可能与肿瘤的自身因素、内分泌活性以及血 - 脑屏障的损害有关。 本研究发现瘤周水肿是 Ki-67 高表达的独自危险因素。 Ki-67 越大,肿瘤增 殖活性越强, 耗氧量增加, 刺激细胞分泌血管内皮 生长因子 ( VEGF ),促进肿瘤血管生成,但新生血管缺乏基底膜,血管壁通透性高,导致血浆外渗,加重瘤周水肿。并且肿瘤增殖活性高,生长速度过快,可在短时间内压迫血管,使血管超出自身代偿能力。 因此,术前评估瘤周水肿程度,可在程度上反映肿瘤的恶性程度。
Ki-67 与肿瘤大小的关系
肿瘤大小除与肿 瘤恶性程度、增殖潜能有关外,还与病程有关。有研究显示病人的中位病程时间为 2 个月 (病程时间按体检发现肿瘤或出现症状就诊开始计算),当肿瘤位于非功能区且未引起明显颅内高压症状时,病人往往未曾察觉,这就导致无法准确获取病程时间。但 Ki-67 指数高的肿瘤,往往生长速度更快,可在短时间内 压迫周围脑组织,引起颅内高压,导致症状出现,病程可短于 Ki-67 指数低者。研究指出:肿瘤级别越高,较大径越大,体积越大。
Ki-67 与 NLR 的 关 系
中 性 粒 细 胞 具 有 趋 化、吞噬和杀菌作用, 活化时既能释放出细胞因子 如腺素 E2 ( PGE2 )、环氧化酶 -2 ( COX-2 ) 影 响炎症细胞的募集和活化, 也能产生大量氧自由 基, 造成氧化损伤、DNA 突变及微环境改变, 促进肿 瘤细胞的生长分化[13] 。中性粒细胞还可释放弹性蛋 白酶、白细胞介素 -1 ( IL-1 )、白细胞介素 -6 ( IL-6 ),控制肿瘤坏死因子 -α ( TNF-α ) 的生成,分泌 VEGF ,促进肿瘤血管的生成及肿瘤细胞的转移 。淋巴细胞可特异性地识别肿瘤细胞并释放细胞因子,介导 细胞毒性反应,控制肿瘤细胞的增殖和转移,同时也可控制肿瘤细胞的生长,促进其凋亡。但有研究显示:肿瘤细胞可通过程序性死亡因子配体诱导 CD8 阳性的 T 细胞凋亡, 从而控制肿瘤浸润的淋巴 细胞。 因此, 外周血 NLR 升高往往会提示有中性粒 细胞相对升高或淋巴细胞相对减低,或两者同时存在,其主要作用是综合反映促肿瘤炎症反应和抗肿瘤免疫反应的平衡状态。本研究发现 NLR 越高的病人,Ki-67 指数越大, 提示机体处于失衡状态,以促肿瘤生长为主,往往提示临床预后差。
Ki67预后肿瘤复发及预后肿瘤复发的时间
人们普遍认为Ki-67 PI与复发相关,但该认识并非基于长期随访的基于人群的连续数据。 实际上,先前的文献报导是存在有相互矛盾的,目前也有小部分学者对此是质疑态度的。今年一篇发表于神经外科顶刊Neurosurgery的文章研究报导了,Ki-67 是复发的合适评估因子,长期随访表明,Ki-67 是何时可能复发而不是脑膜瘤是否复发的标志。 长期随访策略需要考虑切除范围和肿瘤增长率,而Ki-67 能够很好地反映增长率,研究结果不支持将高Ki-67 指数定义为复发风险组。

解析三:脑膜瘤到底放疗与否?
脑膜瘤的治疗一般以手术切除为主, 根据较新的脑膜瘤治疗指南,WHO1/2级脑膜瘤全切术后不予放疗,术后有残留予以放疗辅助。WHO3级不论手术切除程度建议予以放疗。同时若有Ki67指数高,部分医师也会结合患者情况建议术后放疗。外科手术切除是脑膜瘤的优选治疗方式,其治疗效果是伽玛刀所无法具备的。但对于因为以下情况而无法手术的患者而言,可以采用伽玛刀进行治疗。
6、患有心肺肾、血液系统疾病或糖尿病等,有手术禁忌或不能耐受手术的患者。
需要特别指出的是,脑膜瘤患者应在专家的指导下选择是否采取伽玛刀治疗;特别是因肿瘤形成占位效应,出现明显功能缺失者,应立刻考虑手术。切勿因畏惧手术而丧失根治疾病的机会。
多发性脑膜瘤应考虑分期治疗
多发性脑膜瘤患者,难以通过一次性照射而达到治疗效果。如病灶恰好分布于脑干两侧,如果同时治疗,脑干位于一次性治疗计划中的高剂量区,危险较大;再如患者脑内不同病理性质的多发肿瘤,由于病灶各自所需的治疗剂量相差悬殊,也应分期进行伽玛刀治疗。
咖玛刀治疗常见并发症
脑水肿
膜瘤伽玛刀治疗后常见的并发症是脑水肿,多数发生在治疗后1-6个月,体大的脑膜瘤水肿可以长达8-12个月。
与瘤周水肿相关的因素包括:治疗前瘤周水肿情况、治疗边缘剂量、肿瘤体积、部位等。其原因可能是认为幕上脑膜瘤邻近皮层静脉,缺乏侧枝循环。当伽玛刀治疗影响深静脉的引流时,将造成或加剧瘤周水肿。
颅神经损伤
由于肿瘤长期侵蚀或压迫颅神经,会降低神经组织对放射线的耐受性,因此颅神经受损也是伽玛刀治疗脑膜瘤常见的并发症,主要包括视神经、动眼神经、三叉神经、外展神经、面神经及听神经。为防止神经受损,制定治疗计划时应综合进行考虑,对不同部位的脑膜瘤放疗进行剂量控制。
放疗副反应
伽玛刀治疗后24~48小时内,是鞍区、岩斜或桥小脑角肿瘤患者可出现短暂的头痛、恶心或呕吐。出现症状的原因与四脑室底部呕吐中枢受射线刺激引起的急性反应,使用镇吐、激素等对症治疗即可缓解。治疗前存在头痛、癫痫等症状者,仍需对症抗癫痫治疗。
总结:WHO病理结果本身也受病理医师、检测方法的影响,甚至术者所取标本组织的差异也会决定病理结果的不一致,临床中这样的情形偶尔可见。在该病例中,凸面脑膜瘤靠近运动功能区,手术全切,WHO分级及Ki67指数不同医院结果不一样,患者病理提示I级或I-II级,Ki67指数5%-15%,放疗或不放疗都有潜在“收益和风险”。根据在德的经验和治疗指南,结合病人年龄、靠近功能区、影像特点、手术全切、病理结果及术后无明显功能障碍,建议密切观察MR及随访,可暂不放疗,如果肿瘤复发,病情允许,建议再次手术治疗。病人遇到这样的情况时,多咨询是对的,建议能最终明确病理结果,若情况允许可以再取标本组织重做病理切片。同时也是建议选择较了解患者病情的好的主管医师就诊,根据病人情况综合决定治疗方案,不同神经外科医师、放疗科决策者的经验和认识不同、病患的需求不同,都会造成治疗建议的差异,况且很多治疗方案都是有潜在的益处和风险,病人个体也具有很大差异,对于很多尚有争议的领域,医学上也没有“统一、正确”的方案,很多时候医者也只能给出医学角度的建议。
5.富于淋巴细胞浆细胞型脑膜瘤临床研究进展.中华医学杂志. 2013




