近日,辛辛那提大学(UniversityofCincinnati)教授安德鲁·斯泰克尔(AndrewSteckl)与约翰·霍普金斯大学(JohnsHopkins University)的研究人员合作,开发了一种治疗多形性胶质母细胞瘤(GBM)的新方法。Steckl的纳米电子实验室应用了一种称为同轴静电纺丝的工业制造工艺,以形成含药物的膜。
多形性胶质母细胞瘤(GBM)是常见和具侵袭性的原发性脑肿瘤,发病率约为3.2例/10万人/年,5年生存率为5.1%,其治疗主要依赖于大水平的顺利手术切除以及手术后的辅助治疗放疗、化疗。但由于脑中血脑屏障(BBB)的存在,药物输送和利用的效果并不好,加上化疗本质上是全身治疗,治疗需通过血脑屏障,这意味着全身剂量要高得多,很大可能对患者产生较大毒副作用。正是由于以上限制,GBM患者平均生存时间小于15个月。
而Steckl教授纳米电子实验室所研究的同轴静电纺丝,其将两个或多个材料组合成由一种材料的重要与另一种材料的鞘包围而成的细致纤维,这种制造工艺允许研究人员利用每一种材料的独特特性,立即或在一段时间内传递药物的强烈部分。
“通过选择纤维的基材和鞘层厚度,我们可以控制这些药物的释放速度,”Steckl说。
静电纺丝技术还使得连续纳米纤维的合成成为可能,其直径从数十纳米到微米不等。纤维静电纺丝及其许多应用已得到证实,纳米纤维的物理和化学性质可以通过控制聚合物浓度、添加剂和溶剂选择来控制。此外,静电纺丝技术的通用性还可以通过使用两个流体同轴喷嘴电纺丝来形成芯鞘纤维进一步得到扩展。
研究发现,将静电纺丝膜转变为纳米膜,在保持纤维结构的同时,降低了膜的孔隙率,提高了载药量。利用静电纺丝制成的uc-1纳米粒片的载药量为95 mgmm。而uc-1膜载药量为17g/mm。明显地,药物负载量在转化为椎间盘型后增加了5.6倍。其增加了可应用药物的数量,降低了最初的爆裂释放,并增强了药物释放的可持续性。
使用电纺纤维的化学疗法在三个单独的动物试验中提高了存活率,这些试验验证了顺利性、毒性、膜降解和合适性。
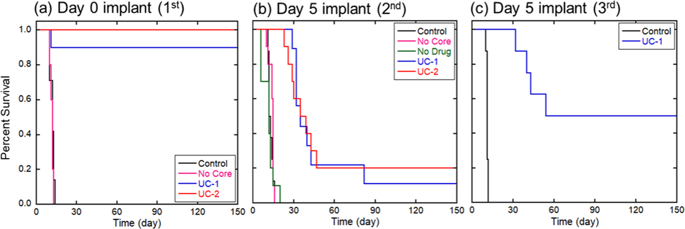
图1:未处理的对照组大鼠和植入“无核”纳米粒子的大鼠的中位生存期为12天,而静电纺丝技术转变的纳米粒子,植入试验小鼠体内,延长了其生存期:(a)试验1、0天植入、植入UC-1和UC-2纳米粒分别获得86%和全切的长期生存率(LTS);(b)试验2、植入5天,观察到uc1和uc2处理组的中位生存期分别增加36和37天(p < 0.0001 vs.对照组);(c)试验3,5天植入物,证实使用50% LTS的uc1处理的动物中位生存增加(p < 0.0001比对照组)。
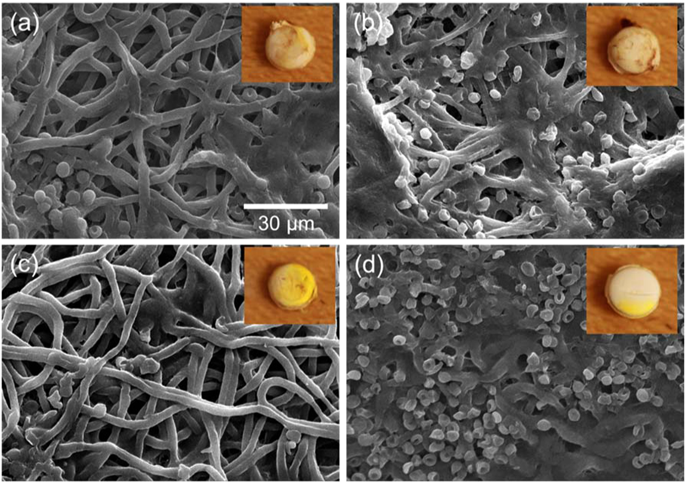
图2:试验小鼠中植入后纳米粒子的电子显微镜(SEM)图像:(a)植入后18天“无芯”;(b)植入后12天“无药物”;(c)植入后32天的UC-1;(d)植入后34天的uc2;插图是相应光盘的图像。
此外,静电纺丝技术制成的纳米膜可以结合不同的疏水和亲水性化合物,根据它们在治疗特定恶性肿瘤的疗效和耐药性,以更个性化的方式定制特定的药物,并提供替代和合适的机会。
这项研究总结:“这代表了目前对GBM治疗的一种有希望的发展。”
虽然这项研究使用了单一的药物,但研究人员注意到静电纺丝的一个优点是能够在长期释放过程中顺序分配多种药物。而较新的癌症治疗方法依靠多种药物来预防耐药性和提高疗效。
Steckl说,这项研究有望治疗其他类型的癌症。
Steckl说:“展望未来,我们计划研究‘鸡尾酒’疗法,在这种疗法中,多种联合治疗难治性脑肿瘤或其他癌症的药物被同时或顺序地从我们的纤维膜中释放出来。”
参考文献:Daewoo Han, Riccardo Serra, Noah Gorelick, Umailla Fatima, Charles G. Eberhart, Henry Brem, Betty Tyler, Andrew J. Steckl. Multi-layered core-sheath fiber membranes for controlled drug release in the local treatment of brain tumor. Scientific Reports, 2019; 9 (1) DOI: 10.1038/s41598-019-54283-y




