James T.Rutka(鲁特卡)教授曾任世界神经外科学院院长,30多年来深耕儿童神外研究,带领团队不断突破,从脑瘤分子分型、精准治疗、新药治疗、微创治疗,为全球神经外科疑难病患儿带来希望,他新近发表了研究《Preclinical assessment of checkpoint blockade combined with DNA methyltransferase inhibition in high-risk pediatric brain tumors reveals limited therapeutic synergy》(高危儿童脑肿瘤中检查点阻断联合DNA甲基转移酶抑制的临床前评估显示有限的治疗协同作用),以下是研究简述。

01
PART
关键要点
PBTs显示出免疫细胞浸润的异质性表达。
DAC治疗显示在H3野生型DIPG和ATRT小鼠模型中延长生存期。
骨髓来源的抑制性细胞丰度可能是治疗反应的主要影响因素。
02
PART
研究背景
尽管进行了强化治疗,高危儿童脑肿瘤(PBTs)的结局仍然很差,这促使我们寻找新的治疗方法。DNA甲基转移酶抑制剂(DNMTi)已被证明可以启动肿瘤,以提高对检查点抑制的反应。本研究的目的是探讨地西他滨(DAC)联合PD-1抑制剂在儿童高危脑肿瘤模型中提高生存期的潜力。
03
PART
研究方法
研究分析了人类PBT数据集以确定免疫细胞标志物的基因表达水平。在代表H3野生型弥漫内生型脑桥胶质瘤(DIPG)、H3K27突变型弥漫中线胶质瘤(DMG)、非典型畸胎样/横纹肌样瘤(ATRT)和髓母细胞瘤(MB)的小鼠模型中,测试了肿瘤对DAC(联合或不联合PD-1抑制剂)的反应。对同种异体移植肿瘤进行CyTOF分析,以表征肿瘤微环境内的变化。
04
PART
研究结果
PBT亚型的分析揭示了免疫细胞标志物、检查点受体和MHC分子的异质性表达。DAC处理降低了人和小鼠肿瘤细胞的DNA甲基化,并增加了新抗原表达。DAC治疗在DIPG和ATRT的同基因小鼠模型中延长了生存期,但在DMG和MB模型中则没有。然而,当与PD-1抑制剂联合使用时,未观察到额外的生存获益。小鼠肿瘤的CyTOF分析揭示了局部免疫细胞浸润的变化。
(1)儿童脑肿瘤免疫相关标志物表达具有异质性
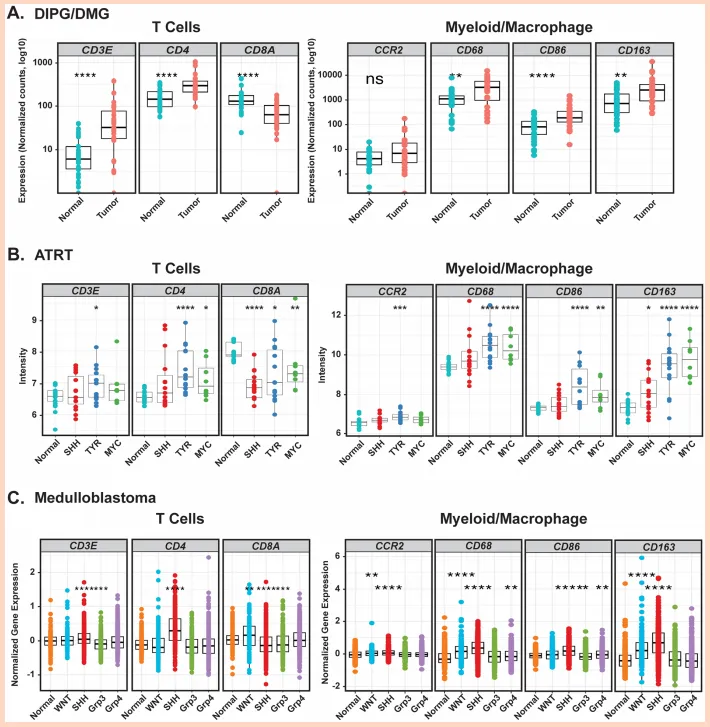
图1.儿童脑肿瘤在特定免疫相关标记物方面具有异质性。(A)对28例DIPG/DMG患者的配对肿瘤与正常组织样本进行表达分析。(B)对ATRT肿瘤样本(包括15例SHH、8例MYG、14例TYR)以及21例正常胎儿脑组织样本进行表达分析。(C)对Swartling数据集进行基因表达分析,该数据集包含23个经过整合和批次校正的转录数据样本,涵盖291例正常脑组织、118例WNT、405例SHH,233例Group3和530例Group4样本。ns=P>.05.星号表示:P<.05,P<.01,P<.001,P<.0001.
(2)儿童脑肿瘤细胞系表现出MHC I和PD-L1表面表达的异质性
(3)DAC在儿童脑肿瘤细胞中诱导MHC I和新抗原表达
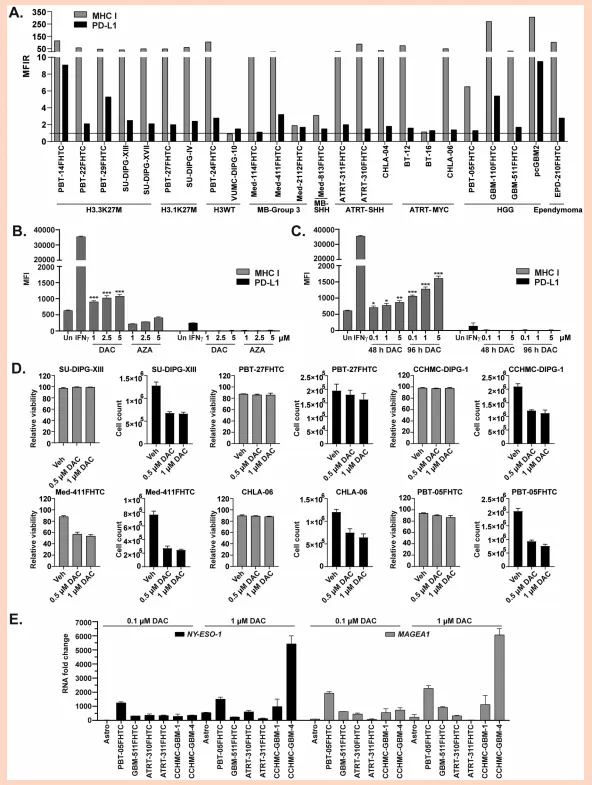
图2.DNA甲基转移酶抑制剂DAC诱导人科脑肿瘤细胞中MHCI和新抗原的表达。(A)各种儿科脑肿瘤细胞系中MHCI和PD-L1的基线表达情况。MFIR等于染色细胞的中值荧光强度除以同型对照。横线表示MFIR为1。(B)DAC或AZA处理2天后PBT-05FHTC细胞中MHCI表达的变化情况。Un为未处理组。IFN-y(50ng/mL作用48小时)被用作阳性对照。星号表示:P=0-0.001,0.001-0.01,0.01-0.05°。(C)DAC对MHCI表达的影响具有剂量和时间依赖性。(D)对多种细胞系进行0.5和1uMDAC处理72小时,评估其细胞毒性。(E)定量PCR评估NY-ESO-1和MAGEA1新抗原基因的表达情况,在多组PBT细胞经DAC处理3天后进行。Astro,正常人类星形胶质细胞。
(4)DAC影响小鼠同基因脑肿瘤细胞系的细胞活力、整体甲基化和新抗原表达
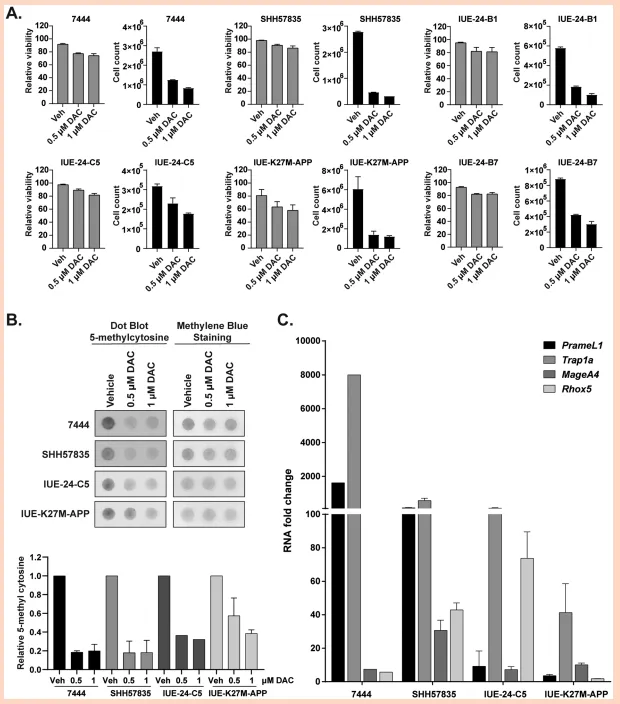
图3.DAC对小鼠同种细胞系细胞生长、存活和新抗原表达在体外的作用。(A)通过评估细胞经0.5和1uM DAC处理72小时后所受的细胞毒性作用来评价细胞毒性。(B)使用5-甲基胞嘧啶特异性点印迹法评估整体低甲基化情况。gDNA从经DAC处理2种浓度(0.5和1M)72小时的相同种细胞系中提取。(上栏)每点加载100 ng的gDNA,并使用甲烯蓝染色作为加载对照。(下栏)对点印迹进行密度分析并绘制为柱状图。(C)定量PCR评估PrameL1、Trapla、MageA4和Rhox5新抗原基因的表达情况,这些基因在多株小鼠同种细胞系经3天0.5MDAC处理后均有表达。
(5)PD-1抑制增强DAC的抗肿瘤活性
(6)DAC处理在异位模型中诱导CTA表达
(7)DAC在DIPG和ATRT模型中提高生存期
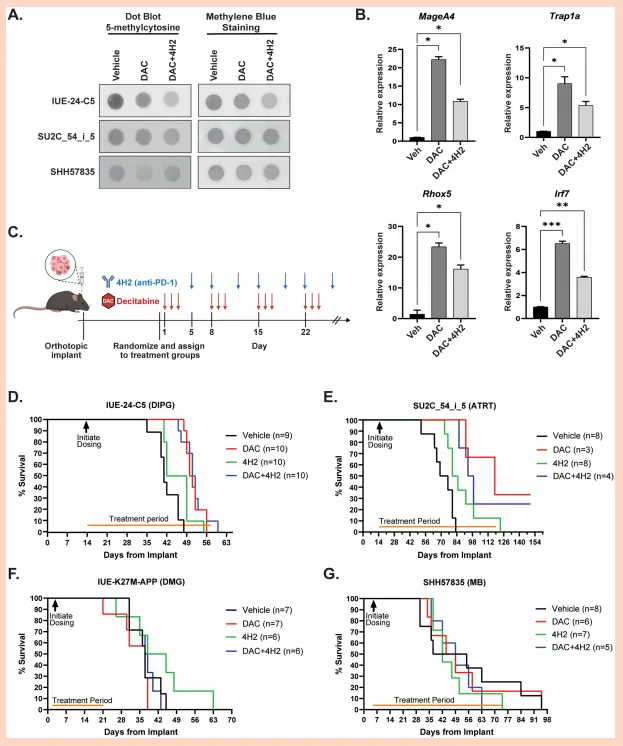
图4.在正位同基因模型中,DAC、DAC+4H2或4H2治疗反应各异。(A)采用5-甲基胞嘧啶特异性点斑分析评估DAC在小鼠脑肿瘤组织中的活性。gDNA从不同模型建立的脑肿瘤中分离,并用DAC或DAC与4H2的组合治疗。每点加载100 ng的gDNA,并使用亚甲蓝染色作为加重控制。(b)利用定量PCR评估肿瘤组织中新抗原基因表达和炎症,该肿瘤组织由IUE-24-C5合成小鼠(用载体(Veh)、DAC或DAC+4H2处理处理。(C)DAC和4H2在合成模型中的处理策略示意表示。红色箭头表示DAC的IP剂量(0.5 mg/kg),蓝色箭头表示抗PD-L1(4H2)的IP剂量(200微克)。用BioRender.com制作的模型。代表存活数据的Kaplan–Meier曲线(D)DIPG模型IUE-24-C5(Veh与DAC P=0.001,Veh与4H2 P=0.6088,Veh与DAC+4H2 P<.0170)、(E)ATRT模型SU2C_54_i_5(Veh与DAC p=0.0079,Veh与4H2 P=0.0027,Veh与DAC+4H2 P=0.0176)、(F)DMG模型IUE-K27M-APP(Veh与DAC P=.6030,Veh与4H2 P=0.4658,Veh vs DAC+4H2 P=0.7927),以及(G)MB SHH57835(Veh vs DAC P=0.9873,Veh vs 4H2 P=0.9690,Veh vs DAC+4H2 P=0.9831)。星星代表:P=0-0.001,0.001-0.01,0.01-0.05。
(8)DAC+4H2治疗可以重塑免疫肿瘤微环境
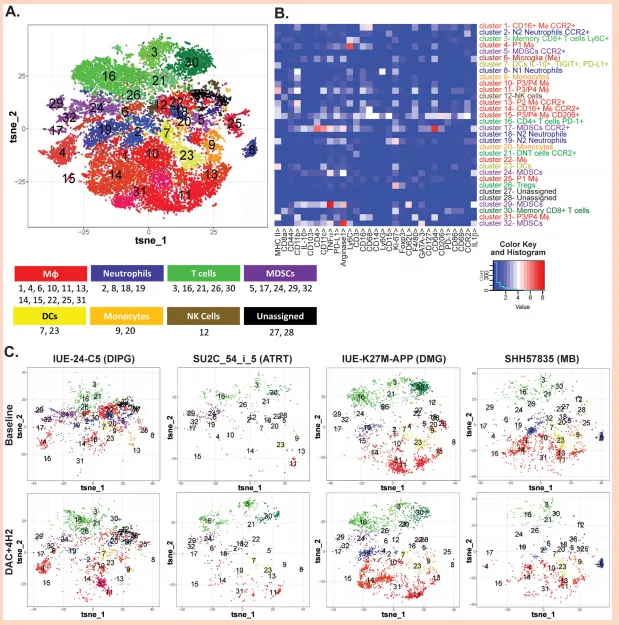
图5.基线时同源TME与DAC+4H2联合治疗的免疫组成。使用CyTOF分析了免疫细胞浸润及联合治疗效果。(A)所有样本的表型图聚类。t-SNE图,表示基线所有模型,不同细胞群体以颜色标示为簇。(B)热图显示各簇中特定免疫标志物的表达。(C)针对每个单个肿瘤模型在基线(上层)及DAC+4H2(下)处理后(n=每个病症、每个模型3颗肿瘤)的t-SNE图。
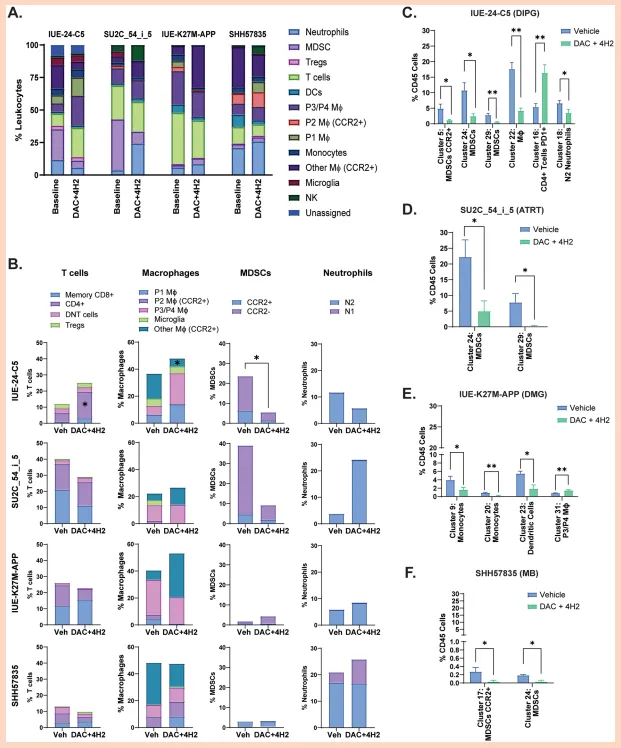
图6.基线与DAC+4H2治疗的联合肿瘤聚类分析。(A)基线及DAC+4H2治疗后各肿瘤类型白细胞群体的相对比例。(B)各肿瘤模型中,载体处理小鼠与DAC+4H2治疗小鼠中T细胞、巨噬细胞、MDSCs和中性粒细胞的相对百分比。(C)IUE-24-C5、(D)SU2C-54_i_5、(E)IUE-K27APP和(F)SHH57835模型的单个细胞簇发生显著变化。P=0.001−0.01,0.01−0.05。
05
PART
总结
DAC单独使用或与检查点抑制剂联合使用可以改变小鼠肿瘤模型中的免疫微环境。在H3野生型DIPG和ATRT模型中观察到了变化,这表明某些肿瘤亚型可能对DNMTi的免疫启动有反应。
PBTs中存在的独特TME具有低淋巴细胞浸润和免疫学惰性的特征,这与低突变负荷相关。这种独特的TME,加上治疗性抗体对BBB的渗透性差,有助于解释历史上在PBTs中ICI治疗后观察到的次优反应。事实上,在一小部分具有高突变负荷的罕见儿科肿瘤中,已经观察到了持久的治疗结果,这些肿瘤对ICI治疗显示出显著的反应。这为免疫启动剂提供了重要的机会,以帮助和解决这种差异,从而提高PBTs中ICI治疗的疗效。
我们的研究结果表明,使用DAC作为免疫启动剂可能在DIPG和ATRT同基因小鼠模型中提供益处。此外,我们注意到在DIPG和ATRT模型中,与对照组相比,治疗后在巨噬细胞、MDSC和T细胞群体方面存在生存期延长和TME差异。有趣的是,DIPG和ATRT模型在用DAC和4H2治疗前都具有高的基线MDSC群体,该群体在治疗后显著减少。这与无反应的DMG和MB模型形成鲜明对比,后者不含如此高的MDSC群体,表明肿瘤亚型之间的潜在差异是免疫启动剂的重要考虑因素。DIPG和ATRT小鼠模型的结果表明,虽然免疫启动剂与免疫检查点抑制剂(ICI)的组合并未将总生存期提高到超过单独使用DAC所达到的水平,但有值得考虑的见解。我们的研究结果表明,DAC治疗成功地在脑肿瘤中诱导了新抗原,尽管它并未导致CD8+T细胞浸润,这与我们在侧腹模型中的发现相反。这表明虽然这种特定组合可能不代表改善患者结局的可行治疗策略,但它为进一步探索优化ICI疗效和了解不同肿瘤环境中的免疫反应打开了大门。
MDSCs是从骨髓释放的成熟和未成熟单核细胞和粒细胞谱系细胞的异质性群体,长期以来一直与肿瘤进展和免疫逃避相关,因为它们能够抑制CD4+和CD8+T细胞增殖。类似于在小鼠卵巢癌模型中的观察,使用像DAC这样可以调节MDSC活性的药物,可能会减少PBTs中MDSCs在微环境中产生的淋巴细胞抑制。此外,实体瘤通常被巨噬细胞群体包围,其中很大一部分是MDSCs。CCR2+单核细胞抑制实体瘤中的T细胞浸润,而我们在IUE-24-C5和ATRT模型中的数据显示了类似的观察结果。这表明在更高级别的肿瘤中,MDSC表达可能增加,逆转由MDSCs驱动的免疫抑制状态对于ICI治疗的疗效至关重要。
相反,另一种方法是促进更具免疫原性的TME。提出的策略包括利用促进内源性逆转录病毒表达和增加I/II型干扰素反应的药物,以驱动PD-1表达并增加肿瘤抗原对宿主免疫细胞的呈递。虽然已知地西他滨具有内源性逆转录病毒表达活性,但我们的研究结果表明,其抗MDSC效应比其促免疫原性效应产生了更大的ICI亲和力,这表明最初促进一个促淋巴细胞增殖的TME比增强肿瘤免疫原性更重要。
虽然我们的研究结果表明是PBT治疗中有希望的第一步,但仍存在一些挑战和局限性。从同基因小鼠模型到临床试验的转化可能无法反映我们患者队列中存在的生物学和TME的复杂性。例如,与小鼠模型中较短的生长时间相比,由于PBTs肿瘤生长的长期性,其MDSC群体可能全面增加。因此,如果靶向MDSC群体能提高ICI疗效,这表明通过免疫启动在PBTs中全面提供不同的患者益处可能有机会。然而,虽然靶向MDSC群体作为在PBTs中产生更大免疫原性反应的策略显示出前景,但不应忽视TME内存在的其他免疫抑制机制的作用。肿瘤已被证明采用了多种逃避和抑制机制,包括调节性T细胞、肿瘤相关巨噬细胞和免疫抑制细胞因子,这些可能为免疫启动和改进ICI治疗提供额外的治疗靶点。因此,需要进一步研究以评估可能使无反应肿瘤(如我们研究中的DMG和MB模型)产生反应的替代免疫学靶点。
其次,ICI分子穿透BBB仍然是一个考虑因素。包括卵巢癌、结肠癌、胰腺癌、和黑色素瘤在内的小鼠癌症模型在用DNMTi和ICIs治疗时显示出显著的临床前疗效。然而,这些模型没有需要应对额外的BBB复杂性,因此到达其靶标的ICIs有效浓度可能更高。这确实可能与我们侧腹和原位IUE-24-C5模型之间观察到的反应差异有关。当前的临床前和临床研究正在积极解决这个问题,以增加向脑肿瘤细胞递送ICIs。对流增强或超声介导的递送、激光间质热疗等技术,以及手术和/或放疗与ICI给药的最佳时机和测序策略,有望降低这一障碍。
最后,联合免疫启动剂和ICI治疗的潜在不良反应需要进一步研究。虽然DAC可以通过调节TME来增强抗肿瘤免疫反应,但其全身效应能够产生骨髓抑制状态并减少造血功能。除了与ICI治疗相关的已确立的免疫炎症副作用和假性进展外,对于接受这两种药物治疗的患者会出现什么不良反应仍不清楚。平衡治疗效果与不良反应对于优化治疗方案和确保患者安全至关重要。此外,DNMTi具有双重活性,即DNA的低甲基化和通过DNA损伤的细胞毒性活性。⁶³这可能会抑制免疫细胞的增殖。因此,选择最佳剂量和时间对于实现预期的免疫调节效果的持续低甲基化非常重要。
总之,我们表明,通过对各种儿童肿瘤基因表达数据集的分析,各种免疫相关标志物的表达存在异质性。具体来说,MHC I和PD-L1的异质性也可以在各种患者来源的细胞系中观察到。我们还证明,低剂量DAC处理可以在体外降低人类肿瘤细胞系的生长并增加MHC I和新抗原表达。此外,我们发现这些对低剂量DAC处理的反应转化到代表各种PBTs的小鼠同基因细胞系,这使我们能够在具有完整免疫系统的动物中进行临床前测试各种治疗。尽管DAC在原位同种异体移植物中诱导了DNA甲基化和新抗原表达的变化,但只有DIPG和ATRT模型显示出生存期改善。这种差异反应可以部分地通过TME免疫细胞组成(特别是MDSCs)的变化来解释,从而为未来临床试验中可能对患者进行分层的方法提供了一些见解。
06
PART
研究重要性
患有高危PBTs的儿童面临严峻的结局。免疫检查点抑制剂(ICI)的成功已在多种成人恶性肿瘤中得到证实;然而,在PBTs中尚未实现此类有益结果。在此,我们在高危PBTs的同基因小鼠模型中研究了DNMTi和PD-1检查点抑制的单药和联合治疗。我们的结果表明,一些H3野生型DIPG和ATRT肿瘤类型可能对DNMTi治疗有反应,值得进一步研究。
中枢神经系统(CNS)肿瘤仍然是儿童癌症相关死亡的主要原因。预后不良的PBTs,如弥漫中线胶质瘤(DMG)(包括弥漫内生型脑桥胶质瘤(DIPG))、高级别胶质瘤(HGG)、非典型畸胎样/横纹肌样瘤(ATRT)以及MYC和MYCN扩增的髓母细胞瘤(MB),其临床结局仍然很差。由手术、放疗(RT)±化疗组成的多模式治疗在该人群中产生了0%-50%的5年无事件生存期(EFS)。不幸的是,幸存者经历了显著的治疗相关后遗症,包括神经认知和神经内分泌功能障碍、耳毒性以及继发性恶性肿瘤,这些对患者、其家庭和医疗保健系统具有长期影响。为解决这一临床缺陷,迫切需要开发和实施新的治疗模式,以提高总生存结局并降低与当前疗法相关的发病率。
近年来,免疫检查点抑制剂(ICIs),如PD-1、PD-L1和CTLA-4抑制剂,提供了替代性的癌症治疗,并在成人肿瘤的亚组中显示出深远的临床生存获益。此外,新出现的证据表明,传统(化疗、放疗)和分子靶向治疗除了细胞内在和遗传机制外,还可能具有免疫调节作用。这些对免疫系统的影响部分被认为是由于增加了肿瘤相关抗原的表达并促进了淋巴细胞浸润,这一过程可以将免疫惰性的肿瘤转变为活跃的肿瘤。由于其在成人肿瘤中的成功,ICIs被认为提供了一个有吸引力的机会,可以利用儿童自身的免疫系统靶向PBTs,从而降低年轻患者手术切除、放疗和化疗的发病率以及对神经元成熟的潜在干扰。不幸的是,除了少数例外,单药免疫检查点阻断剂的儿童试验早期结果令人失望。因此,如果ICIs要在PBT治疗中发挥作用,可能需要与其他药物进行联合治疗。
PBTs中ICI治疗的一个挑战是与成人肿瘤相比,其突变负荷较低,导致可触发免疫反应的新抗原较少。此外,肿瘤细胞上MHC表达的下调导致抗原呈递不良,据报道这是免疫逃避细胞毒性CD8 T细胞的一种形式。其他因素如细胞因子、趋化因子和免疫抑制细胞,包括调节性T细胞(Tregs)和骨髓来源的抑制性细胞(MDSCs),可以将肿瘤免疫微环境推向惰性的“冷”状态。因此,复杂的免疫逃避机制可能导致肿瘤微环境(TME)内淋巴细胞浸润减少,并加剧对ICIs的免疫反应降低。
免疫启动是增强PBTs对ICI反应的一个有前途的策略。DNA甲基转移酶抑制剂(DNMTi),如阿扎胞苷(AZA)和5-氮杂-2'-脱氧胞苷(地西他滨,DAC),就是此类药物,已在其他肿瘤类型中显示出通过整体DNA低甲基化诱导新抗原表达来促进免疫启动反应。骨髓增生异常综合征和胶质瘤的临床前研究已证明DAC通过增加T淋巴细胞浸润发挥免疫调节剂的作用。在表达人乳头瘤病毒16的小鼠肿瘤模型中,DAC联合组蛋白去乙酰酶抑制剂治疗触发了MHC I表达、抗原处理的表观遗传激活,并增加了对细胞毒性T细胞裂解的敏感性。
考虑到这些信息,并为了解决儿科患者对ICIs缺乏反应的问题,我们评估了DNMTi对人和小鼠PBT肿瘤模型的影响,并研究了DAC治疗与PD-1检查点抑制的组合是否可以提高代表各种PBT分子类型的多种同基因小鼠模型的生存期。




