手术会刺激胶质瘤生长或恶化吗?
一次常规的体检,竟然在脑子里查出了脑肿瘤!到底要不要手术?
这个问题对于已经出现症状的患者来说,手术的紧迫和重要显而易见。然而对于无症状早期发现的低级别胶质瘤患者,则是一个让他们无比困惑的问题——手术会刺激肿瘤生长吗?会让原本低级别的胶质瘤恶化吗?怕如果手术了反而刺激肿瘤生长了怎么办?还不如不要刺激肿瘤进行保守观察?事实真的如此吗?
当低级别胶质瘤较小时,或症状轻微时,究竟是尽早还是延迟手术,确实存在争议,争议的归因主要还是在于手术效果和手术并发症的平衡。但至今没有任何一项研究表明尽早手术会刺激肿瘤生长。事实上,很多研究者倾向于在确诊为LGG后,做顺利范围内的较大切除能够提高患者的生存期。
对于低级别胶质瘤早期手术,国际临床研究情况有哪些成果?低级别胶质瘤治疗时机和治疗手段又该如何抉择?一起来看今天的INC神外科普系列精彩交流。
INC胶质瘤专家领衔欧美四大神外中心联合研究揭示:
早期手术对无症状低级别胶质瘤的总体生存益处
在目前的文献中,偶发性低级别胶质瘤(弥漫性低级别胶质瘤)的最佳治疗方案一直存在争议,文献记载也很少,主要是由于偶发性低级别胶质瘤的少见和长期随访的困难。为了克服这一局限,采用了多中心研究方法。在这个临床环境中,重要的问题出现了:偶发性低级别胶质瘤是静态病变吗?哪一种是较好的治疗方法,是“观望”还是早期手术?

美国神经外科学院主席(2015)
美国神经外科医师联合会主席(2012)
旧金山加利福尼亚大学神经外科系教授兼主席(1997-至今)
旧金山加利福尼亚大学Helen Diller家庭综合癌症中心名誉教授
脑肿瘤外科项目主任
神经外科研究中心组脑瘤研究中心主任
美国神经外科医师协会董事会(2007-2010)
神经肿瘤学会主席(1997-1999)
INC旗下组织世界神经外科顾问团成员、美国神经外科学会主席Mitchel Berger教授联合多位教授,基于从美国、法国、意大利三个国家,四个专门的神经肿瘤学中心收集临床数据,INC旗下组织世界神经外科顾问团成员、美国神经外科学会主席Mitchel Berger教授联合多位教授,基于从美国、法国、意大利三个国家,四个专门的神经肿瘤学中心收集临床数据,以确定影响早期接受无症状LGG手术的患者的预后和存活率的因素。研究发现:对于无症状低级别胶质瘤患者而言,早期手术是顺利的,并且正在成为好转无症状患者生存预后的最佳临床选择。

论文截图
在这项研究中,基于外科偶发性低级别胶质瘤的较大队列,10年估计总存活率(OS)为93.2%,这一结果明显高于弥漫性低级别胶质瘤的OS。术前肿瘤体积是OS的独自评估因子,且与切除范围(EOR)呈负相关。肿瘤复发延迟主要受早期手术影响。在随访期间,38.73%的患者检测到肿瘤复发,强调偶发性低级别胶质瘤不能被认为是静态病变,而是缓慢发展的肿瘤,因此较大地支持了早期手术的重要性。
现代文献中也越来越多的数据支持较大切除对总生存率的影响。因此,手术是目前优选的治疗方法。手术主张保留患者神经功能状态下顺利、较大范围地切除肿瘤。
研究方法
作者分析了来自欧美4个肿瘤外科中心的267名接受手术治疗的无症状LGG成人患者的数据。时间段为1998年12月至2019年6月。当因和肿瘤无关的原因偶然发现胶质瘤时,所选病例被定义为无症状LGG,如创伤、无相关占位效应的头痛、其他神经或神经外科检查。进行单变量和多变量分析以确定总生存(OS)和肿瘤复发(TR)的评估因子。
患者纳入标准:
患者年龄>18岁;
既往无手术经历;
幕上半球位置;
术前无化疗或放疗;
从初期诊断到手术均未出现与肿瘤相关的临床症状(如癫痫);
组织病理学诊断为国际卫生组织(WHO)II级胶质瘤;
基于3D T2-FLAIR加权MRI序列,客观评估术前肿瘤体积和DICOM格式MRI图像的EOR;
术后神经学和临床状态数据的可用性。
作者收集的数据包括年龄、性别、神经症状、神经影像学表现(EOR)、患者临床术后结果和分子特征。术前、术后出院时和术后6个月进行神经系统检查。通过随访与运动、感觉、视觉和语言功能相关的新发缺陷来确定神经系统并发症发生率。肿瘤体积通过3D FLAIR序列计算。
数据结果
研究人群的基线人口学、临床、组织学和放射学特征总结如表1。术后容积数据和分子分类数据分别为258例和232例。
▼表1研究人群的基线特征:研究人群的特征用均值±标准差或中位数或相对百分比表示。
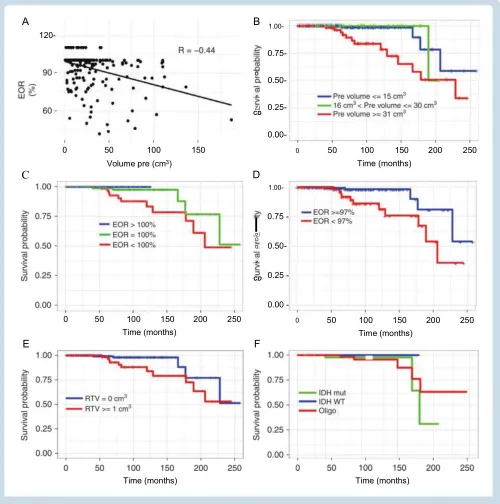
▼图1(A)显示术前肿瘤体积与EOR呈负相关的曲线图(rs=-0.44,P<0.001)。术前较高的肿瘤体积值表明肿瘤有更大的弥漫性生长模式,因此不能切除。(B)偶发性低级别胶质瘤组按术前肿瘤体积分层(HR=1.02;95%CI=1.01~1.03;P=0.001)。(C)偶发性低级别胶质瘤组OS按EOR分层(HR=0.97;95%Cl=0.94~1.0;P=0.037)。行额上切除术的患者无死亡事件发生。(D)偶发性低级别胶质瘤中的OS根据EOR分界值能够对OS组和低风险OS组进行分层(HR=4.09;95%Cl=1.41-11.9;P=0.01)。(E)OS按术后RTV分层(HR=2.93[95%CI 1.00~8.60],P=0.05)。(F)OS根据世卫组织定义的类别分层。属于IDH-WT亚组的患者中没有死亡病例。IDH-Mt偶发性低级别胶质瘤与IDH-Mt/1p19q密码子偶发性低级别胶质瘤之间无生存益处(P=2;HR=2;95%CI=0.74~5.43)。
研究结论
早期手术正在成为好转无症状患者生存预后的最佳临床选择
这项多中心研究将客观肿瘤体积数据与手术结果相结合,证实了早期手术对无症状LGG治疗的临床重要性。这是迄今为止较大样本的无症状LGG治疗策略分析。结果表明对于无症状LGG患者而言,早期手术是顺利的,并且正在成为好转无症状患者生存预后的最佳临床选择。
早手术会刺激胶质瘤生长或恶化吗?
低级别胶质瘤治疗时机和手段如何把握?
无症状真的就是一点症状都没有吗?很多病人发现低级别胶质瘤时,往往觉得没有什么明显症状,认为疾病不重。然而经过认真检查,发现百分之三十到百分之五十的“无症状病人”存在认知功能障碍,这也从另一方面说明低级别胶质瘤不能等待观察。如果等神经损伤加重或出现新损伤再治疗,造成的结果就难以弥补了。当然前提是手术治疗的代价不会比观察等待的代价高。
治疗时机
关于治疗时机,很多医生可能会建议低级别胶质瘤保守治疗,这并不代表肿瘤不会进展,千万不能掉以轻心。因为低级别胶质瘤,通常处于非活动状态或者生长速度缓慢,但也有部分恶化成高级别胶质瘤的情况。所以我们一直强调,早诊断、早规范治疗,可以明显提高胶质瘤的治疗效果,好转患者的预后。
治疗手段
关于胶质瘤的治疗,国内外指南都指出:应该以手术为主,放化疗为辅。很多患者都会来问,国际上有没有什么新技术?我们都会反复跟他们强调国内外指南的,胶质瘤一线治疗手段,一直都是手术。根据手术切除程度、病理结果,和基因分析等因素,来制定后续的放化疗方案。很多新技术,比如说:溶瘤病毒、120万一针的CAR-T治疗,还停留在临床试验阶段,而且只针对部分恶性脑胶质瘤,还需要大量患者在临床上的长期观察。




