在全球范围内,儿童死亡的第二大原因是癌症。随着白血病管理水平的提升,脑肿瘤现已成为儿童期癌症相关死亡的最常见病因。值得注意的是,低级别胶质瘤是儿童最常见的脑肿瘤,约占儿童脑肿瘤的30%-40%。当患者出现梗阻性脑积水、难治性癫痫或明显症状时,家庭通常首先寻求神经外科诊疗意见。因此,神经外科医生有必要参与多学科团队讨论,以制定这些患者的最佳管理方案。
在规模最大的儿童脑肿瘤观察性研究之一中,Wisoff等人证实无论亚型如何,高达80%的低级别胶质瘤患儿可预期存活十年。在神经外科作为专业学科的第一个世纪里,低级别胶质瘤的完全切除术始终为患者提供最佳的治愈机会。然而,在许多情况下,肿瘤可能在手术难以切除的区域生长。当全切除不可行时,对于剩余肿瘤的助治疗策略有哪些?虽然传统化疗和放射治疗长期以来一直是低级别胶质瘤辅助治疗的支柱,但新兴技术和疗法正在迅速改变这类疾病的诊疗格局。高难胶质瘤手术案例可点击阅读:【INC巴特朗菲教授】案例集锦
影像学进展
在经验丰富的神经影像科医师手中,神经影像学技术进步使得超过90%的低级别胶质瘤病例能够在术前获得诊断。此外,现代磁共振成像序列可帮助神经外科医师判断肿瘤是推挤还是浸润正常脑组织结构。功能神经影像学还能确定低级别胶质瘤与相邻语言、运动或感觉皮质之间的界面关系。弥散张量纤维束成像可鉴别肿瘤的浸润性与融合性特征,并显示功能连接的移位情况。高场强术中磁共振成像技术使我们实现全切除或最大安全切除的可能性提高了一倍,同时降低了神经功能损伤风险。
分子分型
2021年6月29日,第五版世界卫生组织(WHO)中枢神经系统(CNS)肿瘤分类(WHO CNS5)最近发布,并刊发在欧洲神经肿瘤协会EANO旗下的神经肿瘤专刊Neuro-Oncology。这是继在2016年WHO中枢神经系统肿瘤更新首次将分子数据与组织学结合起来对中枢神经系统肿瘤进行第二次分类更新。WHO CNS5的变化将肿瘤分为更多生物学和分子定义的病理类型,具有更好的疾病自然史特征,并引入了新的肿瘤类型和亚型,尤其是在儿童人群中。这些更新的分类将使临床医生能够更好地了解特定CNS肿瘤患者的预后和更好治疗,它还将有利于更多同质化的患者群体参与临床试验,促进对新疗法的评估。
2021
新版脑胶质瘤分类
表:2021年中枢神经系统WHO分类(暂定分类用斜体字标示)

新型放射治疗技术
数十年来,放射治疗已被用于胶质瘤术后辅助治疗。早期采用对穿射野的光子治疗虽能实现较好的肿瘤控制,但代价是辐射副作用波及大范围正常脑组织及周围结构。考虑到大多数低级别肿瘤患者生存期较长,恶性转化与继发肿瘤成为其长期生存过程中的重要隐患。随着磁共振引导的三维适形放疗技术发展,更精准的光子投照在提高正常组织保护的同时,显著改善了患者生活质量,并降低了继发肿瘤风险。近年来,质子治疗优势凸显,碳离子治疗作为新兴技术,与质子治疗类似具备布拉格峰优化特性,其能量沉积曲线较质子更为陡峭。目前全球已有十余个中心正开展该技术治疗多种肿瘤的临床研究。
立体定向近距离治疗是通过植入放射性同位素粒子在肿瘤局部实施放射治疗。从历史沿革看,该治疗模式虽具有明确的疗效证据,但在现代医疗背景下已较少使用,这主要得益于通过非手术方式实现更精准放射治疗的能力提升。
聚焦超声
聚焦超声技术在低级别胶质瘤治疗中一个极具潜力的应用方向,是其低强度聚焦超声开放血脑屏障的能力。该技术不会导致热消融或不可逆的组织损伤,而是通过将循环微泡与低强度超声脉冲相结合,将能量聚焦于血管系统,实现血脑屏障的暂时性局部开放,从而增强大分子物质的渗透性。
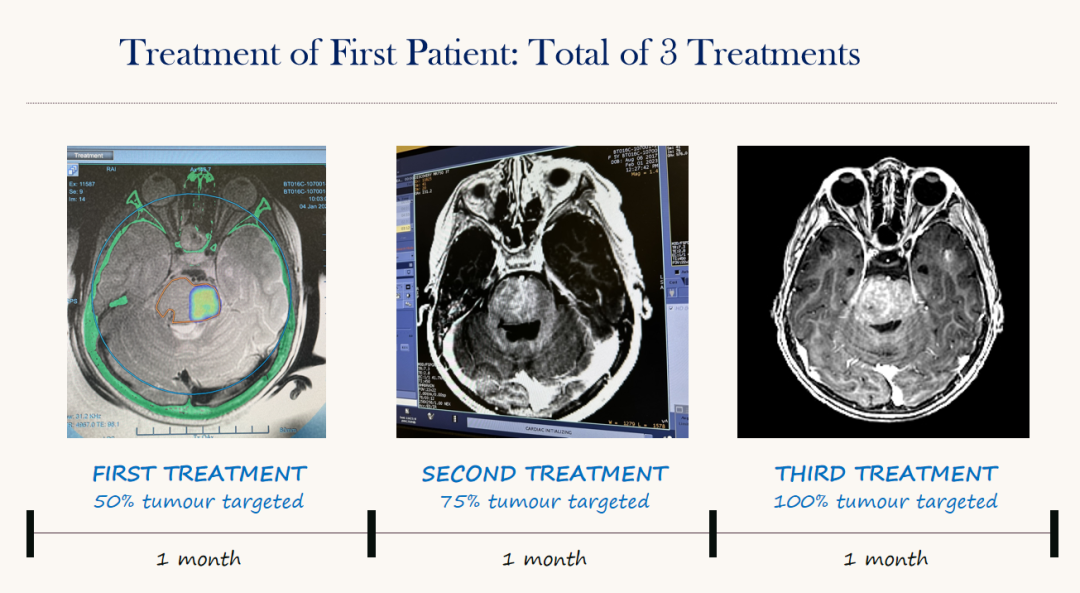
2023年1月10日,James T.Rutka教授所在的加拿大多伦多大学儿童医院(SickKids)官网发布他们已完成世界首例磁共振引导聚焦超声(MRgFUS)为儿童脑肿瘤提供化疗。作为儿童肿瘤安全性和可行性临床试验的一部分,首例儿科患者最近成功地接受了该手术。点击阅读了解:对话胶质瘤突破性技术研发者:如何突破血脑屏障,将化疗药物精准送达脑干?
激光间质热疗LITT
激光间质热疗是近年来用于治疗脑肿瘤的新型手术技术之一。LITT是一种MRI磁共振成像引导下的经皮微创手术,神经外科医生可以清晰地识别癫痫病灶或肿瘤与周围健康脑组织的位置关系,进而制定精确的手术路径。手术过程首先需要在患部头皮上切一个约2-4mm宽的小切口,之后在其中插入激光光纤探头,最后将探头引导到病灶目标所在的位置,利用脉冲激光消融或烧掉肿瘤及病变组织即可。
首例应用激光间质热疗治疗儿童患者的病例报告发表于2011年。尽管已过去十余年,相较于成人患者,关于儿童脑肿瘤激光间质热疗治疗的文献仍相对有限。成人研究主要集中于高级别胶质瘤、转移瘤及放射性坏死。初步研究显示,激光间质热疗在疾病控制方面展现出良好前景,且围手术期并发症发生率相对较低。
INC旗下世界神经外科顾问团(WANG)专家成员、世界神经外科学院前主席James Rutka教授还曾总结了这项技术的三个关键要素:立体定向方法,将激光探针精确定位在治疗目标内;手术激光系统随时间变化的热组织消融;MRI热像仪可实时监测温度变化和组织破坏。

Rutka教授在INC年会上展示的LITT相关文献资料

新兴化疗试验
尽管聚焦超声和激光间质热疗为微创消融提供了诱人前景,新兴化疗试验正在探索新治疗方案在儿童低级别胶质瘤治疗中的作用。化疗历来是手术需要系统治疗患者的主要治疗手段,也是无法切除或进展性肿瘤患者的一线治疗。公认的一线方案包括长春新碱联合卡铂方案、硫鸟嘌呤-丙卡巴肼-洛莫司汀-长春新碱联合方案以及长春花碱或卡铂单药治疗。这些方案的研究显示5年总生存率在70%至95%之间,但无进展生存率仍较低,约为45%-55%。尽管具有合理的控制率,标准化疗方案伴随多种毒性,包括骨髓抑制、周围神经病变、过敏反应、电解质紊乱、继发恶性肿瘤及肝肾功能异常。约50%的儿童患者因这些方案的毒副作用需更换二线化疗方案。
靶向治疗
肿瘤(包括成人和儿童)分子分型的新时代为儿童低级别胶质瘤提供了更好的治疗选择前景。目前研究的通路主要是MAPK/ERK和mTOR通路。当前的主要挑战聚焦于靶向治疗作为初始治疗或常规治疗失败后二线方案的疗效,同时需评估不同治疗方案及组合的安全性和监测潜在副作用。尽管神经影像学显示对靶向治疗有鼓舞人心的反应,但一旦停止治疗,肿瘤再生长存在公认的反弹效应。因此,接受这些药物治疗的患者必须参与能够记录长期副作用和疗效的临床试验方案。将靶向治疗用作一线治疗目前仍属个案报告。
目前针对儿童低级别胶质瘤的靶向治疗试验包括BRAF抑制剂、MEK抑制剂、mTOR抑制剂和FGFR抑制剂。在第18届儿童神经肿瘤学国际研讨会(ISPNO)上,James T.Rutka教授曾发表“靶向BRAF抑制治疗BRAF V600E儿童胶质瘤的疗效”研究成果,为后续BRAF V600突变胶质瘤的治疗及预后提供参考。

结论
对于大多数诊断为低级别胶质瘤的患者,十年生存几率超过80%。目前,对于适合接受最大安全手术切除的患者,这仍是治愈的最佳机会。神经影像学和分子谱分析技术的快速发展,为手术无法治愈的低级别胶质瘤患者(如视路胶质瘤、弥漫性皮层肿瘤或弥漫性中线肿瘤)带来了有前景的替代治疗方案。个体肿瘤的分子谱分析提供了比传统组织病理学更客观、更具预测性和更精确的信息,使得获取每位患者肿瘤组织的重要性变得至关重要。尽管未来可能实现仅凭影像学或仅通过活检来诊断和治疗低级别胶质瘤,但目前,在多学科团队里,这些肿瘤的治疗仍主要依靠神经外科,即手术手段。




