现代神经外科手术之父哈维·库欣(Harvey Cushing)把颅咽管瘤称为颅内较可怕的肿瘤。尽管颅咽管瘤的组织病理学是良性的,但它却具有恶性肿瘤的生长方式,随着肿瘤的不断生长会不可避免地侵占和包围视神经交叉、垂体柄、动脉环、脑干、下丘脑、三脑室、额叶、颞叶等结构、造成多种各样的神经功能损害,临床症状表现多样。
肿瘤全切并保留神经功能是颅咽管瘤治疗的最终目标,是获得更高的没有复发生存率和保留的生活质量。对于大多数符合适应症的患者而言,内窥镜经鼻入路可达成等同或优于经颅入路的效果,由于其侵入性较小,可能会好转视力和缩短术后住院时间。

图1。颅咽管瘤的位置与表面标志的关系。注意经鼻内镜可以增加沿肿瘤长轴斜角的手术路径。与经颅路径相比,大多数肿瘤是在视交叉后占位,理想的是通过该路径暴露。
鼻内窥镜手术起源于颅底中线,通常位于视交叉后间隙,视交叉腹侧 (图1),并允许直接的暴露他们的长轴通过内镜鼻内的方法,这样就不需要脑牵拉或光学仪器,从而降低与经颅入路相关的脑牵拉相关损伤风险。
术前注意事项
手术适用于引起神经功能缺损、垂体功能障碍或梗阻性脑积水或以及在连续影像上有生长的颅咽管瘤病变。评估还包括神经眼科检查,特别注意视野,内分泌检查,以及颅脑磁共振的动态观察。
医源性下丘脑损伤通常是由于过于激进地切除附着在下丘脑上的肿瘤引起的。下丘脑的损伤会导致暴饮暴食,随后导致病态肥胖以及认知障碍,这在儿童中值得关注。在进行任何颅咽管瘤手术之前,应根据下丘脑和漏斗肿瘤受累程度,制定次全切除与全切除的方案。一个顺利的次全切除术优于伴有下丘脑损伤的全切除术。术前应与患者和家属详细讨论术中可能出现的情况,是涉及到牺牲垂体柄以促进肿瘤全切除术这将引起全垂体功能减退。内窥镜下经鼻入路较适合于没有颈动脉分叉处、血管包裹或多个夹层位置的外侧延伸的鞍区和鞍上颅咽管瘤。
全身麻醉诱导后,常规腰椎脑脊液引流,然后在手术期间夹紧引流管。如果需要,引流管可用于鞘内注射荧光素。患者的头部可以放置在环形支架上,或用硬针固定,颈部略微伸展,头部略高于心脏水平。采用术前CT和MRI记录无框架立体定向神经导航。需准备一个筋膜供区用于颅底重建。常规鼻粘膜准备;术前使用抗生素和应激剂量的甲基强的松龙。手术入路-鼻通道的暴露
首先将带血管的鼻中隔皮瓣抬高。将皮瓣的黏膜侧移入鼻咽部,直到肿瘤完全切除,要注意防止蒂扭转和由此造成的缺血。术中,一名外科医生双手工作,另一名外科医生操作内窥镜,使用动态可视化技术促进对手术区域的三维视觉。另一种选择是使用内窥镜支架技术,手术的初始阶段包括双侧中、下鼻甲的侧移,确定蝶窦口,进行后中隔切除术,扩大蝶窦切开术,切除蝶黏膜,进行部分后筛窦切除术,在蝶窦内钻取骨分隔。中鼻甲可以从一侧切除,以容纳内窥镜,以防止其干扰仪器操作,但一般可以保留中鼻甲。在随后的暴露和随后的切除步骤中,较好使用30°角的内窥镜,这样内窥镜的可以在手术器械的工作区域之外不占用术野同时保持足够的可视性。
蝶骨切开术对于手术的其余部分是很重要的,因为它可使在交叉上方的深度手术视野中有更大的通道和操作器械的自由度,并将器械/内窥镜碰撞的可能性降到较低。如果在0°镜下看不到两侧颈内动脉凹陷,则外侧暴露不足。
手术通道的外侧面受限于鼻甲骨,而不是蝶骨前壁的残余物。后筛窦切除术可充分暴露蝶窦平面,虽然病变可能不会延伸到这里,但这种手术方式扩大了手术通道,扩大了手术角度,并防止悬垂的骨头妨碍了器械的操作和组织的暴露。完整切除蝶窦粘膜可防止术后粘液囊肿的形成,同时为后续手术步骤提供了重要的骨性标志,也为带蒂鼻中隔皮瓣的粘连提供必要的骨基质。利用高速金刚石钻头(或超声骨刮匙)去除蝶鞍、鞍结节和蝶鞍平面后半部的骨头,骨切除从侧面延伸到内侧视颈动脉隐窝(图2)。用钻头将骨头变薄,然后用骨钳取出。当钻过颈动脉内侧隐窝时,要进行大量的冲洗,以防止视神经受到热损伤。静脉出血是骨磨除时经常遇到的情况,但即使是激烈的静脉出血,用凝胶泡沫填料和轻微的压力通常很容易得到控制。

图2。沿碟后壁的骨标志物暴露。骨从侧面移到视颈动脉内凹处水平,下至鞍前壁的一半左右以保护垂体,上方至蝶骨平面后部水平。
沿蝶骨平面的骨性开口不需要扩大,因为大部分的解剖是在交叉下进行的。然而,如果肿瘤明显延伸至交叉之上,需要经终板入路,则可能需要沿平面进行额外的骨切除。导航证实充分的骨切除后,凝固上海绵窦,硬脑膜以十字交叉的方式打开(图3)。硬脑膜边缘电凝回缩,以增加视野。也可以切除硬脑膜边缘以扩大手术通道。在开放硬脑膜之前,常规使用微多普勒超声探测血管以避免损伤颈内动脉,是当其近端床突部分向内侧走行时。

图3。请注意,我们更倾向于从颈动脉外侧切除骨,以便通过轻轻地移动这些血管结构,更便于操作角度。硬脑膜以十字交叉的方式打开鞍区。超声引导下硬脑膜切口可避免损伤ICAs。
肿瘤切除中尽可能早、尽可能长时间地保留动脉,直到确定完全切除将需要牺牲垂体功能为止。然后切开包膜,囊性肿瘤可引流或使用环形刮匙清除实体瘤的内部。(图4)。

图4。当打开硬脑膜时,可见的结构可能是蛛网膜和肿瘤包膜。术者应保持耐心并为肿瘤减压,因为这样操作可以减少肿瘤空间并识别周围的脑血管结构。过度的去骨可能会增加术后的风险
一旦肿瘤被切除,外科医生可以从视神经交叉的下侧将其囊壁切开,同时小心地保留供应交叉的穿支(图5)。这种穿孔器的损伤是颅咽管瘤手术后视力下降的主要原因。随后将包膜打开得更大,进一步切除肿瘤(图6)。

图5。切除肿瘤后,将包膜从视交叉的下表面剥离,注意防止对该区域的血管造成伤害

图6。穿孔器的损伤是颅咽管瘤手术后视力下降的主要原因。随后将包膜打开得更大,进一步切除肿瘤(图6)。一旦肿瘤部分脱离视神经交叉,就将包膜打开得更大,进一步进行肿瘤内部减容。环状刮匙用于切除肿瘤的实性钙化部分并排出相关囊肿
然后利用足够的牵引力将包膜移动并向内侧切开,以拉伸蛛网膜粘连而不撕裂小血管(图7)。这些蛛网膜粘连被锐利的切开,进入颈动脉池,然后精确的跟踪ICA,同时小心地保护上垂体动脉和其他小的穿支血管。以这种方式,沿着肿瘤两侧进行解剖。

图7。当肿瘤向内侧移动时,进入颈动脉池。蛛网膜粘连被拉长,然后明显分开。沿着肿瘤两侧的ICA进行解剖。肿瘤和交叉的垂体上动脉的分支被识别出来,后者被保留。
继续进行周向解剖,并从视神经交叉的下侧面被进一步解剖肿瘤(图8)。随着解剖的进行,肿瘤从三脑室底部脱离(图9)。这种手术要小心,特别是在肿瘤严重侵犯三脑室的情况下。在许多情况下,三脑室底部不完整,剥离物被带进脑室,肿瘤从侧壁和上壁切除。必要时,可留下部分肿瘤,以防止下丘脑核的牵引损伤。我们可以在切除其他部分的肿瘤后再切除三脑室部分的肿瘤。在从下丘脑壁切除肿瘤的过程中,这种方法提供了更广泛的视野。

图8。继续围绕着肿瘤包膜进行锐性分离,肿瘤包膜从视神经交叉的下方被剥离出来

图9。从三脑室壁切除肿瘤。要小心避免对肿瘤的过度牵引,因为这可能会对下丘脑造成伤害。倾斜的内窥镜可以仔细检查脑室壁和下丘脑。
一旦肿瘤从侧脑室中剥离出来后,术者的注意力需转移到肿瘤下方,将其从鞍膈和脑下垂体分离。如果肿瘤向下延伸到鞍区,鞍膈需切断。然后评估垂体柄,垂体柄的处理需要术中详细检查评估对其保存还是牺牲,进行明智的选择(图10)。理想情况下,全部的努力都是为了保留垂体柄,然而,如果术中有全切的可行性,我们建议横切垂体柄以达到完全切除。

图10。肿瘤从蝶鞍鞍膈处切除,并对垂体柄进行评估
处理完垂体柄后,肿瘤仍常系于乳头体或基底动脉及其分支的后方,在这个阶段,切勿牵拉肿瘤。迅速、耐心地将肿瘤从乳头体、视神经束、Liliequist膜、大脑后动脉、后交通动脉和丘脑穿支动脉中剥离(图11),最后从垂体柄上剥离(图12),最后从垂体柄中切除(图12)。然后用30°、45°、70°内窥镜对瘤腔内进行完全探查,评估出血情况,检查三脑室是否有残余肿瘤(图13)。

图11:切除乳头体中的肿瘤,切除时避免任意牵引肿瘤。肿瘤从视神经束和基底动脉的分支中轻柔得剥离

图12:用弯角显微剪将肿瘤从垂体柄分离开肿瘤

图13。瘤腔中肿瘤清除完后,检查三脑室的出血情况和是否有残留肿瘤,注意基底动脉和大脑后动脉。
使用45°内窥镜分离暴露肿瘤的外侧扩展区。带角度的内窥镜和解剖器械的使用从根本上扩大了内镜经鼻手术和相关手术路径的范围,以切除大型颅咽管瘤,以前这一方法并不被认可。在颅咽管瘤切除术后,建议用水大量冲洗,因为肿瘤残留物会损害正常的神经结构和引发化学性脑膜炎。
并发症
●额叶/颞叶或下丘脑受伤则会导致认知和心理异常。
2. 脑脊液漏和鼻出血是较常见入路特异性并发症。脑脊液泄漏自从扩大内窥镜内鼻入路引入以来一直是一个严重的问题,但是随着颅底重建技术的改进(特别是鼻中隔皮瓣重建的广泛采用),最近的一些报道显示脑脊液泄漏率已经下降到0%。在大多数情况中,术后脑脊液漏的发生率在10% - 15%左右。
3.术后较常见的并发症是尿崩症。42%-64%的尿崩症患者术前常有尿崩症,术后病情恶化,但部分患者术后尿崩症常有随着时间得到好转。
4.垂体前叶激素调节失调也很常见,28%-46%的患者术后出现垂体轴功能障碍,大约2%-7%的患者出现术后视力恶化。
5. 由下丘脑损伤引起的饮食过度可能导致患者病态肥胖,这是颅咽管瘤切除术后的一个常见的并发症,是在儿童之中。
INC国际专家内镜手术案例
INC之德国Henry W.S. Schroeder(施罗德)教授曾在论文中交流了这样一则病例,这位61岁的男性患者有6个月的进行性智力退化史,包括短期记忆减退。入院前10天,患者出现意识障碍、定向障碍及膀胱功能障碍。内分泌学检查显示为尿失禁和尿崩症,有患典型的肾上腺皮质功能减退症Addison病的风险,施罗德教授为其行内镜下颅咽管瘤切除手术。
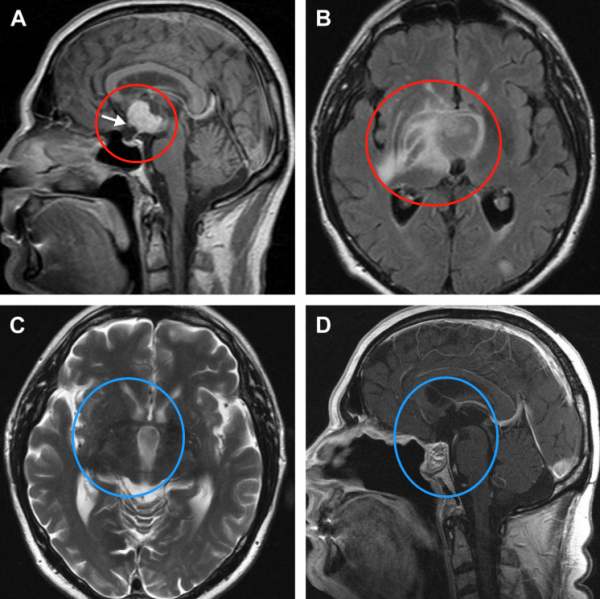
图14。鞍上增强MRI显示,肿瘤延伸至三脑室,有实性成分(a)。视神经交叉向前移位(箭头)。垂体和蝶鞍似乎正常。由于T2病灶周围水肿和反转恢复图像液体衰减并右侧基底神经节外侧延伸,怀疑下丘脑侵犯(B)。施罗德教授在内镜下行全切术,包括已被肿瘤浸润损害的部分垂体柄。术后2年MRI未见肿瘤复发(C, D)。水肿完全消退(C)。图像(D)也显示鼻中隔皮瓣重建颅底。

图15为打开蝶骨的阶段。(A)蝶鞍底(SF)和蝶面(P)在蝶腔内的蛋壳样钻孔。(B)去除薄骨层。(C)全骨切除后显露硬脑膜的全景图,并标记视神经(ON)、颈动脉(CA)和海绵窦内上方(SIS[星号])的位置。(D)鞍上间隙硬脑膜开口。(E)海绵窦内上方凝固。(F)海绵窦内上方截面。

图16为硬膜内操作阶段。(A)锐性分离蛛网膜。(B)暴露鞍膈上区。可见垂体柄(PS)、后交通动脉(PCoA)、垂体上动脉(SHA)、视神经(OT)和肿瘤(T)。(C)切除肿瘤。双手用抓钳和解剖钳进行囊外剥离。垂体柄向左侧偏。(E)切换到30°内窥镜顺利实现交叉后肿瘤去体积(视交叉[OC])(F)将一大块肿瘤从三脑室移至蝶骨腔。(G)完全切除肿瘤后最后检查三脑室背侧部分(脉络膜丛[CP],缰连合[HC],后连合[PC])。(H)使用45°内窥镜检查三脑室前部(脉络丛(CP),穹窿[F],门室孔(FM)和丘脑间粘合(MI))。
术后这名患者经历了短暂的神志不清,但神志及认知功能恢复很快,而且体重保持稳定。需要激素替代。术后两年颅咽管瘤未复发,水肿完全消退。
施罗德教授认为鼻内窥镜鼻内扩张入路的引入是颅咽管瘤治疗的重要进展,其提高了手术切除率、提供了更佳的术野。特别是在交叉后病变推动交叉前(前置交叉),鼻内入路提供了一个更好的进入病变和减少视觉仪器操作程度的选择。内窥镜提供的全景视图和角度光学使术者可以切除延伸到三脑室的病变,同时避免显微外科中如经终板或经胼胝体入路的“开颅之苦”。但鼻内窥镜鼻内扩张入路手术需要和不断的学习和密集的训练,对术者要求较高,操作难度较大。
后记内镜下经鼻入路切除颅咽管瘤相较于开颅手术有着独特的优势,在切除范围和视力好转方面也可能优于经颅入路,且不会引起脑牵拉引起的组织损伤。而且由于该入路特有的并发症(如脑脊液泄漏和鼻腔并发症)发生率持续下降,因此使用该入路可以使部分颅咽管瘤患者更大获益,但其要求内镜手术的主刀医生拥有高超的操作技巧和丰富的临床经验,以便在术中灵活应变,及时调整手术策略,在确定顺利的前提下提高颅咽管瘤的切除率,以期降低术后复发率。
INC旗下世界神经外科顾问团(World Advisory Neurosurgical Group,WANG)是由国际各发达国家神经外科宗师联合组成的教授集团,其中的专家教授均为世界神经外科联合会(WFNS)及各种国际神经外科学术组织的成员,国际神经外科各大杂志主编,以及神经外科教科书中以其本人名字命名手术方式和解剖结构的教科书级神经外科巨擘。囊括了国际颅底肿瘤手术教授巴特朗菲教授、国际儿童神经外科专家 James T. Rutka 教授、WFNS国际颅底主席Sebastien Froelich教授等神外教授,国内患者可拨打400-029-0925咨询INC国际专家远程邮件或视频咨询,听取一位或多位教授的治疗方案,综合考量后再做决策。
2. Andrew R. Conger,et al.Endoscopic extended transsphenoidal resection ofcraniopharyngiomas: nuances of neurosurgical technique.




