前交通动脉通常限制前半球间的手术暴露方法。尽管已经提议了前交通动脉的分离,有时,这种做法很少实践,并且这种手术操作的标准仍然未知。
来自INC国际神经外科医生集团,现任世界神经外科联合会WFNS教育委员会主席、德国INI国际神经学研究所血管神经外科主任的德国Helmut Bertalanffy(巴特朗菲)教授在其论文《Predicting the necessity of anterior communicating artery division
in the bifrontal basal interhemispheric approach》论文中论述了在双额基底半球间入路中分离前交通动脉的必要性。
方法:该研究连续检查了22名通过双额基底半球根间入路进行了手术以切除各种病理性脑部病变的患者。首先,将肿瘤分为中央和外侧病变。接下来,比较了三个肿瘤参数,每个中心和每个中心都有或没有ACoA部门的案例。外侧病变组分别为:肿瘤体积,肿瘤深度(定义为ACoA与后肿瘤之间的距离边缘)和肿瘤侧倾角(定义为几何肿瘤外侧边缘与矢状正中线之间的夹角)。
结果:在两个中心,肿瘤体积与ACoA划分均无统计学意义(P=0.06)和外侧(P=0.13)病变组。然而,肿瘤深度与ACoA划分显着相关在中央病变组(P=0.01),而在外侧病灶组,肿瘤侧倾角呈显着性与ACoA划分的相关性(P=0.04)。
说明性案例:
案例1:一名没有既往病史的20岁女性突然出现意识紊乱并逐渐恶化的意识,并出现左偏瘫。MRI显示新鲜海绵状血管瘤典型的中脑轴内出血,连续性急性梗阻性脑积水出血。病变位于腹侧中脑中线,体积为10.7立方毫米,深度为42.5毫米和11.6°的肿瘤侧倾角(图3a,b)。去除双额基底半球间出血性病变放置右外部心室引流后3天,该方法成功完成。
皮肤切口和开颅手术后,前半球间裂被分离到前壁。三脑室。为了充分暴露前眼穿过三脑室的脑干,前交通动脉的分离估计在手术期间是有益和必要的。这里的前交通动脉被迷你夹闭塞,随后在保留射孔分支的同时进行了分裂(图4A-C)。接下来,纵向切开椎板,然后三脑室底部在乳头体之间打开,直接导致这种中脑血管畸形游离,切除海绵状血管瘤并取出。以零碎的方式微小的动脉给养器反复出现在病灶和病灶之间的界面处凝结并切开实质组织,血肿和海绵状血管瘤完全去除(图4D-F)。
术后病人的恢复也很顺利。患者的意识和偏瘫迅速好转。脑积水消退,不需要分流放置。病人步行出院,没有3个月后随访的神经或认知功能障碍。术后MRI显示完全切除了轴内血肿和血管病变(图3C,D)。

上图示意术中分离前交通动脉。图A-C表示使用微型夹子,同时保留前交通动脉的射孔支,随后在两者之间进行了分离。图D-F表示切掉薄片后纵向终端,打开在乳头体之间的三脑室底部。裸露的中脑海绵状血管瘤完全去除。Rt,右;Lt,左;A1为A1脑前动脉节段;前A2为A2节段脑动脉

图A和B显示术前MRI影像,被分类为Bcentral病变的出血性中脑海绵状血管瘤。黄色虚线表示肿瘤深度(42.5毫米)。图C、D显示完全清除血管病变后的术后MRI
案例2:这位16岁的男性以前曾通过左侧翼状入路手术切除4岁时的鞍上肿瘤,被咨询至德国INI国际神经学研究所。尽管两个周期的辅助化疗治疗诊断为下丘脑毛细胞星形细胞瘤,肿瘤在随后的几年中很快复发。入院时,患者机敏,但患有泛垂体功能减退和严重的左侧视力障碍,几乎等于这只眼睛失明。术前MRI显示较大肿瘤,占据了延伸到左侧的超上层空间。
海马旁回和侧脑室(图5A、B)。肿瘤体积达68.1 mm3,其深度为44.4毫米,侧面角为21.9°。在这一阶段,手术切除被认为是合理的治疗方式。双冠状皮肤切口,双额颅骨开颅和基底半球间入路是常规进行的。首先,将涉及视交叉的肿瘤切除,在垂体下方发现了垂体柄。前交通动脉和椎板终末逐渐暴露。打开椎板终端可以广泛地进入前三脑室并允许明显减瘤,
充满了该区域的后气管肿瘤部分。后脑基底基底分叉和P1节段动脉。尽管肿瘤已被精心切除,完整保留了下丘脑和后循环血管,前交通动脉意外地被拉伸撕裂。由于无法修复撕裂的前交通动脉,因此决定分离前交通动脉,从而在前交通动脉的两个A2段中维持供血。暂时以下两个A1线段的咬合,前交通动脉被迷你夹夹闭住,随后被分离(图6A-F)。血管的通畅反复受到控制,残留肿瘤的清除容易完成。接近全肿瘤切除和在术中MRI上确认了两个A2血管区域的正常灌注,并记录了这些灌注(图5C、D)。视交叉和视神经束、垂体柄和下丘脑保持原样。术后过程平稳,患者继续进行全垂体功能减退的医学治疗。在随访无其他神经或认知功能障碍。
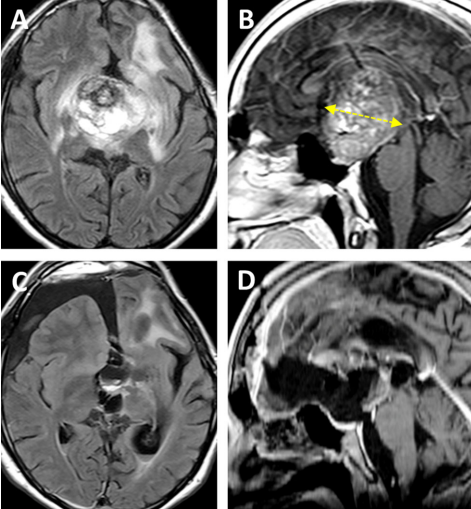
图A、B为术前MRI影像,归类为Bcentral病变的复发性毛细胞星形细胞瘤。
黄色虚线表示肿瘤深度(44.4毫米)。图C、D显示为几乎全切的术后MRI
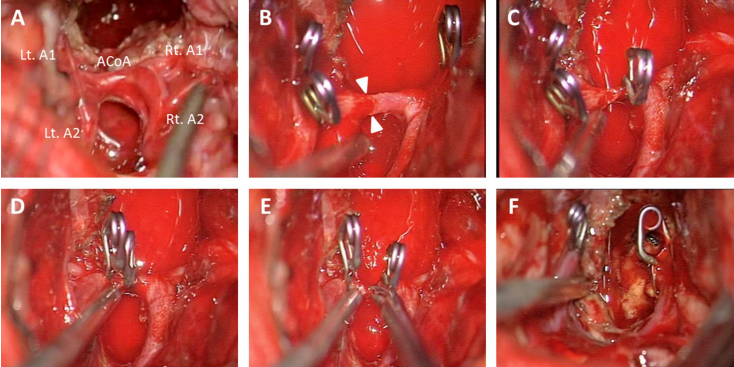
图6表示术中照片分割前交通动脉(ACoA)。由于前交通动脉出乎意料地被割裂了,前路A1节段脑动脉(A1)暂时阻塞流量控制。撕裂点(在白色箭头之间)的前交通动脉被迷你夹闭塞住,剪开,然后进行分割。Rt,右;Lt,左;A2,A2段脑前动脉
结论:
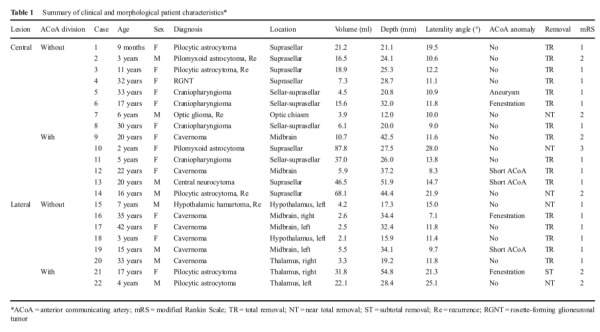
全部患者的临床和形态特征均为总结于表1。十四例患者在中心,八个是外侧病变。在全部22例患者中,有8例(6例和2个有侧部病变的患者)进行了前交通动脉分割,而14名患者(8名有中心病变,6名有侧部病变)做了不需要这种动脉中断。在一名患者中,3毫米偶然发现ACoA动脉瘤,并在切除肿瘤后通过手术夹钳进行治疗(病例5)。16例患者完全切除,5例几乎全部切除(超过肿瘤体积的90%),小计切除(在肿瘤体积的50%到90%之间)1个人。幸运的是,没有与之相关的严重的早期或晚期并发症发生外科手术或ACoA分区。中位数出院时改良的Rankin量表(mRS)评分为2(IQR,1-2)接受ACoA分割且为1的患者(IQR,1-1)在没有动脉中断的患者中。出院时发现ACoA部门和非部门患者之间的mRS评分存在差异(P=1.22)。相反,比较每个组中ACoA分离组和分离组的三种肿瘤特性中央和外侧病变分别导致有趣发现。肿瘤体积与ACoA无关中央(P=0.06)或侧面(P=0.13)划分病变组(表2)。但是,在中央病变组中肿瘤深度与ACoA划分显着相关(P=0.01)(表2),而在外侧病变组中,肿瘤侧倾角与ACoA划分(P=0.04)。
讨论:
在外科手术过程中故意分割ACoA通常能避免保留射孔分支,可以作为主要馈线的ACoA出现漏斗,视交叉和下丘脑前部。此类穿孔的前交通动脉分支可能会受伤引起内分泌功能障碍,认知障碍和精神疾病。此外,将大约60%的ACoA表现出解剖学上的变异,可能并不容易,是对于儿童ACoA细分短不过,有几位作者提到了受控的主要优势。
我们分析了经历了各种组织病理学类型的鞍上病变的患者,通过双额叶基底半球间入路手术,试图确定可以评估前交通动脉分割的必要性。在基底半球间入路狭窄的手术通道中,考虑肿瘤体积和前后及横向范围作为可能影响总肿瘤切除率可能性的基本参数。虽然较小的肿瘤大小显然有利于切除,但较大的肿瘤扩展范围使该区域的手术切除更加困难。特别是肿瘤部位比较深远的,由于前交通动脉通常会阻碍或使显微外科手术暴露复杂化,因此前交通动脉并不容易获得。在此,我们集中了在三种形态肿瘤上的参数,即肿瘤体积、深度和较大
横向范围。
与我们的预期相反,肿瘤体积没有作为评估必要性的适当参数而出现。所谓的中央或侧面的前交通动脉病变组。尽管由于病变不同,平均肿瘤体积的统计差异类型可能会影响我们的分析,在他们的出版物交易中也间接提到。
在颅咽管瘤手术中,有和没有前交通动脉的患者组之间的肿瘤大小没有差异。该报告和我们的结果表明,ACoA分割的必要性可能并不取决于在肿瘤体积上。另一方面,我们的结果表明,可能需要在切除肿瘤之前先将ACoA分开,在所谓的中央病变中(根据本研究)肿瘤深度接近38 mm或超过23度的侧向较大侧向伸展角度,因为我们在当前定义的这个参数
学习。
我们首先想到了测量评估病灶的横向范围。但是,相同的横向位于病灶前方或后方的病灶扩展ACoA关于侧脑后退的必要性可能没有相同的含义。因此,我们倾向于通过测量侧面度来评估病变的侧面度角度。
总而言之,在双额叶基底半球间入路中,前交通动脉可被视为限制或肿瘤后部延伸远时发生阻塞远离ACoA,因此肿瘤深度必不可少。同样,病灶的暴露与半球前裂隙内的横向范围可能会导致对ACoA施加过大的拉伸应力,并且增加意外血管破裂的风险。
因此,侧面度被证明是另一个重要的形态学参数,可以在术前评估成像以帮助评估受控前交通动脉分割的必要性。
总结:
有意和受控的前交通动脉分离可能是双额基底半球间入路手术中的一项有益技术,这可确保手术过程的顺利性,同时能做到全切肿瘤。现在研究确定了两个容易实现的关键因素,评估术前MR成像(肿瘤深度和较大横向范围),这可能有助于评估手术前进行前交通动脉分割的必要性。然而,最终决定是否分割前交通动脉需要在仔细的术中检查后确定,无需在术前进行血管造影就可以在外科手术过程中使用。
参考文献:Helmut Bertalanffy.Predicting the necessity of anterior communicating artery divisionin the bifrontal basal interhemispheric approach.Acta Neurochir(2016)




