松果体区域手术的宝贵经验主要局限于少数有经验的外科医生,并且可能在他们停止执业时失传。如何系统地保存和分析松果体区手术静脉解剖的宝贵实践知识。
INC两大国际大咖William T.Couldwell教授、Tiit Mathiesen教授联合多位专家,以获取经验丰富的外科医生对松果体手术中静脉闭塞后预估风险和个人经验的看法。在126位受邀的神经外科医生中,有40位提交了完整的问卷。关于哪些静脉闭塞后具有高风险和低风险,存在普遍共识。预计牺牲盖伦静脉(83%)、双侧大脑内静脉(69%)和基底静脉(58%)的死亡风险很高。预计牺牲双侧上蚓静脉(13%)和一侧枕内静脉(10%)的死亡风险较低。重要的是,一部分经验丰富的外科医生报告称,牺牲小脑桥静脉(8-13%)存在显着的死亡风险和后果。广泛的术前影像学检查和解剖学研究似乎与更谨慎的风险评估相关。



研究背景:为什么这个问题很重要?
松果体区手术很少见。即使是最有经验的外科医生,这可能不足以全面评估解剖和手术变异的影响。因此收集并系统化经验丰富的神经外科医生在松果体区静脉保留和去除方面的实战经验很重要。
松果体区静脉解剖基础分享
松果体区静脉包括深静脉系统和小脑天幕桥静脉。前者由罗森塔尔基底静脉组成,引流大脑半球外侧部分的血液,在绕脑干外侧走行后与大脑内静脉汇合。两条大脑内静脉在松果体正后方汇合形成盖伦静脉。大脑内静脉在胼胝体下方、尾状核上方走行,引流大脑半球最深部的血液。枕内静脉在引流枕叶内侧部分的血液后,从外侧进入松果体区;上蚓静脉从下方进入该区域,引流小脑上表面部分——这两条静脉均汇入盖伦静脉的近端部分。小脑桥静脉引流小脑上表面,通常分为内侧组和外侧组,并进一步引流入天幕窦或较大的小脑静脉。
传统上,牺牲小脑静脉有助于后颅窝的神经外科入路。有一种隐含的共识,即有些静脉,如盖伦静脉,是不可触碰的,而其他静脉,如岩上静脉,有经验的神经外科医生认为牺牲是安全的。然而,一些病例描述对这一假定的“安全性”提出了挑战,并表明任何静脉牺牲都可能导致死亡。因此,需要更多关于安全性的知识以避免并发症。
120位经验丰富的医生:他们的经验如何?
通常,外科医生表示“首要目标始终是保护静脉系统”,但静脉牺牲的风险评估差异超出预期。对于大脑内静脉、盖伦静脉和基底静脉,普遍共识是绝不故意牺牲。对于闭塞一条枕内静脉、一条或两条上蚓静脉、外侧和内侧桥静脉,多数人同意为改善入路和扩大肿瘤切除范围而故意牺牲。我们发现关于静脉牺牲的风险认知存在两种模式:“通常安全”(死亡风险<10%)和“通常不安全”(死亡风险=/>10%)。对风险的认知似乎因手术经验和自身对松果体手术解剖的研究而异。尽管对实际风险的评估存在差异,但存在共识,即不对预估风险高的静脉(定义为=/>10%)进行主动牺牲。
经验分享:安全VS不安全
通常不安全
大多数外科医生确信牺牲盖伦静脉会带来难以承受的水肿、梗塞和死亡风险;值得注意的是,评估的风险大小呈双峰分布,并且与报告的手术经验相关:最低风险和最高风险分别由经验最少和经验最丰富的外科医生评估。最有经验的外科医生一致认为闭塞一条或两条静脉的预估死亡风险分别为82%和97%。
表4松果体区静脉闭塞单侧或双侧时,预估的梗塞、水肿及死亡风险平均值(N=29)。(包含所有预估风险的中位绝对偏差)
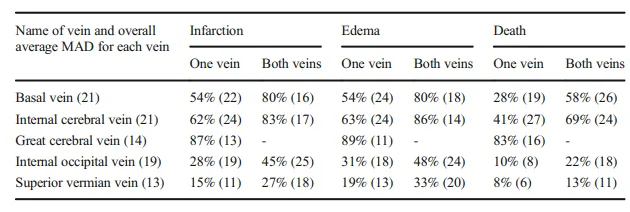
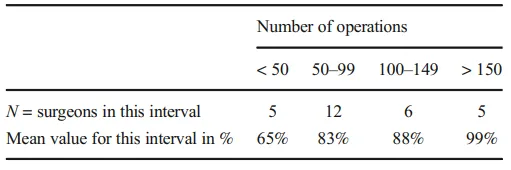
表5基于不同手术经验水平,闭塞单侧或双侧大脑内静脉时预估死亡风险的平均值。

表6基于不同手术经验水平,闭塞大脑大静脉(盖伦静脉)时的预估死亡风险(平均预估风险为83%)
牺牲基底静脉的风险可能较低。它引流大脑外侧部分,可能通过侧裂吻合支形成侧支引流。由于双侧静脉位于相邻脑池的不同部分,意外撕裂后发生双侧闭塞的可能性较小,估计闭塞一条静脉的平均死亡风险为28%;同样,最有经验的外科医生评估的风险比经验较少者更高。
通常安全
枕内静脉通常被认为风险较低,但是经验丰富的外科医生报告了更高的风险评估,并且三分之一的人表示永远不会为了手术入路牺牲枕内静脉。
对上蚓静脉报告的死亡风险评估同样较低。与枕内静脉相比,水肿和梗塞被认为可能性较小,尽管有五位外科医生确实观察到牺牲后发生梗塞或水肿。最有经验的外科医生对上蚓静脉的风险评估往往低于经验较少者:这种模式不同于风险最高的静脉,后者是经验丰富的外科医生评估更高。
一半的外科医生会常规牺牲桥静脉。大多数人从未见过任何临床表现,而25%的外科医生不会牺牲,3位报告了他们在特殊病例中观察到严重并发症。出现的模式是,“通常安全”的静脉在牺牲枕内静脉或上蚓静脉时仍存在有限的(可能<20%)亚临床梗塞和水肿风险,甚至在牺牲通过桥静脉引流的小脑大部分血液时存在严重肿胀和死亡的风险(可能<5%)。风险可能因个体静脉引流解剖模式而异,如果有足够的个体解剖知识,即广泛的影像学检查,或许可以预测。
分歧(MAD)
所有外科医生对盖伦静脉、大脑内静脉和基底静脉的风险评估最高,但评估的风险大小存在差异。最大的分歧(MAD)出现在预估风险低的桥静脉以及预估风险高的基底静脉和大脑内静脉。
关于牺牲桥静脉存在两种不同的态度。
第一种态度存在于评估并发症风险约为零的群体中。这组主要包括经验最少的外科医生,他们可能没有遇到过并发症,因此不预期任何并发症。这组的外科医生可能要么接受一定频率的严重手术并发症,要么没有观察到任何并发症并认为不会发生。这些外科医生相对经验较少的事实支持了第一种解释,即他们自身的观察有限。
第二种评估严重风险在10-20%左右,包含更多有经验的外科医生,可能更多的手术经历包含了罕见并发症的观察。
对风险的不同认知对外科医生的手术指征、入路选择和影像学检查有很大影响。这种差异也影响患者告知,进而影响最终决策。与“高风险静脉”的风险分歧相比,“低风险静脉”的风险差异对患者咨询的影响可能更大。尽管外科医生对基底静脉和大脑内静脉的风险是40%还是85%存在分歧,但一致认为故意牺牲是不可接受的风险。相比之下,<1%和10-20%的死亡风险之间的差异是关键的,因为无论是患者还是外科医生都不会接受择期手术中有10-20%的手术死亡率。因此,大约10%的死亡风险被评估为“低”,而实际手术死亡率很可能远低于5%。
我们注意到风险评估与经验之间存在差异:没有外科医生报告闭塞枕内静脉后出现任何水肿、梗塞或死亡,但闭塞一条枕内静脉的预估死亡风险为10%。这种差异可以解释为应用了“默认”的预防原则,以降低未知的手术风险。正是观察到了这种预防原则,我们才选择将风险手术定义为风险评估>10%的手术,而不是用于事后分析手术风险时定义“高风险”的5%。
术前检查与经验的影响:U型曲线
术前,MRI是非血管性松果体区病变和解剖的首选成像方式。血管成像包括CTA、MRA和DSA。DSA能更好地分析血流、引流和侧支成像,但比MRA和CTA更具侵入性。相比之下,MRA和CTA在地形解剖分辨率方面更优,且不像DSA那样依赖操作者。DSA的辐射暴露显着更高。DSA仍然是金标准,并且是进行高级成像(如3D-DSA重建,可精确多平面显示供血动脉、引流静脉和病理病变的关系)的必要手段。然而,术中成像和导航通常基于术前MRI、CT和DSA,因此,如果要在手术中安全地使用成像,手术解剖学的专业知识是必不可少的。
术前都使用MRI是预期中的一致,但只有75%使用了某种静脉成像。使用CTA和DSA进行术前检查的外科医生更有经验,而经验较少的外科医生则提到MRI血管成像的实用性。我们无法证明是增加的手术经验导致了对CTA和DSA来计划安全手术的需求。有人可能认为,更有经验的外科医生年纪更大,使用的术前检查常规保持不变,尽管有新的成像技术。考虑到所有回复,我们的理解是经验更丰富的外科医生在计划时更广泛地使用成像。静脉解剖知识可能影响手术策略:单侧静脉引流可能促使选择对侧幕下小脑上入路,或者看似危险的桥静脉患者可能采用幕上入路而非小脑上入路。
最有经验者可能见过足够多的病例,形成了第一手的手术实践知识。这种模式可能反映了一种特殊的学习曲线,即最初的谨慎之后是信心和更高的风险接受度,而经验又会缓和这一点,这其实是一条U型学习曲线。
研究结果表明,结合术前影像学检查和解剖学上的深入研究,可以更好地评估风险。交流、分享、减少分歧应能使手术环境更安全,并使实际低风险趋近于0%而非10%。




