一名68岁的女士在过去1至2个月内左眼视力丧失。它与任何疼痛无关。自从两到三个月以来,身体也出现过敏和不自主运动的病史。她的一般体检是正常的。右眼最佳矫正视力为6/24,左眼4米处可视。前段检查显示双眼瞳孔反应迟钝。在眼底检查中,检测到双侧乳头水肿。Ishiara图表的颜色视觉在右眼为5/14,在左眼为2/14。在对抗试验中,右眼和左眼的颞区减少。
相关阅读:5岁视神经胶质瘤小朋友在德国治疗经过
脑部MRI检查发现前交叉颅内视神经增厚,视交叉和后交叉视神经束具有分叶轮廓和弥散信号改变,显示T2W / FLAIR图像上的高信号(图1)。
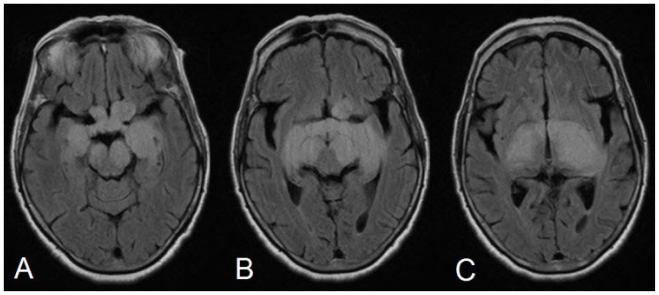
图1
68岁女性患有视神经胶质母细胞瘤。FLAIR(TR -9000ms,TE = 87,TI = 2500)显示具有高信号信号改变的前交叉颅内视神经,交叉和后交叉视神经束的增厚。
在下丘脑,双侧丘脑束(左侧达到室旁区域),双侧近中颞叶,大脑小脑和上中脑,也观察到邻近的大边缘近对称信号改变,在T2W / FLAIR图像上显示高信号(图2)病变在T1W图像上呈低信号至等信号,对扩散图像无明显限制。涉及的结构似乎扩大了。颅内和眶内视神经正常。
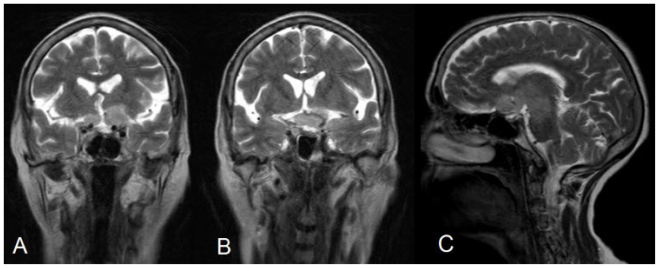
图2
68岁女性患有视神经胶质母细胞瘤。T2W冠状面(TR -4100ms,TE = 91.0 SL -5mm,FOV 173×230)和T2W下垂图像显示下丘脑,双侧丘脑束膜区,双侧近中颞叶,大脑小脑和上中脑的对称高信号信号改变。还注意到庞大的交叉和前交叉神经。
后对比图像(使用20ml的Gadodiamide,OMNISCAN,GE Healthcare)显示出一个小的(14×12mm)异质环,增强了左侧视交叉上方的焦点(图3)。病变的其余部分未显示出显着的增强(图4)。然而,在左颞区观察到微妙的脑膜增强。
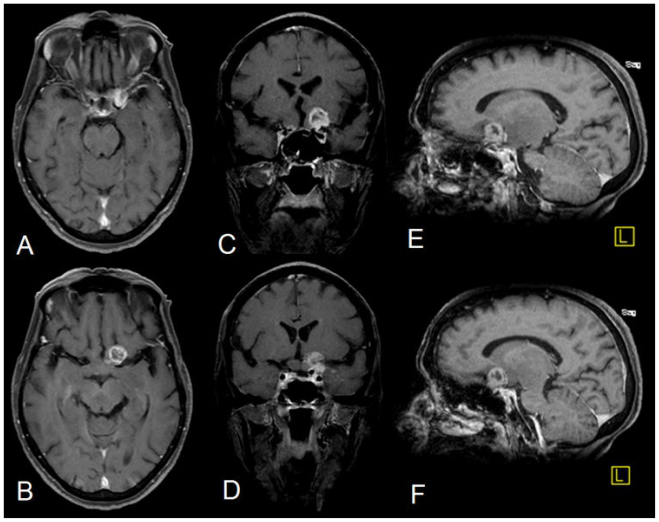
图3
68岁女性患有视神经胶质母细胞瘤。后对比T1W(TR = 845,TE = 9,SL 5mm)轴向(A和B),冠状(TR = 825,TE = 11,C&D)和下垂。(TR = 825,TE = 9,E&F)注射20cc 0.3mmol / kg Gadodiamide(OMNISCAN,GE医疗保健)后,显示小的异质环增强焦点,在左侧视神经上方,左侧颞侧脑膜增强。在视神经,束和通路中没有看到增强。

图4
68岁女性患有视神经胶质母细胞瘤。对比后T1W轴向图像显示病变的其余部分没有显着增强。
在多个位置(TE 30,135和270 ms)拍摄的病变的SV MR光谱显示Cho升高,Cho / NAA比率升高(1.3-1.9)。(图5)
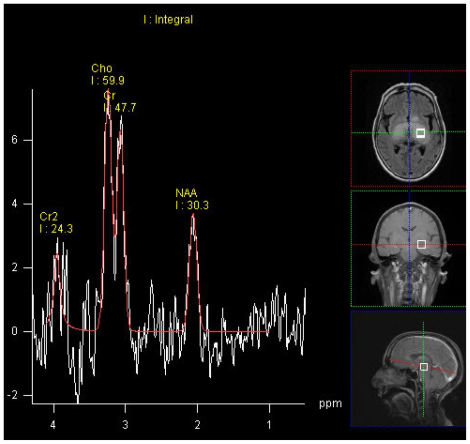
图5
68岁女性患有视神经胶质母细胞瘤。左侧丘脑(TE 135 ms)病灶的SV MR光谱显示Cho升高,Cho / NAA比值升高(1.3 - 1.9)。
然后将患者收集进行开放式活组织检查。使用左翼点入路,可以看到一个柔软且边界清晰的大型轴外粉红色肿瘤。然后凝固肿瘤表面并进入。它是血管,很容易被吸入。它扩展了后内侧。最后,进行了大量的活组织检查。
活组织检查的组织病理学检查(图6)显示脑组织具有不同程度的细胞构成,特征性细胞形态,丰富的有丝分裂图,增加的血管分布和肿瘤坏死的多灶性区域,与多形性胶质母细胞瘤的诊断一致。
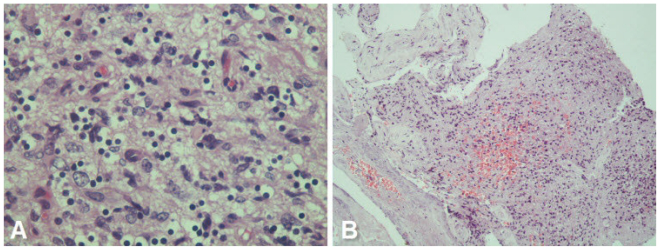
图6
68岁女性患有视神经胶质母细胞瘤。A-显微镜下显示原纤维背景中的间变性肿瘤细胞 - 肿瘤细胞显示出丰富的细胞质清除 - 有点像“煎蛋”外观。然而,细胞多形性显着(H&E,400X)。B-显微镜照片显示肿瘤组织内的局灶性坏死和出血(H&E,100X)。
胶质瘤占全部原发性和转移性颅内肿瘤的40-50%。胶质母细胞瘤是较常见的胶质瘤类型。WHO 2000分类对从I级到IV级的星形细胞肿瘤进行评分。WHO I级肿瘤包括毛细胞星形细胞瘤,多形性黄色星形细胞瘤和室管膜下巨细胞星形细胞瘤。其他星形细胞瘤包括弥漫性星形细胞瘤(II级),间变性星形细胞瘤(III级)和胶质母细胞瘤(IV级)。
除非出现出血或钙化,否则胶质瘤通常在T2w图像上显示高信号强度并且在T1w图像上显示低信号强度。低级星形细胞瘤(WHO I级和II级)倾向于明确定义,非出血性并且表现出很小的质量效应,血管源性水肿或异质性。间变性星形细胞瘤(WHO III级)定义不太明确,并且表现出适度的质量效应,异质性和水肿,具有不同程度的增强。胶质母细胞瘤(WHO IV级)定义不明确,并且通常具有相当大的质量效应,血管源性水肿,出血和异质性。不规则环状强化与结节和坏死灶是胶质母细胞瘤的典型。
除了常规和对比MR之外,还在扩散加权图像,MR灌注和MR光谱的基础上进一步尝试了胶质瘤分级。
DW图像上胶质瘤的信号强度是可变的(超 - ,等 - 或低信号)。肿瘤细胞性可能是脑肿瘤ADC值的主要决定因素。尚未发现ADC值在个别病例中可靠地区分神经胶质瘤类型。DW图像和/或ADC图对于区分恶性胶质瘤患者的肿瘤细胞浸润和肿瘤周围水肿也不可靠。
磁共振波谱显示胶质瘤中Cho值增加,NAA / Cho和Cr / Cho比值与脂质 - 乳酸峰值相关。一项研究表明,当标准化为水时,特定代谢物在将肿瘤分为三类中具有诊断价值。具体地,乳酸/水比率可用于区分GBM,间变性星形细胞瘤和低度恶性肿瘤。胆碱/水,胆碱/肌酸和乳酸/肌酸比率可用于区分高级别和低级别肿瘤。
MR灌注研究显示相对脑血容量与肿瘤分级之间存在相关性。
视神经通路的胶质瘤分类为(a)相对良性的视神经胶质瘤(通常发生在儿科年龄组)和(b)成年期的恶性视神经胶质瘤。良性视神经胶质瘤占眼眶肿瘤的4%,颅内胶质瘤的4%和颅内肿瘤的2%。它们也占全部原发性视神经肿瘤的三分之二。
良性视神经胶质瘤更常见,被认为是低级星形细胞瘤。有10%~38%的儿童视神经胶质瘤患者有NF-1; 相反,15-40%的NF-1儿童患有视神经胶质瘤。双侧视神经胶质瘤几乎是NF-1的特征。
另一方面,成人的恶性视神经胶质瘤是较其少见的视神经通路肿瘤。到1990年,本世纪只报告了30例。在最近由Bettina Wabbles等人于2004年对文献进行的综述中,已经描述了45例成人恶性视神经胶质瘤。在这些患者中,51%是男性,49%是女性; 诊断时的平均年龄为54岁(中位数为59岁,范围为22至79岁)除了视交叉和视神经外,发现恶性视神经胶质瘤的发生部位为50%的下丘脑患者中,颞叶占22.5%,基底神经节占15%。其他更少见的部位是中脑,顶叶皮质,小脑和颈椎,胸椎和腰椎蛛网膜下腔。没有报道与成人视神经胶质母细胞瘤的神经纤维瘤病有关。成年期恶性视神经胶质瘤在病理学上被分类为间变性星形细胞瘤或多形性胶质母细胞瘤。在成人中,恶性视神经胶质瘤很少见并且很快致命视觉通路肿瘤。Dodge等人于1958年提出了OPG的解剖分类,将肿瘤定义为仅涉及视神经(1阶段),有或没有神经受累的交叉(2阶段),以及下丘脑或其他相邻结构(3阶段) 。修改后的道奇分类进一步将阶段1分为阶段1a(即单个视神经受累),1b(双侧视神经受累),1c(视神经的脑池段)。阶段2分为2a(中心交叉)和2b(非对称交叉)。阶段3a是视神经束受累,3b是不对称的束受累。4阶段是弥漫性后路受累,4b阶段是不对称的后路受累。下丘脑受累)。
到目前为止报告的大多数病例显示出视神经/交叉或视神经通路的显着增强。在这种不同情况下,没有增强光学神经/通路。
成年期的大多数视神经胶质瘤最初显示出一种视神经的某种程度的增大和增强。随着进展,视交叉变得复杂,然后肿瘤扩散到对侧视神经并随后扩散到视神经通路。在临床过程中可能出现的下丘脑受累症状,例如多尿和烦渴,表明下丘脑的继发性侵袭。
我们的病例中的症状和临床表现遵循Hoyt等人定义的成人恶性视神经胶质瘤综合征的模式。在这种综合征中,通常会引起对眶内肿块的怀疑的体征不存在,或者,如果存在,则在临床过程的晚期发生并且程度较轻。在成年期恶性视神经胶质瘤综合征中,视力的逐渐丧失,视网膜中央静脉和/或动脉闭塞以及单眼失明迅速发生,如我们的情况所发生的那样。
从临床角度来看,呈现时的单眼视力丧失意味着视神经的起源,而呈现时的双侧视觉变化意味着视神经的起源。
涉及视交叉的视神经通路的胶质母细胞瘤可能显示出对下丘脑,基底神经节和内囊的连续扩散。还报道了成年期恶性视神经胶质瘤向内侧颞叶和脑干的软脑膜和皮下扩散。我们的病例显示左侧颞区的细致软脑膜增强。其中一个病例报告显示左侧颞叶增强的局灶性病变,左侧视神经扩张增强,交叉的左侧外侧和左侧视神经通路。在我们的病例中可以看到类似的增强中央坏死病变。
可用于成年期视神经胶质瘤的治疗选择包括手术,放射和化疗。但治疗结果并不令人鼓舞,并且总是被认为是一种致命的疾病。从出现时起的平均生存期通常不到1年。患者存活了两个月,然后失去了随访。




