脑干胶质瘤(BSG)约占全部儿童中枢神经系统肿瘤的10-20%。它们大致分为两组:低级别(或局灶性/外生性)脑干胶质瘤和弥漫性固有脑桥神经胶质瘤(DIPG),包括那些经组织学证实的或仅用放射学诊断的。弥漫性肿瘤是典型的浸润性星形细胞瘤,根据组织病理学特征可分为2-4级,与局灶性星形细胞瘤相比预后较差。这些类型的脑干胶质瘤通常来自脑桥,但也可能发生在其他部位。当它们起源于脑桥时,它们被称为DIPGs,通常代表80%的BSG患者。
每天分次外照射治疗6周是儿科高级别脑干胶质瘤的标准疗法,并且经常提供替莫唑胺化疗。Hart等人的Cochrane系统综述和荟萃分析表明,在对患有高级别神经胶质瘤的成年人进行的研究中,使用替莫唑胺可提高生存率(死亡风险比为0.6,95%CI为0.46–0.79)。尽管之前尚未完成对涉及化疗治疗的儿科研究的荟萃分析,但增加化疗似乎并不能明显提高脑干神经胶质瘤的存活率。
已经假设某些特征可能是预后性的。这包括诊断前症状的持续时间,诊断时年龄不到3岁,组蛋白H3突变,以及ACVR1突变。关于使用化疗、免疫疗法、替代性放疗(包括1、2和3期试验)的研究未能证明结果有任何好转。
儿童高级别脑干胶质瘤生存研究
这个综述纳入了65项研究(2336名参与者)。荟萃分析显示1年总生存率(OS)为41%,2年OS为15.3%,3年OS为7.3%。
《Survival rates and prognostic predictors of high grade brain stem gliomas in childhood: a systematic review and meta-analysis》这是一个多方位系统的文献综述,试图总结高级别脑干胶质瘤患者的生存结果。对1151篇引文进行了系统搜索,包括66篇论文(2279名参与者),证实这些肿瘤的总体存活率低。没有足够的数据对5年和5年以上的OS进行汇总分析。
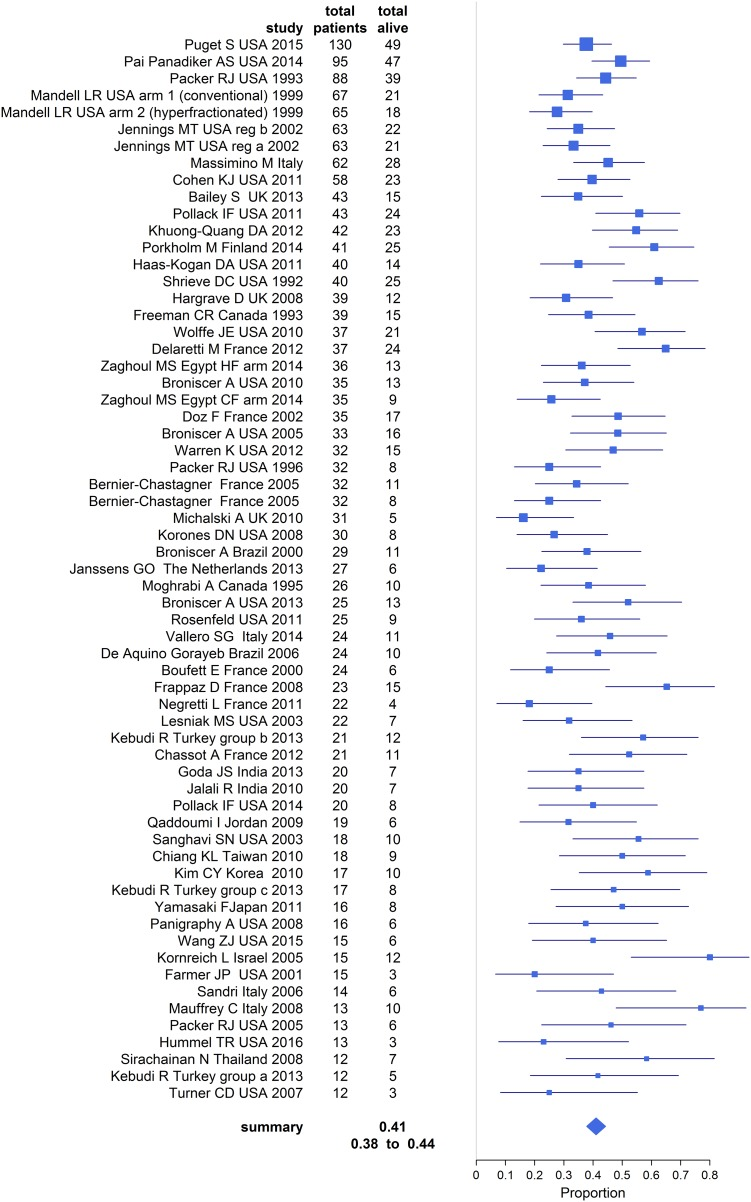
图1:1年总生存率的汇总估计值
儿童高级别胶质瘤1年总生存率研究结果(表2)
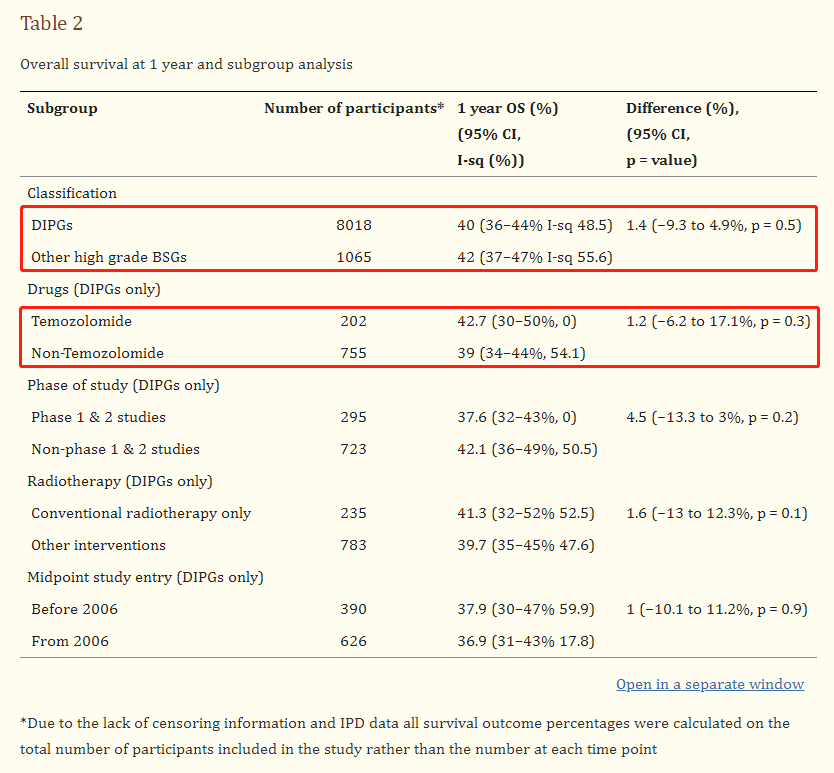
表2:1年总生存率和亚组分析
James T.Rutka教授:小儿脑胶质瘤的新分子靶点和治疗方法
INC旗下世界神经外科顾问团(WANG)的专家成员James T.Rutka教授在论文《New Molecular Targets and Treatments for Pediatric Brain Tumors》中表示:我们现在正面临下一代(Next-Gen)测序时代,它将为深入了解每种瘤种中信号传导途径异常提供更多信息。驱动突变的鉴定将使人们更好地了解肿瘤发生,并导致建立更准确的临床前模型。此外,大批肿瘤群的转录组,遗传和表观遗传学事件的谱图最终将为特定亚组的起源细胞提供一些信息,并且也是肿瘤生发,维持和发展的重要驱动因素。
在临床方面,这种知识将使患者分为适当的风险组,并根据每个肿瘤的基因组情况定制治疗方案。在本文中,Rutka教授将介绍常见的小儿脑肿瘤的分子基因组学的较新进展及其对临床的预后意义和相关性。我们还将重点介绍使用分子靶向疗法的较新临床试验,并讨论治疗小儿脑癌的其他可能途径。
1.星形细胞瘤
毛细胞星形细胞瘤(PA)的一线治疗是手术切除。尽管大多数患有这些肿瘤的儿童可以生存很长一段时间,但有些儿童会复发,特别是如果肿瘤切除不完全的话。复发和进行性肿瘤可用放射和/或化学疗法治疗,但直到最近,人们对复发和恶性转化的机制仍知之甚少。
早期对PA中染色体畸变的研究表明,大多数情况下染色体核型正常。5号染色体,7号染色体和7q染色体的三体性是一些发现的少数细胞遗传学异常。Pfister等人使用基于阵列的比较基因组杂交(array-CGH)。研究了一系列儿科低度星形细胞瘤以及这些肿瘤中未发现的丝裂原活化蛋白激酶(MAPK)激活机制。作Rutka教授在超过50%的PA中发现了BRAF基因位点(7q34)的串联重复,并且在较小比例)的肿瘤中发现了BRAF激活突变V600E(在热点密码子上缬氨酸转变为谷氨酸)。
后来,证明了BRAF的组成性激活是由于一个新基因(KIAA1549)和BRAF癌基因之间的融合所致,而且这种融合还与不完全切除的低度星形细胞瘤的临床疗效更好有关。在PA中,其他较少见的报道的基因融合包括BRAF与FAM131B基因的融合以及Raf激酶家族成员(RAF1)和SLIT-ROBO Rho GTPase激活蛋白3(SRGAP3)基因之间的融合。BRAF和异柠檬酸脱氢酶1(IDH1)的组合分析对弥漫性星形细胞瘤(WHO II级)分离的PA表现出敏感性和特异性。
PAs中有70%的病例含有KIAA1549:BRAF融合,但没有IDH2或IDH2突变,而弥漫性星形细胞瘤则有76%的病例具有IDH1突变,但没有BRAF融合。肿瘤位置与MAPK改变类型之间也存在有趣的相关性。颅后窝肿瘤通常会增加KIAA1549:BRAF融合的发生率,而幕上肿瘤的BRAF V600E发生率较高突变。文献中报道的大约80-90%的PA病例在MAPK途径中至少有一种改变。有趣的是,MAPK途径中描述的全部变化似乎都是互斥的,这表明单个点击可能足以诱导转化。
随着大多数PA中MAPK途径的组成性激活和BRAF改变的发现,人们越来越有兴趣将这些靶物用于新型治疗方法。目前正在进行许多I期和II期临床试验,以测试MAPK的小分子控制剂及相关途径(表1)。
2.胶质母细胞瘤
多形胶质母细胞瘤(GBM)是成人中常见的脑肿瘤,在儿科人群中发病率较低。尽管神经外科和神经肿瘤学有所好转,但即使采用的治疗方案,被诊断患有GBM的儿童仍具有令人沮丧的结果,存活率低。尽管小儿和成年GBM的组织学看起来相同,但这些肿瘤的分子生物学却不同。因此,针对儿童GBM的合适疗法的开发可能不应该依赖于成人肿瘤的进展。
在成人恶性神经胶质瘤中,磷酸酶和张力蛋白同源物(PTEN)的突变以及EGFR的扩增很常见,但在儿科患者中较少见。然而,与小儿低度神经胶质瘤相比,小儿GBMs的EGFR表达显着较高,尽管没有报道突变且EGFRvIII缺失少(〜17%)。虽然在成人GBM中的AKT通路的激活的结果PTEN突变,儿童肿瘤这些都是少见的,虽然AKT和其与生存的关联较差的过度表达有报道。Bax等人在一项涉及大量小儿高级别神经胶质瘤(HGG)(37个肿瘤样本中有37个GBM)的研究中。
确定PDGFRα扩增和细胞周期蛋白依赖性激酶控制剂2A/B(CDKN2A/B)缺失是较常见的病灶。有趣的是,具有高级别肿瘤和稳定基因组特征的患者具有更好的生存率,而与组织学等级或类型无关。多项研究表明,IDH1突变常见于成人继发性GBM(98%),在儿科GBM中很少见。TP53(肿瘤蛋白53)小儿高度恶性肿瘤中报道有突变,年龄较大的儿童(40%)与少于3岁的儿童(12%)相比,发生频率更高。p53而不是TP53突变的过表达也与5年无进展生存期的显着降低有关。
最近的一项研究使用高分辨率单核苷酸多态性(SNP)阵列来鉴定小儿GBM中的新型染色体改变,包括7q21-22和1q43-44的扩增以及15q15.1-15q23和17p13-17p11.2中杂合性(LOH)的丧失。参与细胞周期调控和细胞死亡途径的基因是LOH的主要靶标。
已经表明,在HGG中少见的是O 6-甲基鸟嘌呤-DNA甲基转移酶(MGMT)的过表达,但是也有报道说,它与儿童的总体生存能力差有关。的MGMT基因编码DNA修复酶,可以降低烷化剂的功效。当MGMT基因被启动子甲基化沉默时,肿瘤组织中的DNA修复受到损害,患者的存活率更高。
最后,最近的一项研究发现了小儿GBM中遗传事件和表观遗传事件之间有趣的相互作用。教授对48例小儿GBM进行了全外显子测序,发现44%的肿瘤在染色质重塑途径的基因中存在体细胞突变,包括组蛋白H3基因(H3F3A),α地中海贫血/智力低下综合征X连锁(ATRX)基因和死亡域相关蛋白(DAXX)基因。有趣的是,发现H3F3A突变是GBM特有的,在儿科人群中更为普遍。此外,H3F3A和/或ATRX的全部病例中有54%和患者中有86%突变,还显示出TP53体细胞突变。
参考文献:James T.Rutka.New Molecular Targets and Treatments for Pediatric Brain Tumors.2012




