脊索瘤(CHs)是具有良性组织病理学的肿瘤,但表现出具有侵袭性和转移性的侵略性临床行为。脊索瘤在治疗肿瘤方面具有挑战性,仍然存在许多问题,是关于其最佳治疗方法。我们可以通过手术治疗令病例延迟复发,但10年或20年后复发是不可避免的。
然而,在过去的十年里,我们取得了重要的进步。首先,随着新技术的发展,如鼻内镜颅底入路(EEA),手术切除的范围得到了提高,这是重要的,因为肿瘤的完全切除仍然是较重要的预后因素。二,基于对脊索瘤癌变过程中相关信号通路的更深入了解,互补靶向化疗正在开发中。需要明确的是,初诊时应行根治性切除术。现在,无论是否完整的切除术,均未明确证明其疗效,目前已常规提出了不论切除质量如何的补充质子治疗。
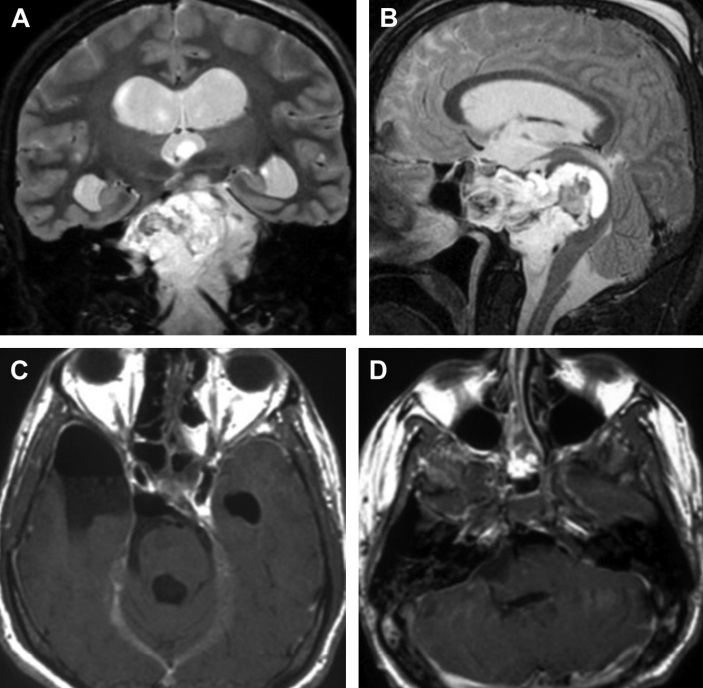
脊索瘤手术治疗
INC旗下世界神经外科顾问团(WANG)的专家成员Sebastien Froelich教授在论文中表示:手术是较为合适的治疗方法,因为完全切除仍然是较为重要的预后因素。考虑到CH的中线位置、起始骨和硬膜外位置,不穿过颅神经和血管的前入路是较为合理的,应优先考虑。长期采用经口、经蝶窦、经面入路。
如今,EEAs正在取代它们。使用内窥镜,可以从鞍背(经垂体转位)到鞍背下尖甚至颅颈交界(CCJ)到达斜坡的任何部分。侧限为静脉结构(海绵窦和颈静脉球)、中枢神经系统和动脉(颈动脉和椎动脉)。微多普勒和神经导航在这些情况和复发性脊索瘤的治疗中都是必需的。对中枢神经系统特别是中枢神经六、十二中枢的监测,也为手术切除带来了顺利保障。气球阻塞测试(BOTs)也可能是一个顺利的术前选择,偶尔会导致术前或术中闭塞。在复发病例中,以往的放疗也增加了脑脊液(CSF)泄漏的风险。如果没有其他缝合方法,颞顶筋膜瓣可以挽救患者的生命。尽管近年来缝合技术有了进步,但术后脑脊液漏的发生率仍然在10%左右,所以要求主刀医生有着丰富的临床经验和预判能力。
脊索瘤补充治疗
关于辅助放射治疗的合适性还存在一些争议。有些研究人员只在术后残留的情况下使用它,有些则在任何情况下,无论切除的程度如何。各种类型的放射治疗已被使用:分割放射治疗,伽玛刀,射波刀,质子治疗,和碳离子治疗。后两种类型通常被认为是合适的,因为它们具有强大的生物学效应,并且即使在靠近重要敏感结构的情况下,也有可能对肿瘤提供高剂量治疗。
在Di Maio的meta分析中,150例接受补充放疗的患者中,不同类型放疗的5年OS和PFS无统计学差异;在10年之后,碳离子疗法的疗效有了细微的差异。在作者系列中,23个质子束治疗应用尽可能多(70%的病例);在精算曲线上,对SB和颅颈交界处脊索瘤,手术后质子束治疗被证明有利于OS和PFS (P=5.04和0.03),但对整个系列无效(P=5.05和0.29)。还发现了一个重要的问题:与不完全切除或不切除质子治疗相比,完全切除加质子束治疗似乎好转了OS和PFS (P=5.01和0.003);在6.5年的随访中,复发率为26%对50%,死亡率为7%对50%。
INC之法国Sebastien Froelich教授在文末总结道:尽管我们正在在了解脊索瘤方面已经取得了进展,但治疗病变和致命肿瘤具有挑战性。脊索瘤的生发位置对预后有影响。然而,每个脊索瘤的生物学行为的标记物仍然是需要的,以便能够调整治疗策略以适应肿瘤的侵袭性。全部的脊索瘤都应在初次发病时进行根治性切除,因为切除的范围是较好的预后因素。无论切除质量如何,补充质子治疗现在都被提及,即使它的疗效并不是在每个病例中都被清楚地证明,特别是在不完全切除的病例中。国内脊索瘤患者如对病情有所疑惑,或希望治疗更为顺利保险,可咨询INC国际专家远程咨询,以明确是否能由其主刀手术以及后续是否接受质子治疗。
参考文献:Sebastien Froelich. Chordomas: A Review. 2015




